Х-сцепленный лимфопролиферативный синдром
Х-сце́пленный лимфопролиферати́вный синдро́м (ХЛПС; синдро́м Дунка́на) — редкое наследственное заболевание из группы первичных иммунодефицитов. Его основу составляет генетическая мутация в гене SH2D1A, XIAP и MAGT1 приводящих к нарушению регуляции иммунного ответа. Ключевой особенностью синдрома является аномально тяжёлая реакция организма на инфицирование вирусом Эпштейна — Барр. Клиническая картина характеризуется развитием фульминантного инфекционного мононуклеоза, возникновением лимфопролиферативных заболеваний и дисгаммаглобулинемии. В качестве лечения применяется симптоматическая терапия, а радикальным методом является трансплантация гемопоэтических стволовых клеток[1].
Что важно знать
История
В середине 1970-х годов американский врач Дэвид Пуртило и его коллеги описали случай семьи, где шестеро из восемнадцати мальчиков скончались от лимфопролиферативного заболевания. У пациентов наблюдалось аномальное размножение клеток крови и нарушения в концентрации иммуноглобулинов. Исследователи выдвинули гипотезу, что неконтролируемое размножение лимфоцитов было спровоцировано вирусом Эпштейна — Барр, а причиной процесса стала ослабленная функция Т-клеток, которая привела к неограниченной лимфопролиферации. Это заболевание получило название синдром Дункана по фамилии исследуемой семьи. Молекулярная основа болезни была обнаружена лишь в 1998 году, когда учёные выявили лежащие в его основе ХЛПС 1-го типа мутации в гене SH2D1A[1][2].
Классификация
Согласно международной классификации первичных иммунодефицитов, разработанной Международным союзом иммунологических обществ, ХЛПС относится к категории заболеваний, связанных с нарушением регуляции иммунного ответа, а именно к группе иммунодефицитов с повышенной предрасположенностью к инфицированию вирусом Эпштейна — Барр и развитию лимфопролиферативных заболеваний. В зависимости от генетической мутации выделяют 3 типа заболевания[2][3]:
- ХЛПС 1-го типа вызывается мутацией гена SH2D1A. Данный ген кодирует белок SAP, функция которого заключается в передаче сигнала активации от SLAM-подобных рецепторов внутрь клетки;
- ХЛПС 2-го типа возникает из-за мутации гена XIAP. Этот ген является ингибитором каспаз 3, 7 и 9, следовательно, он играет ключевую роль в подавлении процесса клеточной гибели (апоптоза);
- ХЛПС 3-го типа обусловлен мутацией гена MAGT1. Этот ген отвечает за транспорт свободных ионов магния в клетку.
Этиология
Известно три гена, мутации в которых вызывают проявления ХЛПС: SH2D1A, XIAP (также известный как BIRC4) и MAGT1. Все подтипы XЛП объединены в одну группу по двум основным критериям: во-первых, из-за наследования по Х-сцепленному типу, и во-вторых, из-за схожести клинической картины. Заболевание наследуется Х-сцепленным рецессивным путём[3].
Патогенез
Патогенез заболевания зависит от его конкретного его типа[3]:
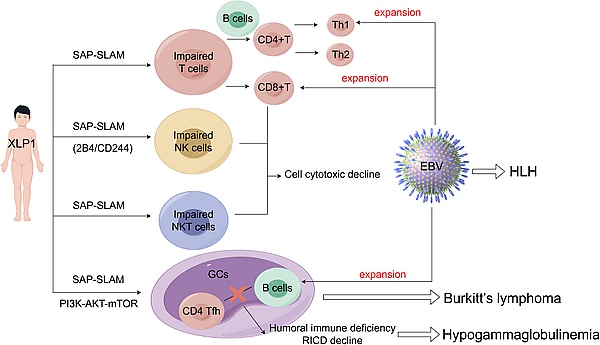
- Патогенез ХЛПС 1-го типа обусловлен мутацией в гене SH2D1A, который кодирует SLAM-ассоциированный белок. Этот белок является ключевой адаптерной молекулой, обеспечивающей передачу сигнала от семейства рецепторов SLAM внутрь клетки. Отсутствие или дефект SAP приводит к комплексным нарушениям в работе иммунитета[3]:
- во-первых, нарушается клеточный иммунитет и цитотоксичность. Снижается цитотоксичность NK-клеток, так как без SAP нарушается их активация и выработка интерферона-γ. Также страдает избирательная цитотоксичность CD8+ T-лимфоцитов против клеток, презентирующих антиген, особенно В-клеток, что объясняет специфическую предрасположенность к инфекции вируса Эпштейна — Барр и В-клеточным лимфомам. Характерным признаком является резкое снижение или полное отсутствие NK-клеток, что также вносит вклад в неадекватный иммунный ответ;
- во-вторых, возникают нарушения гуморального иммунитета и формирования иммунной памяти. Белок SAP критически важен для установления стабильного контакта между T-хелперами и B-клетками. В его отсутствие нарушается процесс дифференцировки наивных B-клеток в плазматические клетки и B-клетки памяти, что приводит к уменьшению количества B-клеток памяти, гипогаммаглобулинемии и неспособности формировать высокоаффинный гуморальный ответ;
- в-третьих, нарушается регуляция иммунного ответа и контроль лимфопролиферации. SLAM-путь задействован в механизме запрограммированной клеточной гибели, индуцированной избыточной стимуляцией. Дефект этого механизма приводит к неконтролируемой пролиферации CD8+ T-клеток в ответ на инфекцию, что является прямой причиной развития жизнеугрожающих состояний, таких как лимфопролиферация и гемофагоцитарный лимфогистиоцитоз.
- Патогенез ХЛПС 2-го типа связан с мутацией в гене XIAP, который кодирует одноимённый цитоплазматический белок, выступающий физиологическим ингибитором каспаз 3, 7 и 9 и, следовательно, ключевым ингибитором апоптоза. В результате его дефицита лимфоциты становятся подвержены избыточной гибели, что, в частности, проявляется характерным снижением количества NK-клеток, которые особенно чувствительны к апоптозу. Помимо своей основной антиапоптотической роли, белок XIAP опосредует сигнальный путь через рецепторы NOD1/2 и Dectin-1, которые распознают бактериальные и грибковые антигены. В норме активация этих рецепторов запускает выработку цитокинов, критически важных для противомикробной защиты и поддержания гомеостаза кишечника. При дефиците XIAP эта продукция нарушается. Одновременно из-за повышенного апоптоза страдают регуляторные популяции лимфоцитов, поддерживающие баланс в слизистой оболочке, — регуляторные Т-клетки, MAIT-клетки и NK-клетки. Совокупность этих дефектов — нарушение цитокинового ответа и утрата иммунных регуляторов — лежит в основе развития воспалительного заболевания кишечника у пациентов с XЛП2. Отсутствие антиапоптотического сигнала от XIAP не позволяет активированным Т-клеткам выживать и пролиферировать для эффективной борьбы с инфекцией, что приводит к её персистенции. Параллельно дефицит XIAP снимает тормоз с образования инфламмасомы в макрофагах и дендритных клетках, что вызывает чрезмерную выработку провоспалительных интерлейкинов. Сочетание персистирующей инфекции и неконтролируемого системного воспаления в конечном итоге и провоцирует развитие жизнеугрожающего гемофагоцитарного лимфогистиоцитоза.
- Патогенез ХЛПС 3-го типа связан с мутацией в гене MAGT1, который кодирует компонент магниевого канала. Этот ген экспрессируется во всех клетках, но особенно сильно в гематопоэтических. Потеря функции гена MAGT1 в Т-лимфоцитах приводит к нарушению быстрого притока свободных ионов магния в клетку, что является критическим звеном для полноценной активации T-клеточных рецепторов после контакта с антигеном. В цитотоксических CD8+ Т-лимфоцитах и NK-клетках дефицит магния вызывает снижение базальной экспрессии ключевых активирующих рецепторов, что в совокупности ослабляет противоопухолевый и противовирусный иммунный надзор. Это объясняет высокую предрасположенность пациентов к персистенции вируса Эпштейна — Барр и развитию ассоциированных с ним лимфом. Важной особенностью синдрома является то, что дефект активации Т-клеток может быть компенсирован более длительной или сильной стимуляцией. Этим объясняется относительно мягкое течение заболевания по сравнению с другими первичными иммунодефицитами: для ХЛПС 3-го типа не характерно развитие фульминантного мононуклеоза, редко наблюдается гемофагоцитарный лимфогистиоцитоз, а количество NK-клеток остаётся в норме.
Эпидемиология
ХЛПС является крайне редким заболеванием, его распространённость примерно 1 случай на 1 млн человек. На территории России описан лишь один клинический случай. ХЛПС проявляется преимущественно у лиц мужского пола[1]
Диагностика
Заболевание характеризуется тремя основными вариантами клинического течения, среди которых наиболее распространённым, встречающимся более чем у половины пациентов, является фульминантный инфекционный мононуклеоз. Два других типа представлены дисгаммаглобулинемией и лимфопролиферативной болезнью[1]:
- фульминантный инфекционный мононуклеоз представляет собой жизнеугрожающее состояние, возникающее вследствие неконтролируемого иммунного ответа на вирусную инфекцию, что приводит к массивной пролиферации цитотоксических Т-лимфоцитов, В-клеток и макрофагов. Клиническая картина включает выраженное увеличение лимфоузлов и печени с селезёнкой, развитие острого гепатита и некроза печёночной ткани, менингоэнцефалита и угнетения костномозгового кроветворения. Помимо этого, наблюдается полиорганное поражение с некрозом селезёночной пульпы, миокардитом и интерстициальным нефритом;
- дисгаммаглобулинемия проявляется стойким снижением концентрации иммуноглобулинов класса G, что создаёт состояние иммунодефицита и предрасполагает к частым рецидивирующим инфекциям;
- лимфопролиферативная болезнь в большинстве случаев реализуется в виде развития В-клеточной лимфомы.
Существенным отличием ХЛПС 2-го типа является развитие воспалительного заболевания кишечника, гистологически сходного с болезнью Крона. Этот тип ХЛПС относится к моногенным заболеваниям с поражением желудочно-кишечного тракта, для которых характерно раннее начало воспалительного процесса в кишечнике[3].
Среди редких проявлений ХЛПС 1-го типа описываются апластическая анемия, лимфоидный васкулит и лимфоидный гранулёматоз лёгких. Для ХЛПС 2-го типа к редким симптомам относятся аутовоспалительные процессы, такие как артрит, увеит и узловатая эритема[3].
Клиническая картина заболевания может быть представлена как одним из перечисленных состояний, так и их комбинацией, причём проявления могут значительно различаться даже среди членов одной семьи[3].
Для пациентов с ХЛПС, особенно при ХЛПС 2-го типа с проявлениями колита, характерно отставание в физическом развитии, затрагивающее массу и рост тела. Частым неспецифическим симптомом являются немотивированные подъёмы температуры, как в виде длительного субфебрилитета, так и лихорадочных эпизодов без чёткого инфекционного очага, что может отражать скрытое течение гемофагоцитоза. Кроме того, лихорадка в сочетании с ночной потливостью и потерей веса служит тревожным признаком, указывающим на возможное развитие злокачественного процесса, например, лимфомы[3].
Со стороны кожных покровов у пациентов с ХЛПС 1-го и ХЛПС 2-го типа могут наблюдаться пятнисто-папулёзные высыпания, характерные для гемофагоцитарного лимфогистиоцитоза. При развитии цитопений, в частности тромбоцитопении, появляется геморрагическая сыпь. Для ХЛПС типичная либо генерализованная лимфаденопатия, либо локальное увеличение одной группы лимфоузлов при формировании лимфомы[3].
Клинический анализ крови: характерны явления лимфопении, анемии, тромбоцитопении и нейтропении[3].
Биохимический анализ крови: характерно повышение концентрации ферритина, триглицеридов, повышение активности лактатдегидрогеназы, снижение концентрации фибриногена, гипоальбуминемия[3].
Иммуноферментный анализ: возможно повышение концентрации IgA, IgG, IgM[3].
Проточная цитометрия: для пациентов с ХЛПС 1-го и ХЛПС 2-го типа характерно полное отсутствие или снижение экспрессии белков SAP и XIAP соответственно[3].
Молекулярно-генетический анализ: характерно выявление мутаций в генах SH2D1A, XIAP и MAGT1 при первом, втором и третьем типе заболевания соответственно методом секвенирования или полимеразной цепной реакции[3].
Гистологическое исследование биоптата: проводят при поражении желудочно-кишечного тракта[3].
Гастроскопия и колоноскопия: проводятся при поражении желудочно-кишечного тракта для уточнения характера поражения[3].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими заболеваниями[2][4]:
- гемобластозы;
- недостаточность Х-сцепленного ингибитора апоптоза;
- апластические состояния костного мозга;
- первичный гемофагоцитарный лимфогистиоцитоз;
- системные заболевания соединительной ткани;
- инфекционный мононуклеоз;
- детский мультисистемный воспалительный синдром;
- сепсис;
- синдром Чедиака — Хигаси;
- синдром Грисцелли;
- семейный гемофагоцитарный лимфогистиоцитоз;
- другие формы первичных иммунодефицитов
Осложнения
Основным осложнением является развитие оппортунистических инфекций[5].
Лечение
В рамках терапии инфекции, вызванной вирусом Эпштейна — Барр, может применяться противовирусная терапия такими препаратами, как ганцикловир, а также внутривенные иммуноглобулины. С целью контроля лимфопролиферации используется ритуксимаб, действие которого направлено против В-лимфоцитов. При развитии у пациента лимфомы лечение проводится по стандартным протоколам химиотерапии[1].
Единственным известным методом радикального лечения XЛП является аллогенная трансплантация гемопоэтических стволовых клеток. Данную процедуру настоятельно рекомендуется рассматривать для всех пациентов мужского пола как можно раньше, в идеале до появления симптомов заболевания. В то же время проведение трансплантации не показано бессимптомным женщинам-носительницам мутации[4].
Прогноз
Прогноз при ХЛПС без проведения радикального лечения остаётся неблагоприятным. Согласно данным исследований, выживаемость таких пациентов не превышает 20 %, причём более половины мальчиков погибают в возрасте до десяти лет. Существенное улучшение прогноза достигается с помощью трансплантации гемопоэтических стволовых клеток, которая позволила снизить общую смертность от этого заболевания с 75 % до 29 %[1][2].
Диспансерное наблюдение
Пациентам с ХЛПС рекомендуется наблюдение педиатра, гематолога, гастроэнтеролога, ревматолога с целью раннего выявления возможных осложнений, предупреждения развития рецидивов имеющихся заболеваний и контроля общего состояния. Сроки проведения лабораторных и инструментальных методов диагностики следующие[2][3]:
- Лабораторные исследования:
- клинический анализ крови с лейкоформулой: 1 раз в месяц (чаще при инфекциях, лихорадке);
- биохимический анализ крови (печёночные ферменты, С-реактивный белок): 1 раз в месяц;
- клинический анализ мочи: 2 раза в год + при интеркуррентных заболеваниях.
- Инструментальные исследования:
- электрокардиография: 1 раз в год;
- ультразвуковое исследование органов брюшной полости и почек: 1 раз в 3 месяца;
- эхокардиография: 1 раз в 3 месяца;
- рентгенография грудной клетки: 1 раз в год.
- Консультации специалистов:
- иммунолог: 1 раз в 3 месяца;
- гематолог: 1 раз в 3 месяца;
- невролог: 1 раз в 6 месяцев;
- окулист: 1 раз в 6 месяцев;
- отоларинголог: 1 раз в год;
- стоматолог: 1 раз в год.
Профилактика
Для долгосрочной профилактики осложнений заболевания показано регулярное введение внутривенных иммуноглобулинов, которое в некоторых случаях комбинируют с ритуксимабом[1].
В целях профилактики ХЛПС проводится медико-генетическое консультирование семей, которое включает проведение пренатальной или преимплантационной диагностики. Данный метод основан на молекулярно-генетическом исследовании биоптата хориона для выявления мутации в соответствующем гене, что позволяет предотвратить рождение детей с данным заболеванием в семьях группы риска[3].
Примечания
Литература
- Балашов Д.Н., Роппельт А.А., Румянцев А.Г., Щербина А.Ю. Первичный иммунодефицит - Х-сцепленный лимфопролиферативный синдром. ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ, 2020 г // Российский Аллергологический Журнал. — 2019. — Т. 16, № 4. — С. 66—77. — doi:10.36691/RAJ.2020.16.4.008.
- Матрос Е.С., Карицкая А.И. Х-сцепленный лимфопролиферативный синдром, осложнённый гемофагоцитарным лимфогистиоцитозом и болезнью Крона: клинический случай // Педиатрическая фармакология : Журнал. — 2023. — Т. 20, № 1. — С. 63—68. — doi:10.15690/pf.v20i1.2522.
- Масленников Д. Н. Синдром Дункана (рус.). Генокарта — генетическая энциклопедия. (19 мая 2022).Дата обращения: 6 октября 2025.