Ангиоиммунобластная Т-клеточная лимфома
Ангиоиммунобла́стная Т-кле́точная лимфо́ма (АИТЛ; ангиоиммунобла́стная лимфаденопати́я с диспротеинеми́ей) — редкий подтип периферической Т-клеточной лимфомы, характеризующийся выраженными воспалительными процессами. Опухолевые клетки при данной лимфоме происходят из фолликулярных Т-хелперов, которые в норме участвуют в формировании гуморального иммунитета. Клональная экспансия этих клеток приводит к нарушению работы герминативных центров, что проявляется системным воспалением, аутоиммунными реакциями и повышенной секрецией иммуноглобулинов. Клинически заболевание проявляется системной лимфаденопатией, гепатоспленомегалией, а также иммунной гиперактивацией в виде поликлональной гипергаммаглобулинемии или гемолитической анемии[1].
Что важно знать
История
В 1974 году Фриццера и коллеги впервые описали это заболевание как атипичную лимфоидную гиперплазию у пожилых людей с симптомами иммунной дисрегуляции и диспротеинемии. К концу 1980-х годов была установлена клональность заболевания, и оно получило признание как лимфома. В 1994 году АИТЛ была официально признана отдельным типом Т-клеточной лимфомы. Исследования 2000-х годов показали, что опухоль происходит из фолликулярных Т-хелперных клеток. Начиная с 2010 года, были обнаружены характерные мутации в генах-регуляторах эпигенетических процессов, включая TET2, DNMT3A и IDH2, а в 2014 году была выявлена соматическая мутация RHOAG17V, встречающаяся в 70 % случаев заболевания[2].
Классификация
АИТЛ относится к классу нодальных Т-клеточных лимфом[1].
Этиология
АИТЛ развивается в результате злокачественной трансформации фолликулярных Т-хелперных клеток. В норме эти клетки помогают В-лимфоцитам созревать в герминативных центрах лимфоузлов. При лимфоме происходит нарушение работы этих клеток, что приводит к избыточной выработке воспалительных веществ, способствующих ангиогенезу и созданию благоприятной микросреды для роста опухоли. В развитии заболевания участвуют генетические мутации, затрагивающие эпигенетическую регуляцию и сигнальные пути Т-клеток, а также реактивация вируса Эпштейна — Барр[2].
Патогенез
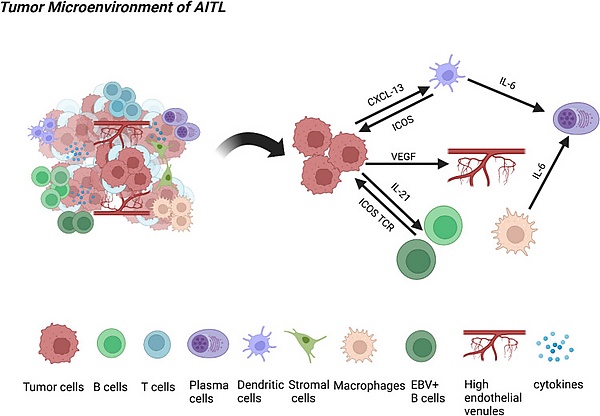
Патогенез АИТЛ представляет собой многоступенчатый процесс, начинающийся с мутаций в генах клеток предшественников. Инициирующим событием выступают мутации в генах эпигенетической регуляции TET2 и DNMT3A, возникающие в клетках-предшественниках и создающие основу для клонального гемопоэза. На эту почву наслаиваются драйверные мутации — прежде всего в гене RHOAG17V, обнаруженная в 60-70 % случаев и специфически нарушающая передачу сигнала от Т-клеточного рецептора, и мутации в гене IDH2, характерные для 20-30 % случаев. Критически важным является взаимодействие мутировавших Т-клеток с микроокружением: мутации TET2 в не-Т-клеточных элементах костного мозга создают необходимые условия для развития лимфомы. Дисфункциональные фолликулярные Т-хелперные клетки продуцируют избыточные количества цитокинов и хемокинов, например, CXCL13, IL-6 и IL-21, что приводит к формированию уникальной провоспалительной микросреды с пролиферацией фолликулярных дендритных клеток, ангиогенезом и привлечением различных иммунных клеток. Реактивация вируса Эпштейна — Барр в В-клетках, наблюдаемая в большинстве случаев, усугубляет иммунную дисрегуляцию[2].
Злокачественные фолликулярные Т-хелперные клетки при ангиоиммунобластной лимфоме, подобно клеткам Рид — Штернберга при лимфоме Ходжкина, составляют лишь незначительную часть клеточного состава поражённого лимфатического узла. Архитектура узла обычно полностью нарушена, фолликулы отсутствуют. При детальном изучении наблюдается разнообразный клеточный состав, включающий бласты, В-клетки, плазматические клетки, эозинофилы, гистиоциты и эпителиоидные клетки. Характерными особенностями являются неправильная пролиферация фолликулярных дендритных клеток и разрастание высоких эндотелиальных венул, вблизи которых и располагаются опухолевые Т-хелперные клетки. При этом активная инфекция вируса Эпштейна — Барр выявляется преимущественно в крупных В-клетках, но не в самих злокачественных Т-клетках[3].
Эпидемиология
АИТЛ составляет от 1 до 2 % всех неходжкинских лимфом и 15-20 % периферических Т-клеточных лимфом, являясь их вторым по распространённости подтипом. Заболевание демонстрирует географическую вариабельность в распространённости, чаще встречаясь в Европе по сравнению с Азией и Северной Америкой. АИТЛ обычно диагностируется у пожилых людей со средним возрастом около 69 лет[2].
Диагностика
Клиническая картина АИТЛ отличается значительным разнообразием проявлений. Заболевание характеризуется системным поражением с вовлечением лимфоузлов и наличием В-симптомов (лихорадка, ночная потливость, значительная потеря веса). У половины пациентов наблюдаются кожные проявления в виде макул, папул или бляшечных высыпаний, которые могут быть первым симптомом болезни. Часто наблюдаются аутоиммунные заболевания, например, аутоиммунная гемолитическая анемия, аутоиммунная тромбоцитопения и васкулиты. Характерна значительная восприимчивость к бактериальным и грибковым инфекциям, которая отражает состояние иммунодефицита[1].
Клинический анализ крови: характерно повышение скорости оседания эритроцитов[1].
Биохимический анализ крови: характерно повышение активности лактатдегидрогеназы[1].
Иммуноферментный анализ: часто выявляется поликлонная гипергаммаглобулинемия, хотя в некоторых случаях отмечается гипогаммаглобулинемия[1].
Предпочтительным методом диагностики АИТЛ является эксцизионная биопсия лимфатического узла с последующим гистопатологическим исследованием, иммуногистохимическим исследованием, гибридизацией in situ для выявления вируса Эпштейна — Барр и проведением секвенирования по Сэнгеру или секвенирования нового поколения для идентификации мутаций генов[1].
Биопсия лимфоузла с гистологическим исследованием: при АИТЛ наблюдается частичное или полное стирание нормальной структуры лимфатического узла с инфильтрацией капсулы и перинодальной ткани. Опухолевые Т-клетки представляют собой малые и средние лимфоциты со светлой цитоплазмой и фолликулярным Т-хелперным иммунофенотипом, которые формируют скопления вокруг высоких эндотелиальных венул. Эти злокачественные клетки часто составляют незначительный компонент ткани и могут отсутствовать в трети случаев. Характерной особенностью является полиморфный клеточный инфильтрат микроокружения, включающий реактивные В-клетки, иммунобласты, плазматические клетки, эозинофилы, дендритные клетки и гистиоциты. Герминативные центры демонстрируют регрессию различной степени. Специфическим признаком является экспансия фолликулярных дендритных клеток в экстрафолликулярных зонах вместе с пролиферацией высоких эндотелиальных венул[2].
В лимфатическом узле при АИТЛ выделяют три архитектурных паттерна, отражающих эволюцию заболевания[2]:
- паттерн I встречается реже всего и характеризуется сохранённой архитектурой с гиперплазией фолликулов;
- паттерн II демонстрирует частичное истощение фолликулов;
- паттерн III является наиболее распространённым и представляет собой классический вариант с полной утратой структуры лимфоузла, исчезновением фолликулов и выраженным разрастанием сетей фолликулярных дендритных клеток.
Проточная цитометрия: наиболее частой находкой является аномальный иммунофенотип sCD3/CD4, выявляемый в 70-90 % случаев, как минимум с одним ослабленным Т-клеточным антигеном, чаще всего CD7. Экспрессия CD10 служит чувствительным маркером для идентификации фолликулярного Т-хелперного иммунофенотипа, однако её уровень варьирует от 50 до 90 % случаев. Экспрессия антигенов может различаться в зависимости от локализации: полная или частичная потеря sCD3 чаще наблюдается в периферической крови и костном мозге, тогда как экспрессия CD10 более характерна для лимфатических узлов. Яркая экспрессия PD-1 при проточной цитометрии является уникальным признаком АИТЛ независимо от локализации и полезна для дифференциальной диагностики с другими периферическими Т-клеточными лимфомами[2].
Молекулярно-генетический анализ методом секвенирования: характерными мутациями при АИТЛ являются: RHOAG17V (50-70 % случаев), TET2 (70-80 %), IDH2 (20-30 %) и DNMT3A (10-25 %). Эти мутации часто сочетаются, особенно TET2 с RHOA и IDH2, формируя уникальный молекулярный профиль заболевания. Дополнительно выявляются мутации генов TCR-сигнального пути (PLCG1, CD28, VAV1, FYN).
Позитронно-эмиссионная томография и компьютерная томография: используются для определение распространённости узловых или внеузловых поражений[1].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими заболеваниями[2]:
- нодальная т-фолликулярная хелперная лимфома фолликулярного типа;
- периферическая т-клеточная лимфома;
- классическая лимфома Ходжкина;
- реактивная фолликулярная гиперплазия;
- болезнь Кимуры.
Осложнения
Заболевание может осложняться развитием гемофагоцитарного лимфогистиоцитоза и диссеминированного внутрисосудистого свёртывания крови[1].
Лечение
Лечение АИТЛ представляет собой сложную многокомпонентную задачу, требующую индивидуального подхода. Особенностью терапии является необходимость учёта молекулярного профиля опухоли — наличие мутаций в генах TET2, DNMT3A и IDH2 может определять чувствительность к различным вариантам лечения. Комбинированные подходы, последовательное применение различных классов препаратов и своевременное использование трансплантации позволяют постепенно улучшать прогноз этого агрессивного заболевания[4].
В качестве первой линии терапии применяется антрациклин-содержащий режим CHOP, однако его эффективность остаётся недостаточной — пятилетняя общая выживаемость не превышает 32-36 %. Значительное улучшение результатов демонстрирует комбинация CHOP с таргетными препаратами, в частности с братуксимабом ведотином у пациентов с экспрессией CD30+. Важным компонентом лечения является консолидирующая аутологичная трансплантация гемопоэтических стволовых клеток у молодых пациентов, с ответом на на индукционную терапию, что позволяет значительно улучшить долгосрочные результаты[4].
При развитии рецидивов и рефрактерных форм заболевания основную роль играют таргетные препараты, направленные на эпигенетические механизмы развития лимфомы. Ингибиторы гистондеацетилазы, например, ромидепсин и хидамид, демонстрируют значительную эффективность. Перспективным направлением является комбинированная эпигенетическая терапия — сочетание ингибиторов гистондеацетилазы с ингибиторами ДНК-метилтрансферазы (азацитидин), что позволяет достичь частоты полных ремиссий до 60 % при рефрактерных формах[4].
Активно изучаются препараты, направленные на различные сигнальные пути. Ингибиторы PI3K/AKT пути демонстрируют обнадёживающие результаты — дувелисиб показывает эффективность у 50 % пациентов с рецидивной лимфомой. Значительный интерес представляет могамулизумаб — моноклональное антитело против CCR4, которое в комбинации с химиотерапией позволяет достичь четырёхлетней выживаемости 46,3 % против 20,6 % при стандартной терапии. Для пациентов с определёнными молекулярными характеристиками перспективны ингибиторы фарнезилтрансферазы, направленные на регуляцию хемокинов, и мультикиназные ингибиторы, воздействующие на последствия мутаций в гене RHOAG17V[4].
Прогноз
Прогноз при АИТЛ в целом остаётся неблагоприятным, с медианой общей выживаемости 2-3 года и пятилетней выживаемостью 32-44 %. К факторам, ассоциированным с неблагоприятным прогнозом, относятся возраст старше 60 лет, экстранодальное поражение, тромбоцитопения, повышение активности лактатдегидрогеназы и концентрации бета-2-микроглобулина, низкая концентрация альбумина и вовлечение костного мозга. Пациенты с высокими баллами прогностических индексов имеют пятилетнюю выживаемость без прогрессирования около 25 %, тогда как в группе низкого риска этот показатель достигает 40 %[2][4].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Xing Y., Huang J., Zhang Y., Wang Y., Qi S. Advancing the understanding and management of angioimmunoblastic T-cell lymphoma: insights into its pathogenesis, clinical features, and emerging therapeutic strategies (англ.) // Front Oncol. — 2025. — Vol. 15. — P. 1479179. — doi:10.3389/fonc.2025.1479179.
- Matsumoto N.P., Xu M.L. Angioimmunoblastic T-cell lymphoma: Current Diagnostic Insights and Advances (англ.) // Hum Pathol. — 2025. — Vol. 156. — P. 105696. — doi:10.1016/j.humpath.2024.105696.
- Feng Y., Ma Y., Li T., Liu M., Hong Z., Yin Q., Zheng M. Angioimmunoblastic T-cell lymphoma: a concise overview encompassing the pathogenetic, pathological, clinical, therapeutical characteristics, and recent advances (англ.) // Clin Exp Med. — 2025. — Vol. 25, no. 1. — P. 218. — doi:10.1007/s10238-025-01754-4.