MALT-лимфома
MALT-лимфо́ма (англ. mucosa-associated lymphoid tissue — лимфо́идная тка́нь, ассоции́рованная со сли́зистыми оболо́чками; экстранода́льная лимфо́ма маргина́льной зо́ны) — индолентная (вялотекущая) неходжкинская лимфома. Отличительной чертой является первичное поражение органов и тканей вне лимфатических узлов. Субстратом опухоли являются В-лимфоциты маргинальной зоны, локализованные в слизистых оболочках. Для MALT-лимфом характерна низкая пролиферативная активность, что объясняет её медленное, часто бессимптомное течение[2][3].
Что важно знать
История
MALT-лимфома была впервые описана как самостоятельное заболевание патологами Исааксоном и Райтом в 1983 году[4].
Классификация
MALT-лимфома относится к лимфомам маргинальной зоны[5].
Классификация TNM для MALT-лимфомы (система Paris)[6]:
| Категория | Критерии |
|---|---|
| T (первичная опухоль) | |
| TX | Распространённость лимфомы не уточнена |
| T0 | Нет признаков лимфомы |
| T1m | Поражение слизистой оболочки |
| T1sm | Поражение слизистой и подслизистой оболочек |
| T2 | Поражение мышечной оболочки |
| T3 | Поражение серозной оболочки |
| T4 | Прорастание в соседние структуры |
| N (регионарные лимфоузлы) | |
| N0 | Нет поражения регионарных лимфоузлов |
| N1 | Поражение перигастральных лимфоузлов |
| N2 | Поражение внутрибрюшных лимфоузлов (удалённых от желудка) |
| N3 | Поражение внебрюшных лимфоузлов |
| M (отдалённые метастазы) | |
| M0 | Нет отдалённых метастазов |
| M1 | Есть отдалённые метастазы (неконтактные участки ЖКТ, костный мозг) |
Этиология
Подавляющее большинство пациентов с MALT-лимфомой (около 90 %) являются носителями инфекции Helicobacter pylori. Механизм развития опухоли напрямую связан с длительным антигенным стимулированием слизистой оболочки желудка. Это хроническое воздействие приводит к формированию стойких воспалительных изменений[2].
Патогенез
Патогенез MALT-лимфомы представляет собой многоступенчатый процесс, инициируемый хронической инфекцией Helicobacter pylori. Длительное антигенное воздействие бактерии на слизистую оболочку приводит к стойкому воспалению, особенно в антральном отделе желудка. Helicobacter pylori не только непосредственно раздражает слизистую, но и через выделяемые токсины активирует иммунные клетки — Т-лимфоциты и макрофаги. Эти клетки, в свою очередь, выделяют цитокины, которые стимулируют пролиферацию В-лимфоцитов и образование в желудочной стенке лимфоидных фолликулов — организованной лимфоидной ткани, которая в норме в желудке отсутствует[2].
На фоне постоянной антигенной стимуляции в пролиферирующих В-клетках накапливаются молекулярно-генетические повреждения. Ключевую роль играют специфические хромосомные транслокации, такие как t(11;18)(q21;q21), t(1;14)(p22;q32) и t(14;18)(q32;q21). Наиболее характерной и специфичной является транслокация t(11;18), встречающаяся в 30—50 % случаев и не отмечаемая при других лимфомах. Она приводит к образованию химерного гена API2-MALT1, продукт которого блокирует апоптоз. Параллельно подавляется активность опухолевого супрессора bcl10. Совокупность этих нарушений вызывает постоянную активацию внутриклеточного сигнального пути NF-κB, который включает гены, ответственные за выживание и пролиферацию клеток[2].
Таким образом, основной механизм развития MALT-лимфомы — это не столько высокая скорость деления клеток, сколько дефект апоптоза, что объясняет её низкую пролиферативную активность. Присутствие транслокации t(11;18) ассоциировано с более агрессивным течением и устойчивостью к стандартной антихеликобактерной терапии, так как опухолевые клетки приобретают способность к автономному росту, не зависящему от стимуляции Helicobacter pylori[2].
Эпидемиология
MALT-лимфомы составляют до 50—70 % всех лимфом маргинальной зоны. В структуре всех злокачественных опухолей ЖКТ на их долю приходится от 1 до 10 %. Наиболее частая локализация — желудок, который поражается в 50—75 % случаев. Тонкая кишка вовлекается в процесс в 20—35 % наблюдений, а толстая кишка — значительно реже, лишь в 5—10 % случаев[2][7].
Диагностика
При поражении желудка пациенты часто не предъявляют специфических жалоб, и заболевание нередко выявляется случайно во время планового эндоскопического исследования. Когда симптомы присутствуют, они могут напоминать проявления хронического гастрита или язвенной болезни: дискомфорт или тупые боли в эпигастральной области, ощущение переполнения желудка после еды, тошнота, реже — изжога или отрыжка. Кровотечения и выраженный болевой синдром не характерны[5].
При локализации в тонком кишечнике клиническая картина становится более выраженной. Пациенты могут жаловаться на периодические или постоянные боли в животе спастического характера, вздутие, урчание. Часто наблюдаются нарушения стула в виде диареи или запоров. Для особой формы — иммунопролиферативной болезни тонкой кишки — характерны симптомы мальабсорбции: потеря веса, слабость, отеки и хроническая диарея[5].
При MALT-лимфоме толстой кишки симптомы также неспецифичны. Больные отмечают дискомфорт и боли в животе, чаще в правых отделах (при поражении илеоцекальной области) или в прямой кишке. Диарея или запор являются частыми проявлениями заболевания. Иногда заболевание проявляется только положительным анализом на скрытую кровь в кале без других симптомов[5].
Клинические проявления MALT-лимфомы лёгких часто носят неспецифический характер. На начальных этапах заболевания пациенты могут не предъявлять жалоб вообще либо у них отмечаются сухой кашель, одышка и боль в грудной клетке. По мере прогрессирования опухолевого процесса симптоматика становится более выраженной: сухой кашель может смениться продуктивным, возможно появление кровохарканья, а также рецидивирующих бронхолёгочных инфекций. При дальнейшем развитии болезни присоединяются общие симптомы, свидетельствующие об активности процесса: лихорадка, ночная потливость, потеря веса и общая слабость[3].
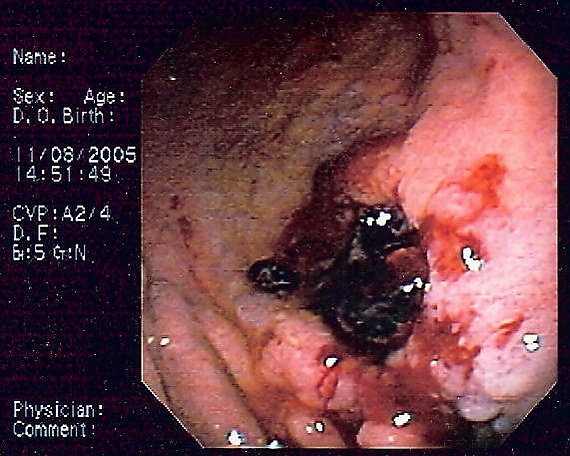
При эзофагогастродуоденоскопии MALT-лимфома желудка чаще всего имеет гастритоподобный вид, что значительно затрудняет её визуальную диагностику. Основными эндоскопическими формами являются антральный гастрит, эрозивный гастрит и очаговый гиперпластический гастрит, которые могут сочетаться друг с другом[2][7]:
- наиболее частым вариантом является картина антрального гастрита. При этом в антральном отделе визуализируется пастозная, разрыхлённая слизистая оболочка с очаговой гиперемией, которая чередуется с участками белесоватого цвета. Характерным признаком является так называемый стекловидный блеск поверхности слизистой. Её эластичность и подвижность снижены, при контакте с эндоскопом отмечается повышенная кровоточивость;
- при эрозивной форме на фоне отёчной и гиперемированной слизистой с усиленным сосудистым рисунком обнаруживаются множественные поверхностные эрозии неправильной или щелевидной формы. Эти эрозии могут располагаться в любом отделе желудка как изолированно, так и на фоне обширных изменений. Эластичность стенки желудка при этой форме обычно сохраняется;
- очаговый гиперпластический гастрит эндоскопически проявляется умеренным, но неравномерным утолщением складок на ограниченном участке, чаще по большой кривизне или в теле желудка. Поверхность утолщённых складок разрыхлена, покрыта вязкой прозрачной слизью, а сами складки плохо расправляются при инсуфляции воздухом, хотя общая эластичность стенки может быть сохранена.
Световая микроскопия биоптата стенки желудка: характерно формирование плотного лимфоидного инфильтрата, расположенного в собственной пластинке слизистой оболочки. В составе инфильтрата наблюдаются фолликулоподобные скопления лимфоцитов, которые нередко содержат светлые центры, напоминающие герминативные центры. Дополнительно могут встречаться единичные трансформированные бласты, рассеянные по всему инфильтрату. Однако ключевым диагностическим признаком является наличие лимфоэпителиальных поражений. Они проявляются в виде инвазии опухолевых лимфоцитов через базальные мембраны в эпителий слизистых желёз, что приводит к их частичному или полному разрушению[2][8].
При иммуногистохимическом исследовании опухолевые клетки MALT-лимфомы демонстрируют экспрессию общих маркеров В-лимфоцитоd, таких как CD20, CD43 и CD79a. При этом они, как правило, не экспрессируют маркеры CD5, CD10 и CD23. Отрицательная реакция на эти антигены имеет ключевое значение для дифференциальной диагностики, поскольку позволяет отличить MALT-лимфому от других видов В-клеточных лимфом, в частности от лимфомы из клеток мантийной зоны (CD5-позитивная) и фолликулярной лимфомы (CD10-позитивная)[2][7].
Эндосонография желудка: типичным является неравномерное утолщение слизистого слоя стенки желудка, которое вызвано его очаговой или диффузной инфильтрацией лимфоидными клетками. Этот патологический процесс часто распространяется и на подслизистый слой. При этом изменённые участки слизистой оболочки могут чередоваться с зонами, сохранившими нормальное строение. В случаях, когда заболевание сопровождается образованием эрозий, визуализируется нарушение целостности слизистого слоя, его локальное утолщение, а в центре эрозивных дефектов определяются гиперэхогенные включения, обусловленные фибринозными наложениями[2].
При рентгенографии органов грудной клетки у пациентов с MALT-лимфомой лёгких наиболее часто обнаруживаются очаги затемнения диаметром до пяти сантиметров, имеющие как чёткие, так и размытые контуры. Характерным рентгенологическим признаком является визуализация симптома «воздушной бронхографии», когда на фоне уплотнения лёгочной ткани просматриваются просветы воздушных бронхов[3].
Компьютерная томография грудной клетки у пациентов с MALT-лимфомой лёгких выявляет разнообразные варианты поражения. Опухоль может иметь вид солитарного узла с чёткими контурами, множественных одно- или двусторонних очагов, а также диффузных инфильтратов, распространяющихся вдоль бронховаскулярных пучков и междолевых щелей. Нередко наблюдаются обширные долевые уплотнения с воздушными бронхограммами, что рентгенологически может имитировать картину пневмонии, или же участки снижения прозрачности по типу «матового стекла». Типично множественное и двустороннее поражение. В отличие от других заболеваний, такие изменения, как формирование полостей, отложение кальцинатов, кистозная трансформация лёгочной ткани или наличие плеврального выпота, встречаются крайне редко[3].
Иммуноферментный анализ: возможно выявление антител класса IgG к Helicobacter pylori[7].
Для выявления транслокации t(11;18)(q21;q21) могут быть использованы такие методы, как флуоресцентная гибридизация in situ или полимеразная цепная реакция в реальном времени. Наличие данной транслокации имеет важное клиническое значение: с одной стороны, такие случаи редко трансформируются в агрессивную высокозлокачественную лимфому, но с другой — они ассоциированы с отсутствием ответа на эрадикационную терапию, направленную против Helicobacter pylori[8].
Дифференциальная диагностика
Дифференциальная диагностика MALT-лимфомы проводится со следующими заболеваниями: В-клеточные лимфомы, диффузные В-крупноклеточные лимфомы, гастрит, рак желудка, узелковая лимфоидная гиперплазия, лимфогранулематоз, инфекционные заболевания, другие неходжкинские лимфомы[9][10].
Лечение
Основой терапии при желудочной MALT-лимфоме, ассоциированной с Helicobacter pylori, является антибиотикотерапия с целью эрадикации Helicobacter pylori. Если лимфома сохраняется, но инфекция устранена, может быть выбрана выжидательная тактика с регулярными эндоскопическими обследованиями. В случаях, когда выявляется транслокация t(11;18), или эрадикация не приносит результата, или лимфома изначально не связана с Helicobacter pylori, применяется лучевая терапия. Альтернативой облучению служит монотерапия ритуксимабом, или иммунохимиотерапия по схемам R-CHOP, R-CVP, или комбинация ритуксимаба с хлорамбуцилом[7].
Прогноз
MALT-лимфома характеризуется в целом благоприятным прогнозом благодаря своему вялотекущему характеру. Средняя выживаемость пациентов составляет около 10 лет. При локализованных стадиях заболевания, когда опухоль ограничена первичным органом, показатели эффективности лечения высоки: 10-летняя выживаемость достигает 75 %. Однако течение болезни не у всех пациентов одинаково. Примерно у 30 % больных наблюдается более агрессивное течение лимфомы, при котором медиана выживаемости сокращается до четырёх лет[9][11].
Диспансерное наблюдение
Пациентам, достигшим полной ремиссии после лечения, устанавливается пожизненное диспансерное наблюдение у онколога или гематолога с определённой периодичностью осмотров: в течение первого года после терапии — каждые три месяца, на втором году — каждые шесть месяцев, с третьего по пятый год — ежегодно, а после пяти лет ремиссии — один раз в два года[7].
Профилактика
Эрадикация Helicobacter pylori позволяет снизить риск развития MALT-лимфомы[12]
Примечания
Литература
- Бакулин И.Г., Бакулина Н.В., Воробьёв С.Л., Попова Е.А., Малихова О.А., Зейналова П.А., Ильчишина Т.А., Лозовая В.В., Аббасбейли Ф.М. MALT-лимфома и эрозивно-язвенные поражения желудка: современные подходы к дифференциальной диагностике и собственное клиническое наблюдение // Онкогематология. — 2019. — Т. 14, № 3. — С. 23—37. — doi:10.17650/1818-8346-2019-14-3-23-37.
- Фролова И.Г., Веснина В.О., Величко С.А., Гольдберг А.В., Попова М.В., Табакаев С.А., Евтеев Л.А., Миллер С.В., Глущенко С.А. MALT-лимфома с поражением лёгких, плевры и внутригрудных лимфатических узлов: клиническое наблюдение // Онкологический журнал: лучевая диагностика, лучевая терапия. — 2018. — Т. 1, № 4. — С. 92—100. — doi:10.37174/2587-7593-2018-1-4-92-100.
- Ishikawa E., Nakamura M., Satou A., Shimada K., Nakamura S. Mucosa-Associated Lymphoid Tissue (MALT) Lymphoma in the Gastrointestinal Tract in the Modern Era (англ.) // Cancers (Basel). — 2022. — 17 January (vol. 14, no. 2). — P. 446. — doi:10.3390/cancers14020446.