Нефрогенный несахарный диабет
Нефроге́нный неса́харный диабе́т (ННД) — синдром, для которого характерна клиническая триада: полиурия, полидипсия и гипернатриемия. Это состояние возникает из-за физиологической неспособности концентрировать мочу в результате нечувствительности почек к антидиуретическому гормону (АДГ), что приводит к повышенному выделению разбавленной мочи[3].
Что важно знать
История
В начале XX века немецкий учёный Де Ланге обнаружил, что некоторые пациенты с несахарным диабетом не реагируют на экстракты задней доли гипофиза, а заболевание в их семьях не передавалось по мужской линии. Позже Форссман подтвердил, что почки играют ключевую роль в развитии резистентных к терапии форм несахарного диабета. Уоринг описал врождённый синдром, проявляющийся вскоре после рождения полиурией, полидипсией, гипернатриемией, дегидратацией и неспособностью концентрировать мочу, предположив дефект канальцевой реабсорбции воды с X-сцепленным наследованием. В 1947 году Уильямс и Генри ввели термин «нефрогенный несахарный диабет» для обозначения врождённого синдрома, характеризующегося нечувствительностью почек к вазопрессину, и установили его наследственный характер с передачей через бессимптомных женщин мужскому потомству, связав патологию с дефектом петли Генле и дистальных канальцев[4].
Классификация
ННД может быть классифицирован на[5][6]:
- врождённый, который в свою очередь делится на аутосомно-доминантную, аутосомно-рецессивную и Х-сцепленную формы. Также к этой группе относится ННД, связанный с мутациями в транспортёре мочевины;
- приобретённый — может развиться вследствие приёма препаратов, блокирующих действие АДГ (например, литий, некоторые антибиотики, противогрибковые и противоопухолевые средства).
Классификация ННД по механизму развития[7]:
I. Первичные нарушения передачи гормонального сигнала (наследственные аномалии):
- изменение количества и аффинности рецепторов;
- нарушения взаимодействия рецепторов с G-белками;
- ускоренная деградация вторичного посредника — цАМФ;
- нарушения свойств водных каналов;
- нарушение реакции целой почки на гормональный сигнал.
II. Вторичные нарушения передачи сигнала и реакции почки на гормональные воздействия:
- нарушения, вызванные изменениями электролитного состава плазмы;
- нарушения, вызванные фармакологическими и токсическими воздействиями;
- нарушения, связанные с приобретённым изменением структуры и целостности почек.
Этиология
Патогенез
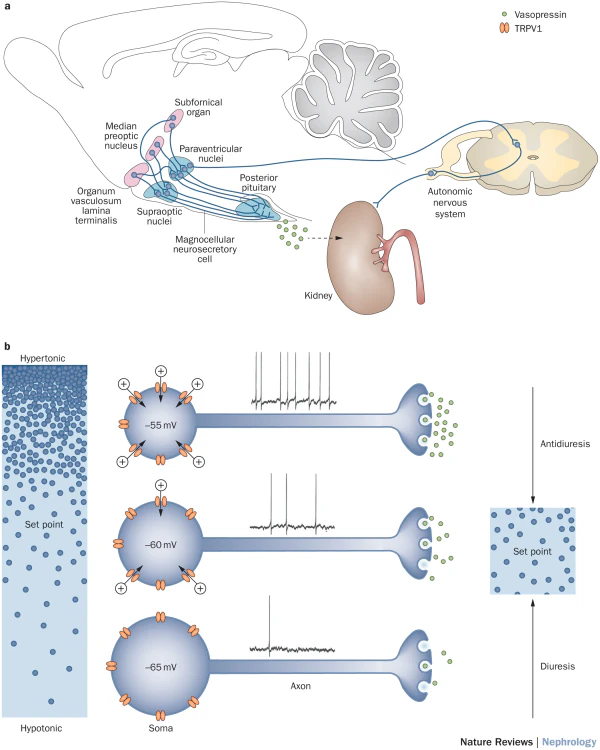
АДГ, синтезируемый в гипоталамусе и секретируемый задней долей гипофиза, играет ключевую роль в регуляции водного баланса. При повышении осмоляльности плазмы (>280—290 мОсм/кг) его секреция усиливается. Гормон связывается с V2-рецепторами на базолатеральной мембране главных клеток собирательных трубочек, активируя каскад реакций: синтез циклического аденозинмонофосфата, фосфорилирование и транспортировку аквапорина-2 к апикальной мембране. Это обеспечивает реабсорбцию воды. При ННД данный механизм нарушается из-за резистентности почек к АДГ[3].
Генетические формы ННД обусловлены мутациями в генах, критичных для работы V2-рецепторов или водных каналов. Х-сцепленный тип связан с дефектами гена AVPR2, приводящими к нечувствительности V2-рецепторов. Аутосомные формы (доминантные/рецессивные) возникают из-за мутаций гена AQP2 , нарушающих функцию аквапорина-2. Реже встречаются дефекты генов SLC14A1 и SLC14A2, кодирующих переносчики мочевины, что ухудшает осмотический градиент мозгового вещества почек[6].
Приобретённые формы ННД развиваются под действием внешних факторов. Литий, накапливаясь в клетках, подавляет аденилатциклазу, снижая экспрессию AQP2. Обструктивная уропатия вызывает аналогичные изменения через угнетение синтеза аквапоринов. Другие причины — электролитные нарушения (гиперкальциемия, гипокалиемия) и лекарственные препараты (тетрациклины, фуросемид), которые нарушают работу канальцев или рецепторов[3].
Указанные механизмы приводят к нарушению реабсорбции воды в собирательных трубочках, что становится причиной неспособности почек концентрировать мочу, которая приводит к полиурии и дегидратации[3].
Эпидемиология
Х-сцепленная форма ННД преимущественно проявляется у мужчин. Женщины могут быть носителями этой мутации, иногда у них наблюдаются лёгкие симптомы. Аутосомно-доминантная, аутосомно-рецессивная и приобретённая формы ННД встречаются с одинаковой частотой у обоих полов. Симптомы могут возникнуть в любом возрасте, обычно внезапно и без предвестников.
Распространённость наследственного ННД точно не установлена, но Х-сцепленная форма встречается примерно у 4 на 1 000 000 новорождённых. При этом приобретённая форма ННД диагностируется значительно чаще наследственных форм. Длительный приём препаратов лития приводит к развитию ННД примерно у 55 % пациентов. Точные данные о распространённости приобретённого ННД в общей популяции отсутствуют[8].
Диагностика
У детей с ННД основными симптомами являются выраженная полиурия (выделение от 3 до 18 литров мочи в сутки в зависимости от возраста) и постоянная мучительная жажда. Характерны сопутствующие нарушения: ночное и дневное недержание мочи, хронические запоры, сниженное потоотделение и слюноотделение. Эти дети отличаются эмоциональной неустойчивостью — они раздражительны, плаксивы, часто демонстрируют резкие перепады настроения. Со стороны когнитивных функций отмечаются ухудшение памяти, снижение концентрации внимания, рассеянность. Может наблюдаться как гиперактивность, так и патологическая заторможенность. Формируется типичный астеноневротический синдром с задержкой физического развития. Постоянная жажда и необходимость частого мочеиспускания меняют поведенческие стереотипы[6].
Пациенты с ННД могут отставать в физическом развитии. Это может быть связано с неоптимальным контролем заболевания в детском возрасте или недостаточным питанием (например, при синдроме нарушенного всасывания)[8].
У взрослых пациентов с ННД может развиваться ортостатическая гипотензия, которая проявляется головокружениями и кратковременными эпизодами потери сознания (ортостатическими коллапсами)[8].
Клинический анализ мочи: характерны крайне низкие показатели относительной плотности мочи (1001—1003 г/л) и её осмоляльности (<200 мосмоль/кг H₂O)[6].
Молекулярно-генетическое исследование (полимеразная цепная реакция или секвенирование) выявляет патогенные мутации в генах, ассоциированных с различными формами ННД[6]:
- при Х-сцепленном рецессивном типе в 90 % случаев обнаруживают мутации гена AVPR2, кодирующего V2-рецептор АДГ.
- при аутосомных формах (как рецессивных, так и доминантных) идентифицируют мутации гена AQP2.
Биохимический анализ крови: характерно снижение концентрации глюкозы и электролитов[6].
Магнитно-резонансная томография головного мозга позволяет исключить центральную форму несахарного диабета[9].
Ультразвуковое исследование почек может выявить расширение чашечно-лоханочной системы при обструктивной уропатии[9].
Для диагностики ННД применяют тест в водной депривацией. Суть теста заключается в создании контролируемого состояния умеренного обезвоживания для оценки способности почек концентрировать мочу. Исследование проводят в стационаре под постоянным медицинским наблюдением с регулярным лабораторным мониторингом. Критерии диагностики ННД[3]:
- осмоляльность сыворотки >300 мОсм/кг;
- осмоляльность мочи <600 мОсм/кг после дегидратации;
- отсутствие реакции на десмопрессин подтверждает нефрогенную форму.
Дифференциальная диагностика
Дифференциальную диагностику ННД проводят со следующими заболеваниями[8]:
- центральный несахарный диабет;
- сахарный диабет;
- первичная (психогенная) полидипсия.
Осложнения
Характерными осложнениями ННД являются[6]:
- дилатация чашечно-лоханочной системы;
- мегауретер;
- мегацистис;
- гидронефроз;
- хроническая болезнь почек.
Лечение
Основная цель терапии — уменьшение полиурии и полидипсии при профилактике осложнений[6].
Медикаментозная терапия включает несколько подходов. На первом месте стоят тиазидные диуретики, которые снижают диурез. Их можно применять как в виде монотерапии, так и в комбинациях. В комбинированных схемах тиазиды сочетают с нестероидными противовоспалительными препаратами или калийсберегающими диуретиками. Такие сочетания позволяют усилить антидиуретический эффект и уменьшить побочные действия[6].
Все пациенты с врождённой формой заболевания нуждаются в пожизненном лечении. Терапия подбирается индивидуально с учётом возраста, массы тела и сопутствующих состояний[6].
Прогноз
Врождённый ННД — это тяжёлое наследственное заболевание почечных канальцев, требующее постоянного лечения. У маленьких детей даже незначительное ограничение жидкости может вызвать опасное обезвоживание с повышением уровня натрия в крови и лихорадкой. Согласно исследованиям, выживаемость пациентов с врождённым ННД составляет[6]:
- 96 % в первые 20 лет жизни;
- 85 % к 25—30 годам;
- 73 % к 35 годам.
Прогноз при приобретённых формах зависит от прогрессирования заболевания и развития хронической болезни почек[10].
Диспансерное наблюдение
Пациентам с ННД показано диспансерное наблюдение[9]:
- Плановая оценка (1 раз в год при стабильном течении):
- количество и продолжительность эпизодов жажды в течение суток;
- суточный диурез;
- частота ночных мочеиспусканий;
- клинический анализ мочи;
- биохимический анализ крови: концентрация натрия, калия, глюкозы, креатинина;
- Дополнительные исследования при декомпенсации:
- анализ мочи по Зимницкому.
Примечания
Литература
- Смирнова Н. Н. Наследственные формы нефрогенного несахарного диабета // Нефрология. — 2005. — № 4.
- Семёнова О. А., Савенкова Н. Д., Степанова А. А. Врождённый нефрогенный несахарный диабет, ассоциированный с интракраниальными кальцификатами // Педиатр. — 2011. — № 1.
- Клепалова В.В., Пушкарёва О.С., Изюрова Н.В., Аксёнов А.В. Семейная форма нефрогенного Х-сцепленного несахарного диабета (рус.) // Проблемы Эндокринологии : журнальная статья. — 2022. — Т. 68, № 5. — С. 87—90. — doi:10.14341/probl13098.