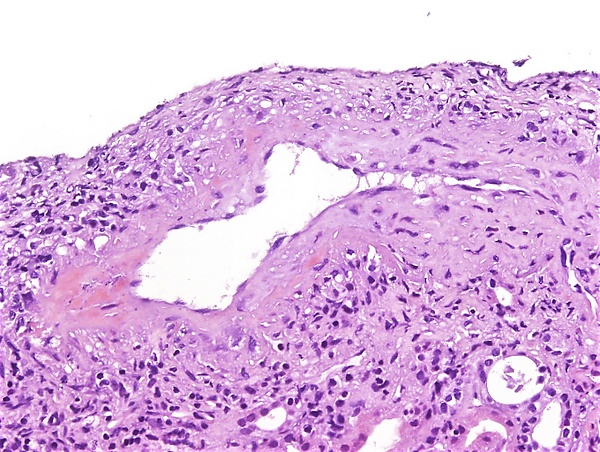
АНЦА-ассоциированный гломерулонефрит
АНЦА-ассоции́рованный гломерулонефри́т (гломерулонефри́т, ассоции́рованный с антинейтрофи́льными цитопламазти́ческими антитела́ми) представляет собой форму быстропрогрессирующего гломерулонефрита (ГН), в основе которого лежит некротизирующее воспаление почечных капилляров с минимальным отложением иммунных комплексов или их полным отсутствием. Данное заболевание патогенетически связано с образованием антинейтрофильных цитоплазматических аутоантител (АНЦА). Оно может проявляться как изолированное поражение почек или в рамках системных АНЦА-ассоциированных васкулитов. Для этой патологии характерно тяжёлое течение с быстрым развитием почечной недостаточности и неблагоприятным прогнозом. Без своевременной иммуносупрессивной терапии заболевание приводит к летальному исходу у большинства пациентов в течение первого года. Даже на фоне агрессивного лечения пятилетняя выживаемость не превышает 75 %, при этом у значительной доли выживших пациентов сохраняется зависимость от заместительной почечной терапии[1].
Что важно знать
История
История понимания АНЦА-ассоциированных васкулитов, в частности их почечного компонента, началась задолго до открытия самих антител. Изначально поражение почек при системных васкулитах, таких как узелковый полиартериит, не дифференцировалось. Ключевой вехой стало исследование Дэйвсона, Болла и Платта в середине XX века, которое впервые выделило две специфичные группы: одна с системным артериитом без выраженного ГН (соответствует современному узелковому полиартерииту), а другая — с поражением лёгких и распространённым некротизирующим ГН, что предвосхитило понятие микроскопического полиангиита. Позже, в 1982 году, австралийские исследователи впервые описали связь между сегментарным некротизирующим ГН и наличием в сыворотке антител, окрашивающих цитоплазму нейтрофилов, хотя значимость этого открытия не была сразу оценена. В 1985 году Фолк и Дженнетт систематизировали знания, показав, что АНЦА встречаются при некротизирующем ГН и ГН с образованием полулуний, который может быть как ограниченным почками, так и частью системного васкулита (например, гранулематоза с полиангиитом), и идентифицировали два основных типа антител: к протеиназе-3 и к миелопероксидазе[2].
Классификация
Существует несколько систем классификации, основанных на клинических, гистологических данных или их сочетании, которые применяются для распределения пациентов по группам с наибольшей вероятностью положительного ответа на иммуносупрессивную терапию. Начиная с 2010 года, для прогнозирования исхода почечного заболевания у пациентов с АНЦА-ассоциированным ГН используются гистопатологические классификации, среди которых наиболее распространены классификация Бердена и шкала почечного риска при АНЦА (ANCA Renal Risk Score)[3]:
- согласно классификации Бердена, выделяют четыре категории поражения почек: фокальный класс (≥50 % нормальных и <50 % повреждённых клубочков), экстракапиллярный класс (≥50 % активных клеточных полулуний), смешанный класс (≥50 % повреждённых клубочков, но <50 % полулуний и <50 % глобального склероза) и склеротический класс (≥50 % глобального склероза клубочков);
- шкала почечного риска при АНЦА (ANCA Renal Risk Score) рассчитывается на основе трёх параметров: процентного содержания нормальных клубочков (0 баллов при >25 %, 4 балла при 10-25 %, 6 баллов при <10 %), степени интерстициального фиброза и атрофии канальцев (0 баллов при ≤25 %, 2 балла при >25 %) и расчётной скорости клубочковой фильтрации на момент постановки диагноза (0 баллов при >15 мл/мин, 3 балла при ≤15 мл/мин). Сумма баллов позволяет отнести пациентов к одной из трёх групп риска: низкому (0 баллов), среднему (2-7 баллов) или высокому (8-11 баллов).
Этиология
В развитии АНЦА-ассоциированного ГН задействован комплекс факторов, включающий генетическую предрасположенность, влияние окружающей среды, инфекции и особенности иммунного ответа. Установлена связь между серотипом АНЦА с наличием антител к протеиназе-3 (ПН-3 АНЦА) и генами, кодирующими альфа-1-антитрипсин, в то время как АНЦА с антителами к миелопероксидазе ассоциирован с HLA-DQ. Например, аллель HLA-DRB1*15 повышает риск развития ПН-3 АНЦА ГН у лиц африканского происхождения, а аллель HLA-DPB1*0401 увеличивает риск рецидива. Полиморфизм rs62132293 гена PRTN3, кодирующего протеиназу-3, также связан с повышенным риском рецидива. Эпигенетические факторы играют важную роль в экспрессии генов, связанных с АНЦА, и в активации нейтрофилов. Среди внешних триггеров выделяются инфекции, такие как инфекция золотистым стафилококком, и приём некоторых лекарственных препаратов, в частности гидралазина и пропилтиоурацила, которые, накапливаясь в нейтрофилах, могут связываться и изменять антиген миелопероксидазы. Эпидемиологические исследования также демонстрируют чёткую дозозависимую связь между возникновением АНЦА-ассоциированного ГН и воздействием кремнезёма и курения[4].
Патогенез
АНЦА являются ключевым элементом патогенеза АНЦА-ассоциированных ГН. Эти аутоантитела первично нацелены на антигены протеиназу-3 и миелопероксидазу, которые в норме находятся внутри нейтрофилов и моноцитов. При воздействии провоспалительных сигналов происходит «прайминг» нейтрофилов — транслокация этих антигенов на клеточную поверхность, где они становятся доступны для связывания с АНЦА. Это связывание приводит к чрезмерной активации нейтрофилов, которые начинают вырабатывать активные формы кислорода, литические ферменты и нейтрофильные внеклеточные ловушки[4].
Именно этот каскад реакций непосредственно приводит к повреждению почек и развитию ГН. Активированные нейтрофилы усиленно прилипают к эндотелию мелких сосудов почечных клубочков. Высвобождаемые ими протеолитические ферменты и активные формы кислорода вызывают прямое токсическое повреждение и гибель клеток клубочкового фильтра. Это запускает процесс фокального некроза капиллярных петель клубочка, который является гистологической особенность. АНЦА-ассоциированного ГН. В ответ на повреждение в пространстве Боумена — Шумлянского активно пролиферируют клетки париетального эпителия, формируя «полулуния» . Эти клеточные скопления сдавливают клубочки, механически нарушая процесс фильтрации и быстро приводя к потере функции почки, что клинически проявляется как быстропрогрессирующий ГН. Дополнительное повреждение усугубляется активацией альтернативного пути системы комплемента, а также провоспалительными цитокинами от активированных макрофагов и Т-лимфоцитов, которые мигрируют в очаг поражения. Почечное повреждение носит малоиммунный характер, то есть сопровождается минимальным отложением иммунных комплексов, что отличает его от других форм быстропрогрессирующего ГН. Итогом этого агрессивного воспаления является склероз и фиброз клубочков и почечной ткани, что в конечном счёте приводит к необратимой потере нефронов и развитию терминальной почечной недостаточности, требующей заместительной почечной терапии[4].
Эпидемиология
Ежегодная заболеваемость АНЦА-ассоциированным ГН в Европе составляет от 1,2 до 1,3 случая на 100 000 жителей в возрасте 18 лет и старше, аналогичные показатели отмечаются в Японии. В США зафиксирована более высокая заболеваемость АНЦА-ассоциированными васкулитами — примерно 3,3 случая на 100 000 человек, причём у около 60 % этой популяции на момент диагностики уже наблюдалось поражение почек. При этом популяционные данные, конкретно описывающие эпидемиологию АНЦА-ассоциированного ГН и связанные с ним исходы в США, остаются недостаточными[5].
Данные о заболеваемости и распространённости АНЦА-ассоциированного ГН на территории Российской Федерации в настоящее время остаются неизвестными, однако исследователи отмечают чёткую тенденцию к их росту[1].
Диагностика
Клиническая картина АНЦА-ассоциированного ГН характеризуется быстрой, в течение нескольких недель или месяцев, потерей почечной функции, которая на начальных этапах может сопровождаться неспецифическими симптомами. Ключевым проявлением служит быстропрогрессирующий ГН, выражающийся в гематурии и отёках. Нередко первыми признаками заболевания становятся лёгочные симптомы: одышка, кашель и кровохарканье. Внепочечные проявления крайне разнообразны и включают системные признаки в виде лихорадки, ночной потливости, потери веса и артралгий[6].
Гистологическое исследование биоптата почки: наиболее типичным является очаговый сегментарный фибриноидный некроз с разрушением базальной мембраны клубочка. Параллельно наблюдается экстракапиллярная пролиферация с образованием клеточных и фиброзно-клеточных полулуний в пространстве Боумена — Шумлянского, которые состоят из скоплений макрофагов и эпителиальных клеток. В просветах поражённых капиллярных петель часто обнаруживаются ядерный детрит и фибриновые тромбы. Активное воспаление вокруг клубочка может приводить к разрыву капсулы Боумена, иногда с формированием перигломерулярной гранулёматозной реакции. При этом для картины не характерна эндотелиальная пролиферация, типичная для иммунокомплексных ГН. В интерстиции наблюдается воспалительный инфильтрат различной интенсивности, состоящий преимущественно из лимфоцитов, гистиоцитов, плазматических клеток и иногда значительного количества эозинофилов. Васкулит поражает мелкие артерии, артериолы, капилляры и венулы, часто проявляясь как лейкоцитокластический васкулит с фибриноидным некрозом и нейтрофильной инфильтрацией. В мозговом веществе может развиваться некротизирующий васкулит сосудов прямых канальцев, что ассоциировано с интерстициальным кровоизлиянием и нейтрофильным воспаление почечных канальцев[7].
Иммунофлюоресцентный анализ биоптата почки: типичен малоиммунный тип поражения, который является характерным диагностическим признаком. При этом наблюдается слабое гранулярное свечение иммуноглобулинов (IgG, IgM, IgA) и компонентов комплемента (C3, C1q). Значительные отложения иммунных комплексов в клубочках отсутствуют, что принципиально отличает данное заболевание от иммунокомплексных ГН. В участках фибриноидного некроза и активных клеточных полулуниях выявляется выраженная флюоресценция фибрина, что отражает активность воспалительного процесса и повреждение сосудистых стенок[7].
Клинический анализ мочи: отмечается гематурия, протеинурия и цилиндурия[8].
Клинический анализ крови: характерно повышение скорости оседания эритроцитов[8].
Биохимический анализ крови: определяется повышение концентрации креатинина, мочевины и С-реактивного белка[8].
Иммуноферментный анализ крови: характерно обнаружение АНЦА в крови[8].
Дифференциальная диагностика
Дифференциальная диагностика АНЦА-ассоциированного ГН проводится со следующими заболеваниями[6]:
- острая травма почки;
- обструктивная уропатия;
- нефротический синдром, вызванный фокально-сегментарным гломерулосклерозом, болезнью минимальных изменений или мембранозной нефропатией;
- антифосфолипидный синдром;
- тромботическая микроангиопатия.
Осложнения
Проведение иммуносупрессивной терапии при АНЦА-ассоциированном ГН сопряжено с риском развития различных оппортунистических инфекций, некоторые из которых могут представлять угрозу для жизни. Применение циклофосфамида несёт в себе специфические риски, такие как развитие геморрагического цистита и появление гематурии. Проведение плазмафереза, в свою очередь, может привести к удалению факторов свёртывания крови, что повышает склонность пациента к кровотечениям[6].
Лечение
Терапия АНЦА-ассоциированного ГН преследует цель достижения быстрой и длительной ремиссии через двухэтапный подход. Индукционная терапия предполагает применение глюкокортикостероидов в комбинации с циклофосфамидом или ритуксимабом, которые считаются равноэффективными, при этом выбор конкретного препарата определяется тяжестью состояния, доступностью и индивидуальными факторами пациента. При угрожающих жизни органных поражениях протокол лечения усиливается за счёт пульс-терапии метилпреднизолоном и рассмотрением вопроса об использовании плазмафереза, чья эффективность продолжает дискутироваться, хотя он может приносить пользу отдельным пациентам с активным воспалительным процессом. На этапе поддержания ремиссии осуществляется постепенное снижение дозы глюкокортикостероидов вплоть до полной отмены с переходом на длительную иммуносупрессивную терапию, направленную на профилактику рецидивов заболевания[4].
Прогноз
Без лечения АНЦА-ассоциированный ГН характеризуется уровнем летальности до 80 %. Однако применение агрессивной иммуносупрессивной терапии позволяет повысить выживаемость до 75 % в течение пяти лет. Примерно у 25 % пациентов с данной патологией в конечном итоге развивается терминальная стадия почечной недостаточности, при этом наиболее неблагоприятные исходы наблюдаются у пациентов пожилого возраста, лиц, нуждающихся в диализе. Около 40 % пациентов сталкиваются с рецидивом заболевания[6].
Диспансерное наблюдение
Пациенты с АНЦА-ассоциированным ГН нуждаются в постоянном наблюдении у врача-нефролога. Кратность и объём обследовании определяется индивидуально.
Профилактика
Не разработана.
Примечания
Литература
- Постникова Г. А., Симонова О. В., Столяревич Е. С. Клинико-морфологические особенности АНЦА-ассоциированного гломерулонефрита // Нефрология и диализ. — 2023. — Т. 25, № 2. — С. 275-283. — doi:10.28996/2618-9801-2023-2-275-283.
- Christodoulou M., Moysidou E., Lioulios G. et al. The prognostic value of two histopathologic classification models of ANCA-associated glomerulonephritis: a prospective study (англ.) // Journal of Nephrology. — 2024. — Vol. 37. — P. 941-950. — doi:10.1007/s40620-023-01855-x.
- Berti A., Cornec-Le Gall E., Cornec D. et al. Incidence, prevalence, mortality and chronic renal damage of anti-neutrophil cytoplasmic antibody-associated glomerulonephritis in a 20-year population-based cohort (англ.) // Nephrology Dialysis Transplantation. — 2019. — 1 September (vol. 34, no. 9). — P. 1508-1517. — doi:10.1093/ndt/gfy250.
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |