Синдром Гительмана
Синдро́м Гительма́на — это редкое генетическое заболевание, часто протекающее без явных симптомов в течение длительного времени. Иногда могут возникать приступы лихорадки, рвоты, болей в животе, мышечной слабости, судорог и метаболические нарушения. Болезнь в основном проявляется у подростков и взрослых, но также может встречаться у новорождённых детей. Синдром вызван мутациями в гене SLC12A3[2].
Что важно знать
История
Синдром Гительмана (СГ) впервые был описан Гительманом в 1966 году на основе наблюдений за тремя пациентами, у которых отмечалась мышечная слабость из-за нехватки калия, а также хронический дерматит, вероятно, вызванный дефицитом магния. Эти симптомы были связаны с повышенным выведением данных электролитов с мочой. Заболевание сопровождалось избыточной выработкой альдостерона и ренина. Позже это состояние получило название «синдром Гительмана» и оказалось схожим с синдромом, описанным ранее Барттером. Из-за сходства синдром Гительмана иногда рассматривают как более лёгкую форму синдрома Барттера. Ген SLC12A3, мутации в котором приводят к развитию СГ, был идентифицирован в 1996 году[2].
Классификация
Выделяются типичную форму СГ с характерными клиническими проявлениями и атипичную форму с церебральными кальцификатами[3].
Этиология
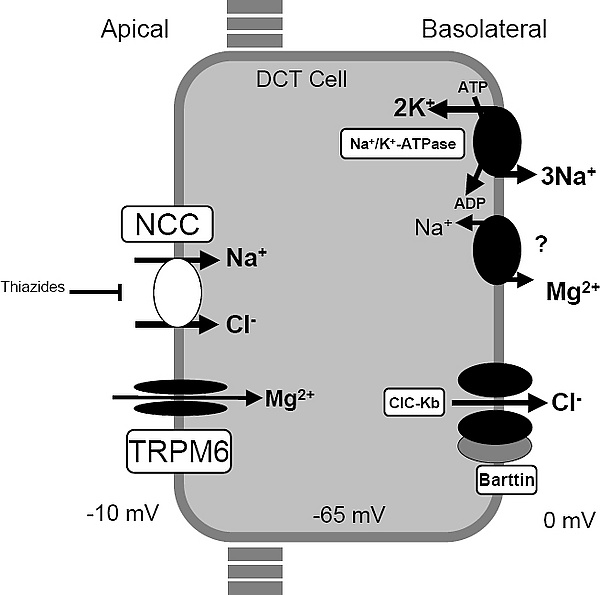
СГ- это аутосомно-рецессивная тубулопатия, вызванное мутациями в генах, кодирующих переносчики натрия, хлора и магния в апикальной мембране дистального извитого канальца, который отвечает за 7—10 % канальцевой реабсорбции электролитов. Также наблюдается снижение экспрессии магниевых каналов в клетках двенадцатиперстной кишки.
Мутации затрагивают:
- Ген SLC12A3, кодирующий тиазид-чувствительный котранспортер натрия и хлора;
- Ген TRPM6, кодирующий белок клаудин, отвечающий за транспорт магния в дистальных канальцах.
Выявлено более 350 мутаций в SLC12A3. Большинство больных являются гетерозиготами по мутациям этого гена[4].
Патогенез
Нарушение транспорта ионов в почках
Обработка натрия, хлора, магния, кальция и калия в почках зависит от слаженной работы канальцевых транспортёров. Дистальные извитые канальцы играют ключевую роль в этом процессе. Нарушения функции этих каналов приводит к различным электролитным нарушениям.
Роль SLC12A3
Ген SLC12A3 кодирует тиазид-чувствительный котранспортёр натрия и хлора в апикальной мембране дистальных извитых канальцев. При мутациях в этом гене дистальные извитые канальцы теряет функцию, что приводит к:
- увеличению поступления натрия и хлора в собирательные трубочки;
- активации ренин-ангиотензин-альдостероновой системы;
- повышенной реабсорбции натрия через каналы в обмен на усиленную экскрецию калия и водорода, что вызывает гипокалиемию и метаболический алкалоз.
Механизмы гипомагниемии и гипокальциурии связаны с мутацией в гене TRPM6:
- нарушается функция магниевых каналов в дистальных извитых канальцах почки и в двенадцатиперстной кишке, что приводит к потере магния с мочой и нарушение всасывания в кишечнике, провоцируя гипомагниемию;
- гипомагниемия нарушает действие паратиреоидного гормона и кальцитриола, снижая чувствительность костей и кишечника к их эффектам.
Дополнительные эффекты:
- гипомагниемия может снижать активность пирофосфатазы, что провоцирует отложение кристаллов пирофосфата в суставах (хондрокальциноз, артралгии);
- гиповолемия и стимуляция ренин-ангиотензиновой системы могут вызывать полидипсию;
- метаболический алкалоз дополнительно влияет на кальциевый обмен.
Таким образом, патогенез синдрома Гительмана представляет собой каскад взаимосвязанных нарушений ионного транспорта, гормональной регуляции и компенсаторных механизмов[4].
Эпидемиология
Распространённость синдрома оценивается примерно в 25 случаев на 1 миллион населения, а частота носительства (гетерозигот) составляет около 1 % в популяциях европейского происхождения, что делает его одним из самых распространённых наследственных заболеваний почечных канальцев[5].
Диагностика
СГ обычно проявляется у подростков и взрослых, но может встречаться и у детей. Основные клинические признаки, указывающие на диагноз:
- тяга к солёному;
- мышечная слабость, усталость, снижение физической выносливости;
- эпизоды обмороков, судорог, тетании, парестезий, карпопедальных спазмов;
- задержка роста и физического развития, позднее половое созревание;
- повышенная жажда или необычное питьевое поведение;
- эпизоды болей в животе;
- у взрослых могут отмечаться головокружение, полиурия, никтурия, боли в суставах, чувство учащённого сердцебиения, проблемы со зрением;
- аритмии;
- в редких случаях может быть внезапная смерть[4][6].
Рентгенография и ультразвуковое исследование суставов может выявить хондрокальциноз[6].
Осмотр глазного дна может выявить склерохороидальную кальцификацию[6].
- хроническая гипокалиемия (<3,5 ммоль/л);
- увеличенная фракционная экскреция хлоридов (>0,5 %);
- гипомагниемия (<0,7 ммоль/л) у 40 % пациентов;
- гипокальциурия (соотношение кальций/креатинин <0,2 ммоль/ммоль);
- метаболический алкалоз.
Окончательный диагноз выставляется на основании анализа на наличие мутации в гене SLC12A3[4][6].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями:
- синдром Барттера;
- первичные формы почечной гипомагниемии;
- длительное использование диуретиков;
- хлоридная диарея;
- псведосиндром Барттера — Гительмана[4][6]
Осложнения
К потенциальным осложнения СГ относят:
- судороги;
- тетания;
- желудочковая тахикардия;
- рабдомиолиз;
- псевдоопухоль мозга;
- склерохороидальные кальцификации[4].
Лечение
На данный момент не разработано специфической терапии СГ. Основной подход к лечению заключается в купировании симптомов. Пациентам показана пожизненная магниезаместительная терапия и соблюдение диеты, обогащённой натрием и калием[2].
Прогноз
Прогноз заболевания в большинстве случаев благоприятный[2].
Диспансерное наблюдение
Большинство пациентов без симптомов наблюдаются у нефролога 1-2 раза в год. При каждом визите врач особо внимательно проверяет жалобы, связанные с нехваткой калия (слабость, упадок сил, проблемы со стулом, перебои в работе сердца) и дефицитом магния (судороги, мурашки по коже, боли в суставах и мышцах), а также назначает анализы крови на калий, магний и бикарбонаты[7].
Примечания
Литература
- Гринштейн Ю. И., Шабалин В. В. Клинический случай синдрома Гительмана с тяжёлой гипокалиемией и псевдоишемическими ЭКГ-измененями // Международный журнал сердца и сосудистых заболеваний. — 2016. — № 9. — doi:10.24412/2311-1623-2016-9-48-53.
- Кисина А. А., Рысс Е. С., Яковенко А. А., Колосова И. М., Каюков И. Г. Синдромы Барттера и Гительмана в практике «Взрослого» нефролога // Нефрология. — 2006. — № 1.