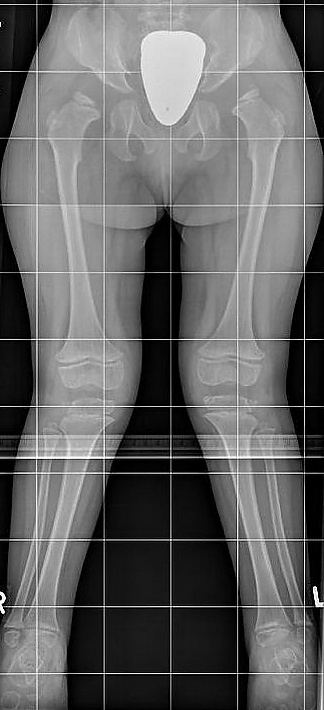
Синдром Моркио
Синдро́м Морки́о (СМ; мукополисахаридо́з IVA типа; спондилоэпифиза́рная дисплази́я, хондроостеодистрофи́я, деформи́рующая остеохондродистрофи́я, синдро́м Морки́о — Бре́йлсфорда, синдро́м Морки́о — У́льриха, К-мукополисахаридо́з, эксцентрохондроплази́я, синдро́м Ду́гве — Мелхио́ра — Кла́узена) — это лизосомная болезнь накопления с аутосомно-рецессивным типом наследования, вызванная мутациями в гене GALNS. Гомозиготные или компаунд-гетерозиготные изменения в этом гене приводят к снижению активности фермента N-ацетилглюкозамин-6-сульфатной сульфатазы, что вызывает накопление гликозаминогликанов (хондроитин-6-сульфата и кератансульфата) в различных тканях. Для пациентов с СМ характерен широкий спектр клинических проявлений разной степени тяжести и скорости прогрессирования, при этом, в отличие от других форм мукополисахаридозов, интеллектуальное развитие не нарушено. Заболевание проявляется тяжёлой системной дисплазией скелета, поражением сердечно-сосудистой и дыхательной систем, а также жизнеугрожающим стенозом шейного отдела позвоночника. При своевременно начатой заместительной терапии прогноз благоприятный[1].
Общие сведения
История
Впервые заболевание независимо друг от друга описали в 1929 году два врача: англичанин Дж. Ф. Брейлсфорд и уругвайский педиатр Л. Моркио[1].
Классификация
Различают несколько форм мукополисахаридоза IV типа[2]:
- тяжёлую или классическую;
- лёгкую.
Этиология
Этиология СМ связана с мутациями в гене GALNS, который локализован на хромосоме 16q24.3, состоит из 14 экзонов и 13 интронов и кодирует белок из 522 аминокислот. Известно более 360 патогенных вариантов этого гена, которые в гомозиготном или компаунд-гетерозиготном состоянии вызывают снижение активности фермента N-ацетилглюкозамин-6-сульфатной сульфатазы. В результате в различных тканях организма накапливаются гликозаминогликаны — хондроитин-6-сульфат и кератансульфат[1][3].
Патогенез
Мутации в гене GALNS приводят к снижению активности фермента по четырём различным механизмам, что обусловливает широкий спектр клинической тяжести заболевания — от тяжёлых до более лёгких фенотипов. Дефицит фермента N-ацетилгалактозамин-6-сульфатазы ведёт к патологическому накоплению в тканях, прежде всего в костной и хрящевой, гликозаминогликанов — кератансульфата и хондроитин-6-сульфата. Это запускает каскад нарушений: избыточное отложение субстратов повреждает клетки и внеклеточный матрикс, нарушает нормальное формирование скелета, вызывает прогрессирующую дисплазию, что клинически проявляется низким ростом, деформациями позвоночника и грудной клетки, а также нестабильностью суставов[3].
Эпидемиология
СМ является крайне редким заболеванием: его распространённость варьирует в зависимости от популяции и составляет от 1 случая на 640 000 живорождённых детей в Австралии до 1 на 76 000 живорождённых детей в Северной Ирландии[1].
Распространённость СМ в России не определена. Имеются единичные публикации клинических наблюдений пациентов с данным заболеванием[4].
Диагностика
Клиническая картина СМ характеризуется выраженным полиморфизмом[1]:
- СМ характеризуется низким ростом, грубыми чертами лица, которое нередко имеет треугольную форму. Типичны прогнатия, макростомия (большой рот), широкие межзубные промежутки и сероватый оттенок эмали зубов, а также помутнение роговицы. Шея обычно короткая. Изменения костно-суставного аппарата — самые частые проявления СМ, встречающиеся при любой степени тяжести. Наиболее распространены кифосколиоз и килевидная деформация грудной клетки с веслообразным расширением рёбер, которые со временем усугубляются. Рост пациентов задержан: дети растут примерно до 10 лет, а пубертатного скачка роста обычно не наблюдается. Характерны также прогрессирующие деформации нижних конечностей, включая вальгусную деформацию ног, и нарушения походки. Возможны подвывихи или вывихи бедра; связанный с ними болевой синдром уже в подростковом возрасте может приковать пациента к инвалидному креслу. Отмечается гипермобильность в голеностопных и лучезапястных суставах;
- с раннего возраста дети часто болеют респираторными инфекциями. Из-за отложения веществ, особенностей костей черепа, позвоночника, грудной клетки и низкого роста происходит сужение и извитость дыхательных путей, деформация трахеи, развивается трахеобронхомаляция;
- со стороны глаз развиваются диффузное помутнение роговицы и нарушения рефракции (астигматизм, близорукость, дальнозоркость), что приводит к снижению остроты зрения и нарушению световой чувствительности. Описаны также катаракта, глаукома, ретинопатия и отёк диска зрительного нерва;
- снижение слуха чаще связано с рецидивирующими инфекциями дыхательных путей, повторными отитами и деформацией слуховых косточек; оно может быть нейросенсорным или смешанным;
- одними из ранних проявлений со стороны желудочно-кишечного тракта служат пупочные, паховые и диафрагмальные грыжи (часто рецидивирующие). Может отмечаться увеличение печени, реже — селезёнки, а также запоры и диарея. Зубы небольшие, широко расставленные, с истончённой остроконечной эмалью; встречаются различные аномалии развития как молочных, так и постоянных зубов;
- сердечно-сосудистая система обычно поражается в лёгкой форме: возможны недостаточность или стеноз клапанов, тахикардия, небольшой диаметр левого желудочка, артериальная гипертензия. Примерно у каждого 6 пациента наблюдается дилатация аорты из-за снижения эластичности её стенки;
- часто диагностируется компрессионная миелопатия шейного отдела позвоночника, которая проявляется слабостью в конечностях, нарушением походки, неуклюжестью, расстройством мелкой моторики, болями, потерей чувствительности, дисфункцией тазовых органов, а в тяжёлых случаях — параличом и спастическим парапарезом.
Молекулярно-генетический анализ: характерно выявление мутаций в гене GALNS[5].
Определение активности фермента GALNS позволяет выявить снижение активности фермента[5].
Рентгенологические изменения скелета включают гипоплазию зубовидного отростка с последующей нестабильностью шейного отдела позвоночника. Наблюдается кифоз, который вызывает сутулость или образование горба. Также выявляется структурный кифоз (гиббус) с клиновидной деформацией одного или нескольких смежных позвонков. Рентгенологические аномалии поясничного отдела могут обнаруживаться уже при рождении у младенцев с быстро прогрессирующим течением болезни. Кроме того, характерны сколиоз, килевидная или воронкообразная деформация грудной клетки, а также укорочение локтевых костей и локтевое отклонение лучевого эпифиза. Отмечается задержка костного созревания. Пястные кости укорочены, при этом проксимальные концы второй-пятой пястных костей имеют закруглённую или заострённую форму. К другим признакам относятся расширенные крылья подвздошных костей, уплощение головок бедренных костей и вальгусная деформация (coxa valga)[5][6].
Эхокардиография: используется для выявления пороков сердца[6].
Офтальмоскопия: используется для выявления катаракты, атрофии зрительного нерва и ретинопатии[6].
Аудиометрия: используется для выявления снижения слуха[6].
Дифференциальная диагностика
Дифференциальная диагностика СМ проводится со следующими заболеваниями[4][6]:
- спондилоэпифизарная дисплазия;
- болезнь Легга — Кальве — Пертеса;
- другие типы мукополисахаридозов.
Осложнения
Грозным осложнением СМ является синдром обструктивного апноэ сна. Трахея становится непропорционально длинной в ограниченном пространстве, что делает её извитой и может вызывать сдавление брахиоцефальной артерией. Это, наряду с сужением просвета трахеи и бронхов, провоцирует обструкцию нижних дыхательных путей, храп, ночное апноэ и при тяжёлом течении — лёгочную гипертензию[1].
Лечение
Основным методом лечения СМ является ферментозаместительная терапия препаратом элосульфаза альфа. Этот препарат представляет собой генно-инженерный фермент человеческой N-ацетилгалактозамин-6-сульфатазы, к которому присоединена концевая олигосахаридная цепь с маннозо-6-фосфатом. Благодаря этому после внутривенного введения фермент распознаётся клетками через маннозо-6-фосфатный рецептор и интернализуется в лизосомы. Данный механизм основан на принципе перекрёстной коррекции: поглощённый фермент повышает специфическую ферментативную активность, запускает катаболизм кератансульфата и хондроитин-6-сульфата и тем самым предотвращает их дальнейшее накопление в клетках[3].
Прогноз
Прогноз заболевания напрямую зависит от своевременности начала ферментозаместительной терапии: при условии раннего лечения он становится благоприятным. При лёгких формах СМ отмечаются умеренные костные изменения и менее частое поражение внутренних органов; такие пациенты могут сохранять относительно хорошее качество жизни вплоть до 50-60 лет[3].
Диспансерное наблюдение
Диспансерное наблюдение за пациентом с СМ предполагает регулярное медицинское сопровождение несколькими специалистами: ортопедом, неврологом, кардиологом, оториноларингологом и офтальмологом. Объём и частота контрольных обследований определяется индивидуально[3].
Профилактика
Медико-генетическая консультация является важной мерой профилактики СМ. На этапе планирования беременности специалист оценивает риск рождения больного ребёнка, выявляет носительство мутаций в семье и при необходимости назначает пренатальное или преимплантационное тестирование. Это позволяет предотвратить появление ребёнка с тяжёлым наследственным заболеванием[6].
Примечания
Литература
- Бурлуцкая А. В., Савельева Н. В., Науменко Г. В. Мукополисахаридоз IVА типа у детей: клинические случаи // Кубанский научный медицинский вестник. — 2022. — Т. 29, № 1. — С. 119—131. — doi:10.25207/1608-6228-2022-29-1-119-131.
- Sawamoto K., Álvarez González J. V., Piechnik M., et al. Mucopolysaccharidosis IVA: Diagnosis, Treatment, and Management (англ.) // International Journal of Molecular Sciences. — 2020. — Vol. 21, no. 4. — P. 1517. — doi:10.3390/ijms21041517.
- Съёмщикова Ю. П., Козлов Ю. А., Яковлев А. Б., и др. Редкий случай синдрома Моркио (мукополисахаридоз IVА типа): трудности диагностического поиска и лечения // Педиатрическая фармакология. — 2022. — Т. 19, № 1. — С. 39—44. — doi:10.15690/pf.v19i1.2352.
- Вашакмадзе Н. Д., Журкова Н. В., Михайлова Л. К., и др. Клиническая характеристика пациента с мукополисахаридозом, тип IVА (синдромом Моркио) // Вопросы современной педиатрии. — 2022. — Т. 21, № 6S. — С. 529—534. — doi:10.15690/vsp.v21i6S.2499.