Болезнь Шиндлера
Болезнь Ши́ндлера (БШ) — очень редкое наследственное заболевание, относящееся к группе лизосомных болезней накопления. Характеризуется клинически гетерогенным течением, тяжесть симптомов варьируется в зависимости от типа патологии. Выделяют три типа заболевания, каждый из которых дебютирует в разном возрасте. Болезнь возникает из-за недостаточности фермента α-N-ацетилгалактозаминидазы. Дефицит этого фермента приводит к внутриклеточному накоплению олигосахаридов и гликопептидов, а также их избыточному выделению с мочой. Лечение носит симптоматический характер. Причиной заболевания служат мутации в гене NAGA[2].
Общие сведения
История
В 1988 году немецкий врач Детлев Шиндлер и его коллеги впервые описали это редкое заболевание. В их исследовании участвовали дети 3-4 лет с тяжёлыми неврологическими нарушениями: психомоторной отсталостью, миоклоническими судорогами, слепотой и полной утратой контакта с внешним миром. При этом обследование периферических нервов не показало значимых изменений, но в слизистой прямой кишки обнаружились патологические изменения аксонов, характерные для нейроаксональной дистрофии[2].
Чуть позже, в 1989 году, японский учёный Тамотсу Канзаки и его команда выявили другую форму болезни у 46-летней женщины с множественными ангиокератомами. Несмотря на разницу в симптомах, причина оказалась той же — дефицит фермента α-N-ацетилгалактозаминидазы[2].
В ходе исследований 1990-х годов было установлено, что все формы болезни связаны с мутациями в гене NAGA, который кодирует дефектный фермент, лежащий в основе патологического процесса[2].
Классификация
Классификация БШ[2]:
- тип I — тяжёлая младенческая форма с прогрессирующей неврологической дегенерацией;
- тип II (болезнь Канзаки) — взрослая форма, проявляющаяся ангиокератомами без неврологических нарушений;
- тип III — промежуточный вариант с более мягким течением.
Этиология
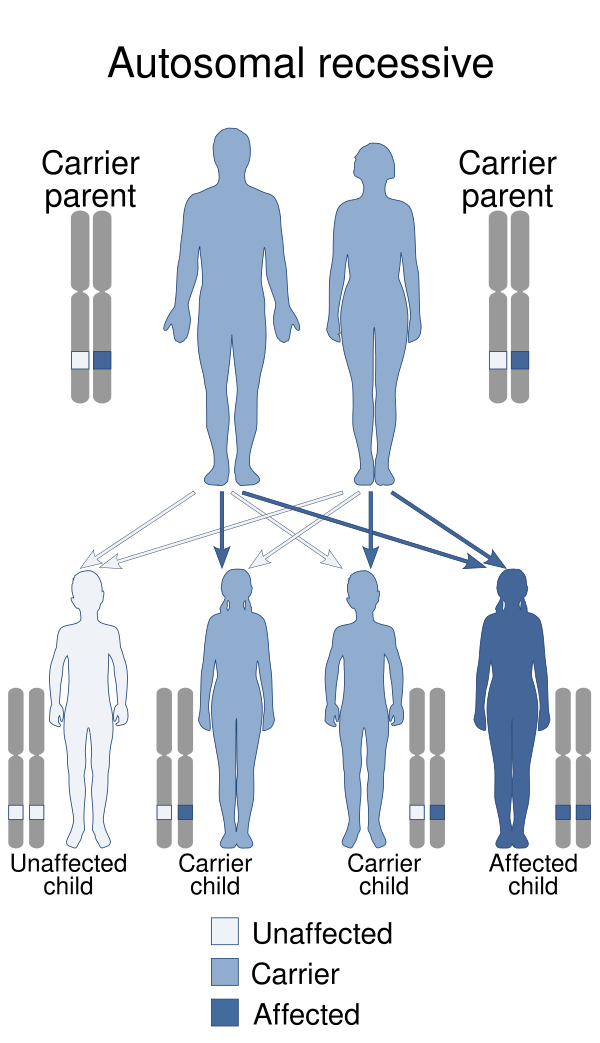
БШ обусловлена мутацией в гене NAGA, расположенном в длинном плече 22-й хромосомы (локус 22q13.2). Этот ген кодирует фермент α-N-ацетилгалактозаминидазу, который функционирует в лизосомах — клеточных органеллах, отвечающих за переработку и утилизацию различных веществ. В лизосомах данный фермент участвует в расщеплении гликопротеинов и гликолипидов — сложных комплексов, состоящих из сахаров, связанных с белками и жирами. Конкретно α-N-ацетилгалактозаминидаза отвечает за отщепление молекулы α-N-ацетилгалактозамина от сахарных компонентов этих комплексов. Заболевания наследуется по аутосомно-рецессивному типу[3].
Патогенез
Мутации в гене NAGA нарушают функцию фермента α-N-ацетилгалактозаминидазы, препятствуя его участию в расщеплении гликопротеинов и гликолипидов. В результате эти вещества накапливаются в лизосомах, что приводит к нарушению работы клеток и их последующей гибели. Повреждение клеток нервной системы и других тканей организма вызывает характерные клинические проявления СШ[3].
Эпидемиология
БШ является крайне редким заболеванием с неизвестной распространённостью. Согласно медицинским данным, к 2021 году в мире было зарегистрировано около 20 случаев этой патологии. На территории России случаи БШ к 2021 году официально не отмечались[2].
Диагностика
Клиническая картина
БШ I типа, классическая форма заболевания, начинается в младенческом возрасте. Поражённые дети развиваются нормально примерно до 9 месяцев — 1 года. Затем у них может наблюдаться задержка психомоторного развития. После периода таких задержек развития поражённые дети могут начать терять ранее приобретённые физические и умственные способности. Такой регресс может начаться примерно в 2-летнем возрасте. Затем у поражённых детей могут проявиться мышечная слабость, снижение мышечного тонуса, мышечные спазмы, приводящие к медленным, скованным движениям, косоглазия, нистагм и ухудшение зрения из-за постепенной дегенерации зрительных нервов (атрофия зрительного нерва). Они также могут испытывать кратковременные, спазмы мышц рук, ног или всего тела[4].
При БШ II типа симптомы могут не проявляться до второго или третьего десятилетия жизни. Характерным признаком БШ II типа является поражение мелких кровеносных сосудов кожи, вызывающее небольшие красноватые кожные поражения, а также гиперкератоз, что обозначается как ангиокератомы. Расширение мелких лимфатических сосудов может приводить к отёкам, особенно нижних конечностей. Ангиокератомы могут сначала ограничиваться одной областью, например нижней частью туловища, а затем появляться и в других местах (например, распространяться от нижней части туловища к области груди). Эти красноватые поражения могут быть плоскими или выпуклыми, различаться по цвету и располагаться группами. У поражённых лиц такие поражения могут также наблюдаться на других участках тела, включая слизистые оболочки рта и глаз[4].
При этом у пациентов с БШ II типа отмечается снижение когнитивных функций, но серьёзные неврологические осложнения, характерные для БШ I типа, отсутствуют. У таких пациентов могут также развиваться грубые черты лица, утолщённые губы, уплощённая переносица и увеличенный кончик носа. В медицинской литературе описаны дополнительные симптомы: головокружение, потеря слуха, шум в ушах и мышечная слабость. Пациенты могут также испытывать болевые кризы[4].
БШ III типа представляет собой промежуточную форму заболевания. Симптоматика может варьировать от выраженных проявлений, включающих интеллектуальные нарушения, неврологическую дисфункцию и судорожные приступы, до более лёгких неврологических и психиатрических расстройств, например, задержка речевого развития и лёгкие симптомы, сходные с проявлениями аутизма[4].
Лабораторная диагностика
Клинический анализ мочи: отмечается повышение концентрации олигосахаридов и гликопептидов[2].
Флуориметрический метод: отмечается снижение активности α-N-ацетилгалактозаминидазы в фибробластах, в плазме и лимфоцитах[2].
Молекулярно-генетический анализ: характерно выявление мутации в гене NAGA методом секвенирования[2].
Пренатальная диагностика
Для семей с отягощённым анамнезом по БШ возможно проведение пренатальной диагностики заболевания с помощью амниоцентеза и биопсии ворсин хориона последующим молекулярно-генетическим анализом[4].
Дифференциальная диагностика
Дифференциальная диагностика БШ проводится со следующими состояниями[4]:
- инфантильная нейроаксональная дистрофия;
- болезнь Фабри.
Лечение
На сегодняшний день не существует эффективного метода лечения БШ, и все клинические мероприятия направлены на облегчение состояния пациентов. Лечение БШ носит симптоматический и поддерживающий характер. Терапевтическая стратегия требует комплексного подхода с участием команды специалистов, включая педиатра, детского невролога, физиотерапевта, сурдолога, кардиолога, гепатолога и других медицинских работников[3].
Для контроля симптомов пациентам могут назначаться противосудорожные препараты и миорелаксанты. В случае развития лимфедемы используется компрессионная терапия, а при тяжёлых формах — хирургические методы лечения[2].
Прогноз
Прогноз при БШ остаётся неопределённым в связи с исключительной редкостью патологии. Согласно имеющимся клиническим наблюдениям, заболевание I типа отличается крайне агрессивным течением с летальным исходом в раннем детском возрасте либо необходимостью пожизненного паллиативного ухода. В то же время при II типе болезни в медицинской литературе описаны случаи относительно благоприятного течения с сохранением жизнеспособности пациентов до пожилого возраста[2].
Профилактика
Не разработана.
Диспансерное наблюдение
Пациентам с БШ показано пожизненное наблюдение у офтальмолога, нефролога и психиатра[2].
Примечания
Литература
- Алифирова В.М., Валикова Т.А., Николаева Т.Н., Пугаченко Н.В., Вторушин С.В. Болезнь Шиндлера (клинический случай) // Бюллетень сибирской медицины : журнальная статья. — 2013. — Т. 12, № 5. — С. 133—138. — ISSN 1682-0363. — doi:10.20538/1682-0363-2013-5-133-138.