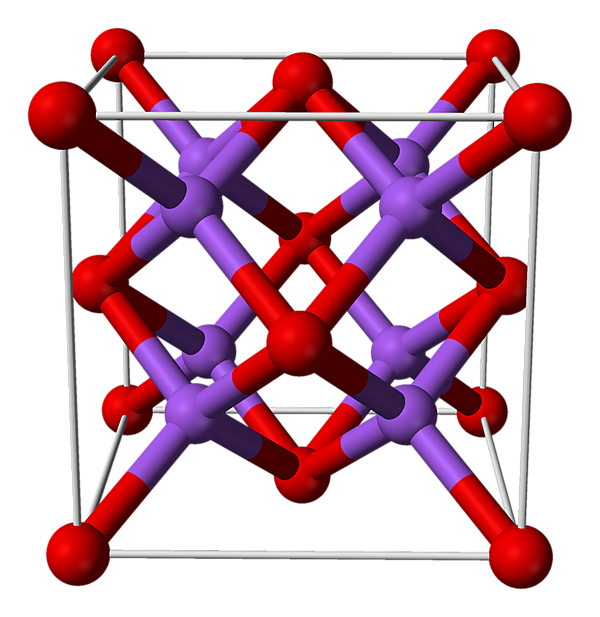
Оксид натрия
Окси́д на́трия (окись натрия) — бинарное неорганическое бесцветное вещество, имеющее химическую формулу Na2O. Типичный представитель основных оксидов. Бурно реагирует с водой.
Общие сведения
| Оксид натрия | |
|---|---|
| Общие | |
| Традиционные названия | окись натрия, натр |
| Хим. формула | Na2O |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 61,979 г/моль |
| Плотность | 2,27 (20 °C) |
| Термические свойства | |
| Температура | |
| • плавления | 1132 °C |
| • кипения | 1950 °C |
| Энтальпия | |
| • образования | −416 кДж/моль |
| Классификация | |
| Рег. номер CAS | 1313-59-3 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 73971 |
| UNII | 3075U8R23D |
| CompTox Dashboard EPA | DTXSID0049781 |
| Рег. номер EINECS | 215-208-9 |
| SMILES | |
| InChI | |
| Номер ООН | 1825 |
| ChemSpider | 66599 |
| ECHA InfoCard | 100.013.827 |
| Безопасность | |
| Пиктограммы ECB |
|
| NFPA 704 | |
Описание
Получение
1. Взаимодействие металлического натрия с кислородом:
Чистый оксид натрия получить непосредственным окислением натрия нельзя, так как образуется смесь, состоящая из 80 % оксида натрия и 20 % пероксида натрия:
2. Взаимодействие металлического натрия с нитратом натрия:
3. Прокаливание пероксида натрия с избытком натрия:
4. Прокаливанием карбоната натрия при 1000 °C, получаемого в свою очередь прокаливанием гидрокарбоната натрия при 200 °C.
5. Разложением нитрита натрия.
Химические свойства
1. При нагревании разлагается до пероксида натрия[1]:
2. Взаимодействие с водой с образованием щёлочи:
- Данная реакция сильно экзотермична, вода при реакции с окисью натрия закипает.
3. Взаимодействие с кислотными оксидами с образованием соли:
4. Взаимодействие с кислотами с образованием соли и воды:
5. Взаимодействие с жидким аммиаком с образованием амида:
6. Окисление кислородом до пероксида[1]:
Применение
Оксид натрия применяется, в основном, в качестве реактива для различных синтезов, для приготовления гидроксида натрия, динептуната(VI) натрия и других веществ.
Примечания
Литература
- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A23. ISBN 978-0-618-94690-7.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3 (Мед-Пол). — 639 с. — ISBN 5-82270-039-8.
- Химические свойства неорганических веществ / под ред. Р.А. Лидина. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.




![{\displaystyle {\ce {NaHCO_{3}->[{T=200}][{H_{2}O+CO_{2}}]Na_{2}CO3->[{T=1000}][{CO_{2}}]Na_{2}O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/a8745afe18b26884d2274af7ff87d73943dfbabd)