Экзотермические реакции
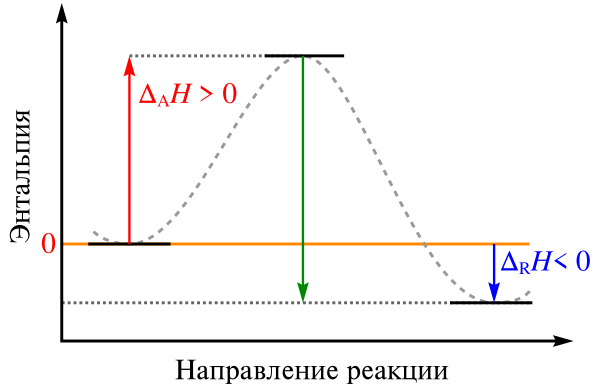
Экзотерми́ческая реа́кция (от греч. ἔξω экзо — наружу и θερμός термос — теплота) — химическая или ядерная реакция, сопровождающаяся выделением теплоты. По знаку тепловыделения противоположна эндотермической реакции — реакции с поглощением теплоты[1].
Полное количество внутренней энергии в любой системе измерить или вычислить достаточно трудно, а вот найти изменение энергии в реакции гораздо легче проще как измерить, так и вычислить. Для измерения изменения энергии химических реакций обычно используют калориметры, а измерения энергии в ядерных реакциях вычисляют по энергиям и массам продуктов реакции.
С изменением энергии тесно связано изменение энтальпии () поэтому во многих случаях эти величины часто путают. Изменение энергии равно изменению энтальпии, если реакция происходит при постоянном объёме[2]. Если реакция происходит при постоянном давлении, то часть выделившейся энергии может расходоваться на работу против сил давления за счёт изменения объёма продуктов реакции, и, соответственно, тепловой эффект экзотермической реакции будет меньше. Для реакций, не сопровождающихся выделением или поглощением газов, или если число молей газа до и после реакции не изменяется, изменение энергии и изменение энтальпии практически равны.
Измеренное значение соотносится с энергией связи молекул следующим образом:
— это энергия, потраченная на разрыв связей в исходных веществах, минус энергия, выделившаяся при образовании связей или разрыв связей в продуктов реакции.
Для экзотермических реакций эта формула даёт отрицательное значение для , так как большее значение вычитается из меньшего значения.
При сгорании водорода, например:
и изменение энтальпии равно ΔH = −483,6 кДж на один моль молекул кислорода .
К экзотермическим относятся реакции: горения, окисления, соединения металлов с другими элементами, радиоактивный распад и ядерный синтез лёгких элементов и т. д.
Примеры
- Горение топлива в кислороде воздуха.
- Горение пороха.
- Добавление концентрированной серной кислоты в воду.
- Окисление жиров и углеводов в живых организмах.
- Адиабатическое горение
- Ядерный взрыв.
- Отверждение эпоксидной смолы или бетона
Примечания
Литература
- Никольский Б. П. и др. Справочник химика. Общие сведения. Строение вещества. Свойства важнейших веществ. Лабораторная техника. — Москва, Ленинград : Химия, 1966.
- Рабинович В. А., Хавин З. Я. и др. Краткий химический справочник. — Ленинград : Химия, 1978.
- Сивухин Д. В. Общий курс физики. Т. 2. Термодинамика и молекулярная физика. — Москва : Физматлит, 2014.
- Савельев И. В. Курс общей физики. В 5 томах. Том 3. Молекулярная физика и термодинамика — Москва : Лань, 2021.