Оксид галлия(III)
Оксид галлия — амфотерный оксид, бинарное неорганическое соединение металла галлия и кислорода с формулой Ga2O3, белые кристаллы, полупроводник.
Общие сведения
| Оксид галлия(III) | |
|---|---|
| Общие | |
| Систематическое наименование |
Оксид галлия |
| Хим. формула | Ga2O3 |
| Физические свойства | |
| Состояние | белые кристаллы |
| Молярная масса | 187,44 г/моль |
| Плотность | α-6,48; β-5,88 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1725; 1740 °C |
| Мол. теплоёмк. | 92,18 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1090 кДж/моль |
| Классификация | |
| Рег. номер CAS | 12024-21-4 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 5139834 |
| UNII | 46F059V66A |
| CompTox Dashboard EPA | DTXSID9031359 |
| Рег. номер EINECS | 234-691-7 |
| SMILES | |
| InChI | |
| RTECS | LW9650000 |
| ChemSpider | 4313617 |
| ECHA InfoCard | 100.031.525 |
Получение
Физические свойства
Оксид галлия — белый или жёлтый порошок, существует в двух модификациях:
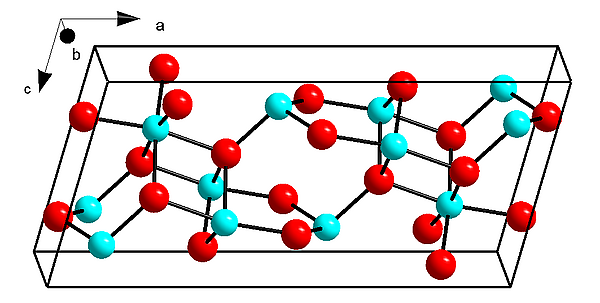
- α-Ga2O3 образует кристаллы тригональной сингонии, пространственная группа R 3c, параметры ячейки a = 0,4972 нм, c = 1,3402 нм, Z = 6.
- β-Ga2O3 — кристаллы моноклинной сингонии, пространственная группа C 2/m, параметры ячейки a = 12,214 А, b = 3,0371 А, c = 5,7981 А, β = 103,83, Z = 4.
β-форма является наиболее стабильной.
Химические свойства
- Реагирует с концентрированными кислотами:
- и щелочами:
- При сплавлении со щелочами образует метагаллаты:
- Восстанавливается водородом до металла:
- Реагирует при сплавлении с хлористым аммонием:
- При прокаливании в токе аммиака образует нитрид галлия:
- С карбонатом цинка при высоких температурах образует шпинель[1]:
- При сплавлении с галлием образует окись галлия(I):
Применение
Для получения галлиево-гадолиниевого граната и других соединений галлия.
В полупроводниковой промышленности (приборы силовой электроники)[2][3].
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.






![{\displaystyle {\mathsf {Ga_{2}O_{3}+2NaOH+3H_{2}O\ {\xrightarrow {}}\ 2Na[Ga(OH)_{4}]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/80b88c31b6d5faf01083a91b5452340a89bab807)