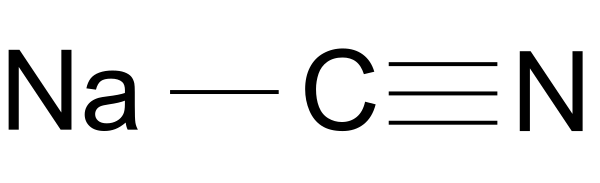Цианид натрия
Циани́д на́трия (циа́нистый на́трий, химическая формула — NaCN) — это неорганическая натриевая средняя соль синильной кислоты.
При стандартных условиях, цианид натрия — это ядовитые бесцветные кристаллы, легко растворяющиеся в воде.
Общие сведения
| Цианид натрия | |
|---|---|
| Общие | |
| Систематическое наименование |
Цианид натрия |
| Традиционные названия | Цианистый натрий |
| Хим. формула | NaCN |
| Физические свойства | |
| Состояние | Твёрдое |
| Молярная масса | 49.01 г/моль |
| Плотность | 1,5955 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 564 °C |
| • кипения | 2725 ± 1[1] |
| Давление пара | 0 ± 1[1] |
| Классификация | |
| Рег. номер CAS | 143-33-9 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 8929 |
| UNII | O5DDB9Z95G |
| CompTox Dashboard EPA | DTXSID4024309 |
| Рег. номер EINECS | 205-599-4 |
| SMILES | |
| InChI | |
| RTECS | VZ7525000 |
| ChEBI | 33192 |
| Номер ООН | 1689 |
| ChemSpider | 8587 |
| ECHA InfoCard | 100.005.091 |
| Безопасность | |
| Предельная концентрация | 0,3 мг/л - в воздухе; в воде - 0,03 мг/л |
| ЛД50 | 0,1-14,3 мг/кг |
| Токсичность | Чрезвычайно ядовит, СДЯВ |
| Пиктограммы СГС |
|
| NFPA 704 | |
Свойства
Бесцветные гигроскопичные кристаллы, хорошо растворимые в воде (33,4 % при +10 °C, 45,0 % при +35 °C). Кристаллизуется в виде дигидрата NaCN•2H2O, выше +34,7 °C — в безводной форме.
В водных растворах гидролизуется с получением синильной кислоты и гидроксида натрия:
Как и цианид калия (KCN), цианид натрия легко образует комплексные соединения.
Получение
Основной способ получения цианида натрия в промышленности — нейтрализация синильной кислоты гидроксидом натрия NaOH:
Применение
- Извлечение драгоценных металлов (золота, серебра) из руд[2] методом селективного выщелачивания;
- Цианирующий агент в производстве нитрилов, изонитрилов, красителей (индиго);
- Для повышения поверхностной твёрдости, износостойкости и воспрепятствования усталости стальных изделий (так называемое «цианирование стали»);
- Пайка и жидкая цементация металлов, при бронзировании и оцинковке, при серебрении зеркал;
- В фотографии и литографии;
- В производстве фармацевтических препаратов;
- Для борьбы с вредителями сельского хозяйства[3].
Токсичность
Цианид натрия, как и все цианиды, чрезвычайно ядовит. Механизм действия при отравлении аналогичен цианиду калия, сила воздействия также сравнима[2]. При попадании в организм он ингибирует ферменты тканевого дыхания, и ткани теряют способность усваивать кислород из крови[4].
ПДК в рабочей зоне — 0,3 мг/м3 (контроль по HCN).
Одним из антидотов являются сахара́, образующие с цианогруппой нерастворимые соединения[4].
Относится ко 2-му классу опасности.
Примечания