Синдром Веста
Синдро́м Ве́ста (СВ; синдро́м инфанти́льных эпилепти́ческих спа́змов) — форма младенческой эпилептической энцефалопатии. Её определяют по трём ключевым признакам: инфантильные спазмы (судорожные приступы), специфическая картина на электроэнцефалограмме, называемая гипсаритмией, и сопутствующая задержка психомоторного развития. Для лечения этого состояния применяют противоэпилептические препараты, кетогенную диету, а в некоторых случаях и хирургические методы. Прогноз заболевания у детей сильно варьируется и определяется целым комплексом различных факторов, однако в целом является неблагоприятным[1].
История
Впервые СВ был описан Уильямом Джеймсом Вестом (1793—1848) в 1841 году на примере своего собственного сына, Джеймса Эдвина (1840—1860). Впоследствии заболевание получило название «синдром Веста». Со временем для его обозначения начали использовать термин «инфантильные спазмы», который отражал ключевое клиническое проявление заболевания. Позже, поскольку начало болезни может выходить за рамки младенческого возраста, был введён более общий термин «эпилептические спазмы»[2].
Классификация
СВ входит в группу заболеваний, относящихся к эпилептическим энцефалопатиям[3].
Этиология
СВ может быть вызван различными факторами, часть из которых остаётся неизвестной, а другие хорошо изучены. К последним относятся структурные изменения головного мозга, инфекционные, метаболические и иммунологические нарушения, а также генетические аномалии. Эти факторы могут выступать как единственной причиной, так и действовать в сложной комбинации. Чёткое разделение по этиологии часто затруднительно, поскольку разные события могут сочетаться. Примерно в 35 % случаев причина спазмов остаётся невыясненной. К возможным этиологическим факторам относятся[2]:
- генетические факторы: генетическая предрасположенность подтверждается семейными случаями эпилепсии и наблюдениями за однояйцевыми близнецами, у которых спазмы начинались практически одновременно, что может указывать на запрограммированный молекулярный триггер или одновременное воздействие внешних факторов на генетически уязвимый организм. Прямое вовлечение генов в этиологию инфантильных спазмов связано, в частности, с мутациями в генах ARX и CDKL5, расположенных на Х-хромосоме и играющих ключевую роль в развитии мозга. Часто ассоциированы с инфантильными спазмами и мутации в других генах, таких как PAFAH1B1/LIS1, DCX, TUBA1A, STXBP1, KCNQ2, GRIN2A/B, MAGI2, SPTAN1, FOXG1 и многих других. Эти гены часто экспрессируются в ГАМК-ергических нейронах, и их нарушение приводит к сбоям в нейрональной миграции и организации коры головного мозга. Исследования выявляют у пациентов разнообразные хромосомные микроделеции и микродупликации, которые могут выступать как прямой причиной, так и фактором риска развития спазмов;
- структурные аномалии головного мозга: к СВ могут приводить различные структурные нарушения развития головного мозга, такие как лиссэнцефалия, фокальная корковая дисплазия, полимикрогирия, гемимегалэнцефалия и перивентрикулярная узловая гетеротопия. Например, гены PAFAH1B1/LIS1 и DCX, связанные с классической лиссэнцефалией, ассоциированы со спазмами примерно у 80 % поражённых детей;
- комплексные синдромы пороков развития: СВ часто наблюдается в рамках известных генетических синдромов, таких как синдром Дауна, синдром Паллистера — Киллиана, синдром Вильямса — Бойрена, а также синдромы Смита — Лемли — Опица, Смита — Магениса и Сотоса. Спазмы являются ключевым проявлением таких специфических синдромов, как синдром PEHO и синдром Экарди;
- врождённые метаболические нарушения: ряд метаболических заболеваний может манифестировать СВ. К ним относятся фенилкетонурия, глициновая энцефалопатия, недостаточность пиридоксина, нарушения цикла мочевины (например, метилмалоновая и пропионовая ацидемия), болезнь «кленового сиропа», дефекты окисления жирных кислот, нарушения митохондриального и пероксисомального обменов, а также лизосомные болезни накопления, например, болезнь Краббе и болезнь Менкеса;
- факоматозы: СВ может быть ранним проявлением факоматозов. Наиболее характерным примером является туберозный склероз. Реже СВ наблюдается при нейрофиброматозе I типа, синдроме Стерджа — Вебера и пигментном мозаицизме (гипомеланозе Ито). В основе эпилепсии при этих синдромах лежат структурные нарушения развития мозга, вызванные генетическими дефектами;
- иммунологические факторы: изучается возможная роль иммунных механизмов в запуске инфантильных спазмов. Это связано с тем, что некоторые гены, вовлечённые в патогенез спазмов, также участвуют в воспалительных каскадах. Описаны случаи СВ у детей с повышенным титром антител к потенциал-зависимым калиевым каналам, что указывает на потенциальный аутоиммунный компонент у части пациентов.
Патогенез
Патогенез СВ изучен недостаточно. Современные исследования на животных моделях концентрируются на конкретных факторах, таких как потеря интернейронов, воспалительные или иммунные реакции, роль стресса и действие кортикотропин-рилизинг гормона[4].
Другие животные модели указывают на общий механизм развития спазмов, связанный с утратой тормозного контроля, опосредованного гамма-аминомасляной кислотой. Это объясняет происхождение инфантильных спазмов, которое может быть следствием аномалии развития головного мозга или корково-подкорковой десинхронизации (фокальной или диффузной). Такое нарушение приводит к патологическому функциональному взаимодействию с структурами ствола мозга, что и проявляется характерными эпилептическими спазмами[4].
Эпидемиология
СВ составляет около 2 % от всех случаев детской эпилепсии, однако на его долю приходится 25 % эпилепсий, манифестирующих на первом году жизни. Распространённость синдрома оценивается в 2,5—6 случаев на 10 000 новорождённых. Распространённость среди детей в возрасте до 10 лет составляет 1,5—2 случая на 10 000. В разных регионах мира распространённость СВ варьируется от 0,05 до 0,41 случая на 1000 детей, а доля этого синдрома среди всех детских эпилепсий — от 1,4 до 7,6 %. Мальчики болеют несколько чаще девочек, но значимых гендерных различий не отмечено. В 90 % случаев заболевание дебютирует у детей младше 12 месяцев, с пиком начала в возрасте от 4 до 6 месяцев[5].
Диагностика
СВ характеризуется эпилептическими приступами в виде спазмов, дебютирующими в младенческом или раннем детском возрасте. Сами спазмы вовлекают мышцы шеи, туловища и конечностей и могут быть сгибательными, разгибательными или смешанными. Также могут наблюдаться движения, напоминающие кивки головой или «складывание» тела. Спазмы обычно протекают в две фазы: начальная фаза имеет внезапное начало, длится менее 2 секунд и представляет собой краткое сокращение одной или нескольких мышечных групп. За ней следует менее интенсивная, но более длительная тоническая фаза продолжительностью от 2 до 10 секунд. Спазмы варьируются от единичных до более сотни за приступ и возникают сериями продолжительностью от менее минуты до 10 минут. Как правило, они происходят в состоянии бодрствования, в дневное время. Сопутствующими проявлениями могут быть двигательная пауза длительностью до 90 секунд, ритмичные нистагмоидные движения глаз или девиация глазных яблок. Также могут отмечаться изменения дыхательного ритма. СВ сопровождается задержкой и регрессом моторного и когнитивного развития. Регресс может затрагивать такие аспекты развития, как перевороты, сидение, ползание или лепет. Родители также могут отмечать потерю социального взаимодействия и улыбки, повышенную раздражительность или молчаливость ребёнка. Всё вышеописанное обычно развивается в несколько стадий[6]:
- Первая стадия относительно мягкая, со спазмами низкой частоты и в изолированной форме. Она ассоциирована с началом регресса развития.
- Вторая стадия является более тяжёлой, с учащением спазмов и их возникновением в сериях. Регресс развития становится более выраженным.
- Третья стадия характеризуется прогрессирующим снижением частоты и тяжести спазмов. Спазмы могут полностью разрешиться, но зачастую сменяются другими типами эпилептических приступов.
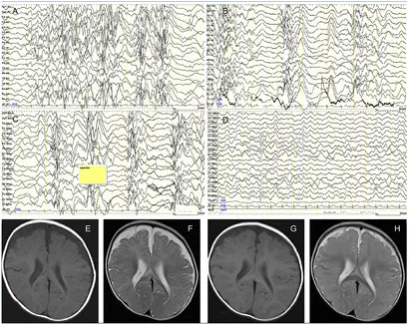
Электроэнцефалография: характерной находкой для диагностики инфантильных спазмов является паттерн гипсаритмии. Он характеризуется высоковольтными, хаотичными медленными волнами и пиками во всех корковых областях. Пики могут возникать генерализованно, но они никогда не бывают ритмичными или организованными. Другие межприступные паттерны у пациентов с СВ включают фокальные или мультифокальные пики и острые волны, диффузное или фокальное замедление, пароксизмальные вспышки медленной или быстрой активности, а также паттерны «медленный пик — волна»[6].
Компьютерная томография головного мозга: структурные аномалии головного мозга, такие как гидроцефалия, гидранэнцефалия, шизэнцефалия и агенезия мозолистого тела, могут быть выявлены с помощью компьютерной томографии. Кроме того, церебральные кальцификаты можно наблюдать у пациентов с туберозным склерозом или внутриутробными инфекциями[5].
Магнитно-резонансная томография головного мозга: используется для выявления очагов корковой дисплазии, нарушений нейрональной миграции или миелинизации[5].
В некоторых случаях при СВ выявляются диффузные структурные заболевания мозга без чётких фокальных признаков на стандартной визуализации. В таких ситуациях проводится позитронно-эмиссионная томография, которая позволяет локализовать очаги патологической активности в головном мозге[6].
Для исключения метаболических причин развития эпилепсии проводится комплексная лабораторная диагностика, включающая клинический и биохимический анализ крови, клинический и биохимический анализ ликвора и биохимический анализ мочи[6][5].
Молекулярно-генетический анализ крови методом секвенирования по Сэнгеру позволяет выявить мутации в генах, приводящие к развитию СВ. К наиболее частым мутациям относятся мутации в генах ARX, CDKL5, PAFAH1B1/LIS1, DCX, TUBA1A, STXBP1, KCNQ2, GRIN2A, GRIN2B, MAGI2, SPTAN1, FOXG1[2][3].
Дифференциальная диагностика
Дифференциальная диагностика СВ проводится со следующими состояниями[3][5]:
- другие формы эпилептической энцефалопатии (синдром Леннокса — Гасто, синдром Ландау — Клеффнера, атипичная доброкачественная парциальная эпилепсия, синдром Дуза, синдром Отахары, эпилепсия младенчества с мигрирующими фокальными приступами, синдром Драве);
- доброкачественный миоклонус раннего младенчества;
- миоклонически-астатическая эпилепсия;
- абсансные приступы;
- приобретённая эпилептическая афазия;
- расстройство аутистического спектра;
- доброкачественная детская эпилепсия;
- неонатальные судороги;
- височная эпилепсия.
Осложнения
У детей с СВ часто наблюдаются нарушения нейроразвития, затрагивающие следующие сферы[6]:
- зрение;
- речь;
- слух;
- навыки письма;
- развитие мелкой и крупной моторики.
Лечение
Гормональные препараты (кортикотропин и пероральные глюкокортикостероиды) являются одними из основных препаратов. Исследования показывают, что они эффективны для краткосрочного купирования спазмов и разрешения гипсаритмии[5].
Вигабатрин признан высокоэффективным препаратом, особенно у пациентов с туберозным склерозом. Его механизм действия связан с повышением уровня ГАМК, основного тормозного нейромедиатора в центральной нервной системе. Другие противоэпилептические средства чаще рассматриваются как терапия второй линии при недостаточной эффективности или непереносимости стандартных схем. К ним относятся: топирамат, леветирацетам, вальпроевая кислота, ламотриджин, зонисамид и клоназепам[5].
Длительная пероральная терапия высокими дозами пиридоксина может быть эффективной у определённой группы пациентов, причём ответ на лечение обычно наблюдается в течение первых 1—2 недель[5].
Кетогенная диета, основанная на высоком содержании жиров и низком содержании углеводов, индуцирует состояние кетоза, что может приводить к снижению частоты приступов у части пациентов[5].
У некоторых пациентов хирургическая резекция локализованного патологического очага в головном мозге может привести к полному прекращению эпилептических приступов[5].
Прогноз
Долгосрочный общий прогноз для пациентов с СВ остаётся неблагоприятным и напрямую зависит от этиологии заболевания. У детей с идиопатической формой прогноз лучше, чем при симптоматической. Только около 14 % пациентов с симптоматическим СВ имеют нормальное или пограничное когнитивное развитие, в то время как при идиопатической форме этот показатель составляет 28—50 %. У 70 % пациентов наблюдается тяжёлая степень интеллектуальных нарушений, часто в сочетании с психиатрическими патологиями, такими как аутизм или синдром дефицита внимания и гиперактивности. Примерно у половины или даже двух третей пациентов со временем развиваются другие типы эпилептических приступов. У значительной части (18—50 %) болезнь трансформируется в синдром Леннокса — Гасто или другую форму генерализованной эпилепсии. В редких случаях сами спазмы могут сохраняться и во взрослом возрасте. Среди пациентов с симптоматической формой выделяются подгруппы с относительно более благоприятным исходом. К ним, в частности, относятся дети с синдромом Дауна и нейрофиброматозом I типа, у которых чаще наблюдается контроль над приступами и лучшие когнитивные результаты[5].
К факторам, улучшающим прогноз, относятся[5]:
- криптогенная или идиопатическая этиология;
- возраст начала заболевания старше 4 месяцев;
- отсутствие атипичных спазмов и фокальных приступов;
- отсутствие асимметричных нарушений на электроэнцефалографии;
- короткий промежуток времени от начала заболевания до старта лечения;
- ранний и стойкий положительный ответ на терапию.
Показатель смертности при данном синдроме варьируется от 5 до 31 %. Большинство летальных исходов происходит в детском возрасте, при этом значительная часть — в первые 10 лет жизни[5].
Диспансерное наблюдение
Профилактика
Не разработана.
Примечания
Литература
- Прыгунова Т.М. Исходы синдрома Веста: обзор литературы и собственные данные // Русский журнал детской неврологии. — 2019. — Т. 14, № 4. — С. 8—16.
- Barbarrosa E.P., Ferrer I.C.P., Tovani-Palone M.R. West Syndrome: Clinical Characteristics, Therapeutics, Outcomes and Prognosis (англ.) // Electronic Journal of General Medicine. — 2020. — Vol. 17, no. 2. — P. em190. — doi:10.29333/ejgm/7800.
- Corsello G., Falsaperla R., Marino S. et al. West syndrome: a comprehensive review (англ.) // Neurological Sciences. — 2020. — Vol. 41, no. 12. — P. 3547—3562. — doi:10.1007/s10072-020-04600-5.