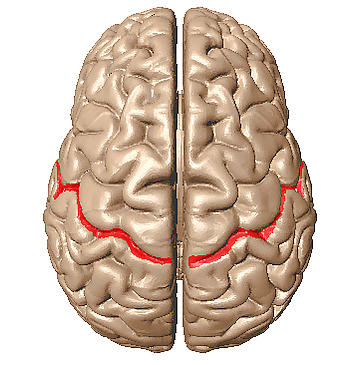
Роландическая эпилепсия
Роланди́ческая эпиле́псия (РЭ; доброка́чественная роланди́ческая эпиле́псия, самоограни́чивающаяся эпиле́псия с центротемпора́льными спа́йками, доброка́чественная де́тская эпиле́псия с центротемпора́льными спа́йками) — наиболее распространённый эпилептический синдром в детском возрасте[1]. Большинство детей перерастают этот синдром (он проявляется в возрасте от 3 до 13 лет, достигает пика в 8—9 лет и проходит в возрасте от 14 до 18 лет), отсюда и название «доброкачественная»[2].
Общие сведения
История
Этиология
Доброкачественная роландическая эпилепсия классифицируется как генетическое заболевание, поскольку примерно у 25% пациентов в семейном анамнезе есть либо фебрильные судороги, либо эпилепсия. Считается, что заболевание передаётся по аутосомно-доминантному типу. Однако все исследования подтверждают роль генетики. Хотя конкретный ген не выявлен, считается, что в этом участвуют 11-я хромосома (11p13) и 15-я хромосома (15q14). В семьях с БРЭ были обнаружены мутации в генах KCNQ2, ELP4, и GRIN2A[4].
Патогенез
Остается предметом активного изучения, однако ключевым механизмом считается возраст-зависимая корковая гипервозбудимость роландической области коры головного мозга, обусловленная генетическими факторами. Основным патофизиологическим субстратом является нарушение баланса между возбуждающими (глутаматергическими) и тормозными (ГАМК-ергическими) процессами в зоне центрально-височных отделов коры в критический период созревания мозга. Специфические эпилептиформные разряды, регистрируемые на ЭЭГ в виде центротемпоральных спайков, возникают вследствие повышенной нейрональной синхронизации в области нижней части прецентральной и постцентральной извилин, что клинически может проявляться фокальными приступами с симптомами в области лица и ротоглотки[5].
Важную роль в патогенезе играет генетическая предрасположенность — у 60% пациентов выявляется семейный анамнез эпилепсии, при этом тип наследования соответствует аутосомно-доминантному с возраст-зависимой пенетрантностью. Идентифицированы несколько генов, ассоциированных с ДРЭД, включая гены, кодирующие субъединицы никотиновых ацетилхолиновых рецепторов (CHRNA4, CHRNB2), а также гены, связанные с ионными каналами и синаптической передачей. Характерная возраст-зависимость синдрома (манифестация в 3-13 лет с последующей спонтанной ремиссией к пубертатному периоду) объясняется процессами естественного созревания мозга, в ходе которого происходит постепенное усиление тормозных ГАМК-ергических влияний и reduction избыточной возбудимости нейронов роландической области[5].
Эпидемиология
Доброкачественная роландическая эпилепсия может начаться в возрасте от 1 до 14 лет, при этом пик заболеваемости наблюдается между 7 и 10 годами. Данное заболевание чаще встречается у мальчиков, чем у девочек, с соотношением примерно 1,5 к 1. Заболеваемость составляет от 10 до 20 случаев на 100 000 детей в возрасте до 15 лет. Этот эпилептический синдром составляет около 15% всех случаев эпилепсии у детей и является наиболее распространённым эпилептическим синдромом в детском возрасте. У взрослых это заболевание не встречается[4].
Диагностика
Приступы отличаются редкой частотой возникновения и носят парциальный характер, поскольку их источник локализуется в роландической области головного мозга. Особенностью этих приступов является сохранность сознания во время пароксизма. Клинические проявления преимущественно односторонние и включают мышечные подергивания и напряжение лицевой мускулатуры, сопровождающиеся чувством онемения и парестезиями в области лица и ротоглотки. Эти симптомы вызывают речевые нарушения в виде характерных булькающих звуков, прерывания речи, а также повышенное слюноотделение. Продолжительность приступов обычно не превышает 2-3 минут. В некоторых случаях двигательные проявления могут распространяться на конечности той же стороны тела. При прогрессировании приступа возможно развитие вторично-генерализованных судорог с двусторонним вовлечением мышц, что может сопровождаться генерализованным тремором, тоническим напряжением мускулатуры, нарушениями функции тазовых органов, потерей сознания и последующим постиктальным состоянием. В связи с преимущественно ночным возникновением и фокальным характером приступов, они часто остаются незамеченными до момента развития генерализованного судорожного припадка. Осложнения в виде эпилептического статуса или внезапной смерти крайне редки. Течение заболевания может сопровождаться цефалгиями, мигренозными эпизодами, а также нарушениями поведения и обучения, особенно у пациентов с продолжающимися приступами и изменениями на электроэнцефалограмме[5].
Основным методом инструментальной диагностики роландической эпилепсии является электроэнцефалография (ЭЭГ), которая позволяет выявить характерные изменения в межприступный период. Патогномоничным ЭЭГ-маркером считаются центротемпоральные спайки (роландические спайки) — высокоамплитудные острые волны или комплексы спайк-медленная волна, локализующиеся в центральных и височных отведениях (C5, C6, T3, T4 по системе 10-20). Важной диагностической особенностью является активация эпилептиформной активности во время медленного сна (NREM-фаза), когда количество спайков значительно увеличивается. При типичной клинической картине этих изменений достаточно для подтверждения диагноза[5].
Магнитно-резонансная томография (МРТ) головного мозга не показывает структурных аномалий при идиопатической роландической эпилепсии и назначается primarily при атипичном течении для исключения симптоматических форм эпилепсии (корковая дисплазия, опухоли, последствия перинатального поражения ЦНС). Длительный видео-ЭЭГ мониторинг рекомендуется в сомнительных случаях для регистрации приступов и уточнения формы эпилепсии[5].
Дифференциальная диагностика
Дифференциальную диагностику данного заболевания проводят со рядом синдромов:
- Синдром псевдо-Леннокса (атипичная роландическая эпилепсия): характеризуется наличием как фокальных (роландических), так и атипичных абсансов, негативного миоклонуса, а также частыми ночными генерализованными тонико-клоническими приступами. В отличие от классической РЭ, на ЭЭГ регистрируются не только роландические спайки, но и продолженная пик-волновая активность в медленноволновом сне, а также возможны когнитивные нарушения.
- Синдром Панайотопулоса (доброкачественная затылочная эпилепсия с ранним дебютом): основное отличие — семиология приступов. Для синдрома Панайотопулоса характерны длительные приступы с вегетативной симптоматикой (тошнота, рвота, бледность), девиация глаз, нарушение сознания, в то время как для РЭ типичны короткие гемифациальные моторные приступы с гиперсаливацией и остановкой речи.
- Симптоматические эпилепсии, обусловленные структурными поражениями головного мозга (например, опухоли, корковые дисплазии в роландической области). Их исключает наличие нормального психомоторного развития ребёнка и отсутствие неврологического дефицита в неонатальный период. Решающее значение для дифференциации имеет МРТ головного мозга.
- Синдром Ландау — Клеффнера (приобретённая эпилептическая афазия): главное отличие — наличие у ребёнка прогрессирующего нарушения речевой функции (афазия), которое является ведущим симптомом, а не редкие эпилептические приступы. На ЭЭГ выявляется продолженная пик-волновая активность в битемпоральных отделах, преимущественно во сне.
- Доброкачественная эпилепсия детского возраста с затылочными пароксизмами (синдром Гасто): дифференциация основывается на локализации пароксизмальной активности на ЭЭГ (затылочные спайки) и клинической картине приступов, включающей зрительные нарушения (амблиопия, зрительные галлюцинации), мигренеподобную головную боль.
- Неврологические заболевания, протекающие с лицевым гемиспазмом, пароксизмальными дискинезиями. Отличие — отсутствие характерного эпилептиформного паттерна на ЭЭГ[6].
Лечение
Роландическая эпилепсия в большинстве случаев не требует противосудорожной терапии. Это связано с ее доброкачественным течением. Немедикаментозная терапия включает в себя соблюдение режима сна и бодрствования и режима питания. В случае необходимости медикаментозной терапии, препаратами выбора являются леветирацетам, сультиам и вальпроевая кислота[5].
Прогноз
Прогноз при доброкачественной роландической эпилепсии остается благоприятным независимо от проведения лечебных мероприятий. Для заболевания характерно самопроизвольное прекращение приступов к возрасту 15-16 лет у абсолютного большинства пациентов. Активный период заболевания обычно длится от двух до четырех лет. Большинство пациентов испытывают менее десяти эпизодов за весь период болезни, при этом у значительной части детей наблюдается всего один приступ. Отмечено, что при раннем дебюте заболевания может отмечаться большее количество приступов и более продолжительный период судорожной активности. Следует учитывать, что раннее начало приступов в некоторых случаях сопровождается обратимыми когнитивными, поведенческими и речевыми нарушениями, которые полностью исчезают к подростковому возрасту одновременно с прекращением эпилептических проявлений. В отдельных ситуациях ранний дебют может указывать на другие формы эпилептических синдромов, что требует проведения дополнительных диагностических мероприятий[5].
Диспансерное наблюдение
Диспансерное наблюдение при роландической эпилепсии осуществляется детским неврологом или эпилептологом и направлено на контроль течения заболевания, оценку эффективности терапии и обеспечение нормального развития ребёнка. Осмотры проводятся регулярно с частотой раз в 3—6 месяцев, а при стойкой ремиссии — раз в год. ЭЭГ-мониторинг выполняется для подтверждения диагноза и оценки динамики эпилептиформной активности, обычно раз в 6—12 месяцев, при этом частая повторная ЭЭГ не рекомендуется, так как активность может сохраняться после прекращения приступов. Нейропсихологическое тестирование проводится при наличии жалоб на трудности в обучении, речь или память, как правило, раз в 1—2 года. МРТ головного мозга не является рутинным методом наблюдения и назначается однократно при первичной диагностике для исключения симптоматических форм эпилепсии. Наблюдение продолжается до возраста 16—18 лет, когда наступает спонтанная ремиссия заболевания. Критерием для прекращения терапии и снятия с учёта является отсутствие приступов в течение 2 и более лет на фоне значительного улучшения или нормализации ЭЭГ. Отмена противоэпилептических препаратов проводится врачом постепенно. Важной частью наблюдения является образовательная работа с родителями: разъяснение доброкачественной природы заболевания, благоприятного прогноза, а также правил оказания помощи при приступе и минимизации провоцирующих факторов, таких как недосыпание и стресс[5][7].
Профилактика
Специфической профилактики для предотвращения возникновения роландической эпилепсии не существует, так как это заболевание относится к идиопатическим формам и связано с генетической предрасположенностью.
Примечания
Литература
- Клинические рекомендации. Эпилепсия и эпилептический статус у взрослых и детей.
- Amrutkar C. V., Riel-Romero R. M.Rolandic Epilepsy Seizure(англ.).StatPearls. StatPearls Publishing (январь 2025). Дата обращения: 5 октября 2025.