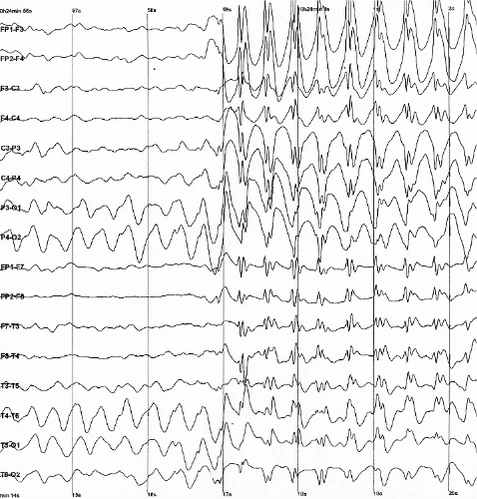
Посттравматическая эпилепсия
Посттравмати́ческая эпиле́псия (ПТЭ) — хроническое неврологическое заболевание, относящееся к вторичным формам эпилепсии. Проявляется повторными спонтанными эпилептическими припадками, которые возникают после перенесённой черепно-мозговой травмы. Развитие ПТЭ обусловлено формированием стойкого эпилептогенного очага в зоне повреждения мозговой ткани в результате таких процессов, как глиоз, нарушение нейронных связей и нейровоспаление. Прогноз при ПТЭ вариабелен и зависит от тяжести исходной травмы, типа приступов и эффективности терапии. В целом течение ПТЭ часто характеризуется склонностью к фармакорезистентности, особенно при тяжёлых повреждениях и очаговых приступах, однако при адекватном подборе антиэпилептической терапии у значительной части пациентов достигается стойкая ремиссия, хотя во многих случаях лечение является пожизненным[1].
История
Связь между травмой головы и возникновением судорожных приступов была отмечена ещё в трудах Гиппократа. Более детальное клиническое наблюдение принадлежит врачу XVI века Деретусу, который описал развитие эпилепсии у молодого мужчины, перенёсшего перелом черепа. В последующие столетия эта тема стала предметом многочисленных научных изысканий. Современное понимание причинно-следственных отношений между черепно-мозговой травмой и эпилепсией в значительной степени сформировалось благодаря масштабному анализу и длительному наблюдению за пациентами, получившими повреждения мозга в период войн XX века[2].
Этиология
ПТЭ по своей этиологии является прямым следствием структурного повреждения головного мозга. К развитию заболевания предрасполагает комплекс факторов, связанных как с индивидуальными особенностями пациента, так и с характером самой травмы[1]:
- факторы, связанные с индивидуальными особенностями пациента: возраст младше 5 или старше 65 лет, хронический алкоголизм, а также наличие аллели аполипопротеина Е4, хотя роль последнего генетического маркера остаётся дискуссионной и подтверждается не всеми исследованиями;
- факторы, связанные с характером травмы: вероятность развития ПТЭ существенно возрастает при тяжёлой степени черепно-мозговой травмы, проникающих ранениях головы, наличии внутричерепной гематомы, линейного или вдавленного перелома костей черепа, геморрагического ушиба мозга, а также если кома после травмы длится более 24 часов. Ключевым предиктором считается возникновение ранних посттравматических судорог в первую неделю после повреждения. Кроме того, риск является кумулятивным при повторных черепно-мозговых травмах в анамнезе.
Патогенез
Патогенез ПТЭ является многофакторным и сложным, охватывающим широкий спектр взаимосвязанных патофизиологических процессов, инициированных механическим повреждением головного мозга. Считается, что тип травмы определяет ведущие механизмы: проникающие ранения, ведущие к рубцеванию, чаще ассоциированы с ранними приступами, в то время как закрытая травма вызывает диффузное аксональное повреждение, ишемию и вторичные изменения[3].
Центральную роль в эпилептогенезе отводят нарушению целостности и функции гематоэнцефалического барьера (ГЭБ). Его повреждение служит фундаментальным катализатором, запускающим каскад событий: изменение сосудистых реакций и метаболизма, развитие нейровоспаления и эксайтотоксичности за счёт накопления возбуждающих аминокислот, таких как глутамат. Образуется порочный круг, где ишемия и метаболический дисбаланс усугубляют повреждение ГЭБ[3].
Ключевое значение имеет развивающаяся дисфункция астроцитов. В норме эти клетки регулируют ионный гомеостаз, в частности, транспорт ионов калия и захват глутамата из синаптической щели. Их повреждение приводит к стойкой деполяризации нейронов, снижению порога возбудимости и нарушению обратного захвата возбуждающих медиаторов. Особое внимание уделяется астроцитарным калиевым каналам внутреннего выпрямления, в частности Kir4.1, кодируемому геном KCNJ10. Генетические вариации, влияющие на функцию этих каналов, рассматриваются как фактор, повышающий индивидуальную предрасположенность к развитию ПТЭ[3].
Повреждение ГЭБ также вызывает ионный дисбаланс во внеклеточном пространстве, приводящий к отёку, и повышению концентрации альбумина в мозговой паренхиме, что само по себе является эпилептогенным фактором. Параллельно активируются мощные нейровоспалительные процессы. Активированные микроглия и астроциты высвобождают провоспалительные цитокины, например интерлейкин-1β, которые, воздействуя на нейрональные рецепторы, способствуют притоку кальция и повышают возбудимость нейронов, способствуя формированию эпилептического очага[3].
Таким образом, патогенез ПТЭ представляет собой сложную сеть взаимодействий, включающую структурное повреждение, нарушение функции ГЭБ, астроцитарную дисфункцию, ионный и нейротрансмиттерный дисбаланс, а также хроническое нейровоспаление[3][4].
Эпидемиология
Эпидемиология ПТЭ характеризуется значительной вариабельностью в зависимости от популяции и тяжести травмы. Распространенность ПТЭ среди всех типов черепно-мозговых травм составляет 2—2,5 % среди гражданского населения. Этот показатель выше в военных условиях из-за травм, наносимых высокоскоростными снарядами. Среди госпитализированных нейрохирургических пациентов распространённость возрастает до 5 %. Если рассматривать только тяжёлые травмы головы, частота ПТЭ составляет 10—15 % для взрослых и 30—35 % для детей[1].
Диагностика
Клиническая картина ПТЭ характеризуется значительным полиморфизмом приступов, которые могут встречаться в любом сочетании. Наиболее типичными являются парциальные (фокальные) приступы, которые могут протекать как без нарушения сознания (простой парциальный приступ), так и с его нарушением (сложный парциальный приступ). Также характерно развитие симптоматических вторично-генерализованных судорожных приступов[4].
Наиболее частой локализацией очага для развития поздних посттравматических приступов являются височные доли. Приступы височного происхождения в примерно двух третях случаев сопровождаются аурой. Ауры могут быть вегетативными (дискомфорт или боли в животе, тошнота), психическими (внезапный страх, тревога, дежавю или жамевю), а также обонятельными или вкусовыми галлюцинациями (обычно неприятного характера). По мере развития приступа сознание может нарушаться: пациент замирает, становится неотзывчивым, у него могут наблюдаться стереотипные движения (жевание, чмокание губами, хрюканье) и автоматизмы (потирание рук, перебирание одежды). Вторичная генерализация для приступов височного происхождения относительно редка[4].
Вторая по частоте локализация — лобные доли. Для лобной эпилепсии ауры нетипичны. Во время приступа часто наблюдаются гиперкинетические моторные феномены: движения, напоминающие езду на велосипеде, толкающие движения тазом, хаотичные размашистые движения, асимметричное тоническое напряжение конечностей. Для приступов лобного происхождения вторичная генерализация в тонико-клонический приступ является частым явлением[4].
Приступы, исходящие из других долей, встречаются реже. Для затылочной эпилепсии характерны элементарные зрительные галлюцинации (вспышки света, зигзагообразные линии, калейдоскопические фигуры). Если очаг расположен в передних отделах затылочной доли или на стыке с височной, галлюцинации могут быть сложными, предметными. Для теменной эпилепсии типичной аурой является головокружение. Если очаг находится рядом с постцентральной извилиной, возникают элементарные сенсорные симптомы (парестезии), которые могут быть болезненными[4].
Любой фокальный приступ может перейти во вторично-генерализованный тонико-клонический приступ. Он характеризуется тонической фазой (вытягивание рук и ног), сменяющейся клонической фазой с ритмичными подёргиваниями. Часто сопровождается кратковременной остановкой дыхания, рвотой, прикусыванием языка и недержанием мочи. После сложных парциальных и генерализованных приступов наступает постиктальный период, для которого характерны оглушение, сонливость, спутанность сознания и последующая амнезия на события до приступа. Этот период может длиться от нескольких минут до нескольких часов. Пациенты часто жалуются на головную боль, головокружение и сонливость, особенно после генерализованного тонико-клонического приступа[4].
Компьютерная и магнитно-резонансная томография головного мозга используются для визуализации структурных повреждений головного мозга[1].
Дифференциальная диагностика
Дифференциальная диагностика ПТЭ проводится со следующими состояниями[1]:
- доброкачественная эпилепсия детского возраста;
- фокальные приступы с нарушением сознания;
- спутанность сознания и острые расстройства памяти;
- головокружение, вертиго и нарушение равновесия;
- лобная эпилепсия;
- генерализованные тонико-клонические приступы;
- травма головы;
- неонатальные судороги;
- психогенные неэпилептические приступы;
- височная эпилепсия.
Осложнения
Если ПТЭ протекает в тяжёлой форме с частыми вторично-генерализованными приступами, то возникает риск внезапной смерти[1].
Лечение
Основным методом лечения эпилепсии является длительная медикаментозная терапия противоэпилептическими препаратами, направленная на достижение стойкой ремиссии приступов с минимальными побочными эффектами. Лечение начинают с монотерапии, индивидуально подбирая препарат в зависимости от формы эпилепсии (фокальной или генерализованной), типа приступов, возраста и сопутствующих заболеваний пациента. Дозу постепенно увеличивают до достижения терапевтического эффекта. При недостаточной эффективности первого препарата рассматривают переход на альтернативную монотерапию или рациональную политерапию с комбинацией противоэпилептических препаратов, имеющих разные механизмы действия[5].
При развитии фармакорезистентной эпилепсии (когда приступы сохраняются на фоне адекватной терапии двумя препаратами) применяются альтернативные подходы. К ним относятся нейрохирургическое лечение (резекция эпилептогенного очага, каллозотомия, гемисферэктомия и другие), стимуляция блуждающего нерва, глубокая стимуляция мозга, а также нефармакологические методы, такие как кетогенная диета. Для купирования эпилептического статуса используют протоколы неотложной помощи с последовательным введением бензодиазепинов, парентеральных противоэпилептических препаратов и, при необходимости, препаратов для общей анестезии[5].
Прогноз
Крупные исследования демонстрируют, что наличие ПТЭ примерно вдвое увеличивает риск смерти по сравнению с пациентами, перенёсшими черепно-мозговую травму без развития эпилепсии. Наиболее высокий риск смерти, связанный с ПТЭ, отмечается у пациентов в возрасте 18–39 лет. Причинами смерти в этой группе часто выступают непосредственно эпилептические состояния, несчастные случаи, связанные с приступом, а также суицид. У пациентов старше 60 лет существенный вклад в смертность вносят сердечно-сосудистые заболевания, на течение которых может влиять терапия ПТЭ[6]
Диспансерное наблюдение
Пациентам с ПТЭ необходимо регулярное динамическое наблюдение у невролога. Основными задачами такого наблюдения являются: оценка частоты и характера приступов, контроль эффективности и переносимости противоэпилептической терапии, мониторинг неврологического статуса, а также проведение нейропсихологического обследования для выявления и коррекции возможных когнитивных и поведенческих нарушений[1].
Профилактика
Первичная профилактика начинается с минимизации риска травмы головы. Рекомендуется использование защитных средств, таких как детские автокресла и шлемы при езде на велосипеде, а также соблюдение правил безопасности в спорте для предотвращения повторных травм[1].
Вторичная профилактика: применение противоэпилептических препаратов в раннем периоде после тяжёлой черепно-мозговой травмы эффективно для снижения риска ранних посттравматических приступов. Например, фенитоин доказанно уменьшает вероятность ранних судорог. Однако нет убедительных доказательств того, что такая профилактическая терапия снижает риск развития поздних приступов, начинающихся после 7-го дня с момента травмы[1].
Примечания
Литература
- Котов А.С., Белова Ю.А. Посттравматическая эпилепсия: теория и практика // Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. — 2010. — Т. 110, № 3—2. — С. 48—51.
- Литвинова А. А., Ковалёв П. С., Маслов Н. Е. и др. Посттравматическая эпилепсия: клинические, диагностические и терапевтические особенности // Эпилепсия и пароксизмальные состояния. — 2021. — Т. 13, № 4. — С. 377—392. — doi:10.17749/2077-8333/epi.par.con.2021.100.
- Karlander M., Ljungqvist J., Sörbo A., Zelano J. Risk and cause of death in post-traumatic epilepsy: a register-based retrospective cohort study (англ.) // Journal of Neurology. — 2022. — Vol. 269, no. 11. — P. 6014—6020. — doi:10.1007/s00415-022-11279-5.