Болезнь Лафора
Боле́знь Лафо́ра (прогресси́рующая миоклони́ческая эпиле́псия 2-го ти́па) — тяжёлое прогрессирующее аутосомно-рецессивное заболевание, форма миоклонической эпилепсии, которая развивается у здоровых подростков. Для неё характерны миоклонус, затылочные приступы и быстро нарастающая деменция. Болезнь неуклонно прогрессирует и заканчивается летальным исходом в среднем в течение 10 лет с момента дебюта[1].
Что важно знать
История
В 1891 году российский невропатолог Александр Генрихович Ландузи (Landouzy) описал случай миоклонической эпилепсии у подростка, что стало одной из первых публикаций на эту тему. Однако решающий прорыв в идентификации болезни как самостоятельной нозологической единицы произошёл двумя десятилетиями позже. В 1911 году выдающийся испанский невропатолог Гонсало Родригес Лафора (исп. Gonzalo Rodríguez Lafora), работая в лаборатории США со своим коллегой Б. Глюком (B. Glueck), провёл гистологическое исследование мозга умершей молодой пациентки, страдавшей от прогрессирующей миоклонической эпилепсии. Именно Лафора обнаружил в нейронах, особенно в отделах мозга, таких как таламус и чёрная субстанция, уникальные патологические включения — шарообразные, базофильные образования, которые он ошибочно принял за амилоидные тельца и которые позже будут названы в его честь тельцами Лафора. Это открытие позволило чётко дифференцировать данное заболевание от других форм миоклонической эпилепсии, например, от болезни Унферрихта, описанной ранее немецким врачом Генрихом Унферрихтом (нем. Heinrich Unverricht) в 1903 году. Ключевая заслуга Гонсало Лафоры заключается не только в обнаружении диагностического маркера, но и в установлении аутосомно-рецессивного типа наследования этого фатального расстройства[2].
Следующий важный этап в истории изучения болезни наступил, когда в 1955 году с помощью гистохимического анализа было установлено, что основным компонентом телец Лафора является не амилоид, а нерастворимый сложный углевод — полиглюкосан, напоминающий гликоген с аномальным разветвлением[2].
Молекулярно-генетическая эра в исследовании болезни Лафора началась в 1990-х годах. В 1995 году интернациональной группе исследователей удалось картировать первый локус гена (EPM2A) на хромосоме 6q24, а в 1998 году был идентифицирован и сам ген, кодирующий белок лафорин. Вскоре после этого, в 2003 году, был открыт второй ген (NHLRC1, или EPM2B), кодирующий белок малин. Мутации в этих генах, играющих ключевую роль в регуляции метаболизма гликогена, и являются причиной развития этой тяжёлой болезни[2].
Этиология
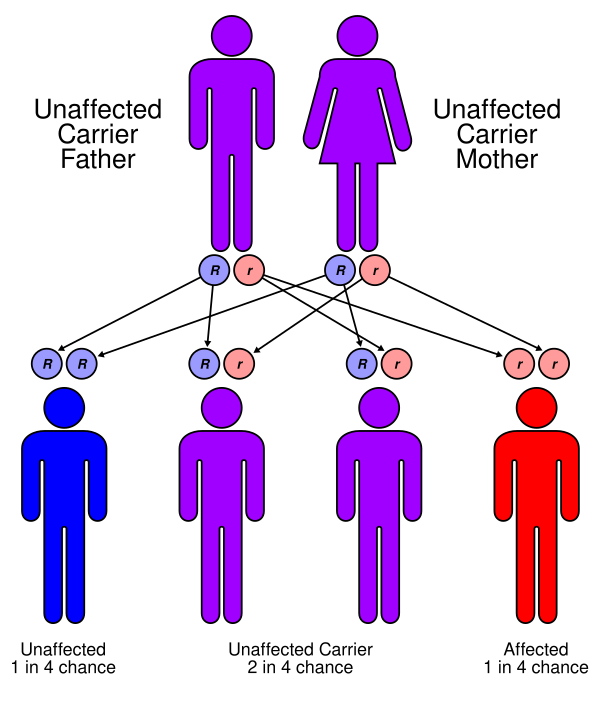
Болезнь Лафора представляет собой наследственное нейродегенеративное заболевание, которое передаётся по аутосомно-рецессивному типу. Это означает, что у носителей одной копии мутировавшего гена (гетерозигот) болезнь не развивается и протекает бессимптомно. Известно, что развитие заболевания связано с мутациями в двух основных генах: EPM2A, расположенном на хромосоме 6q24.3, и EPM2B (также известном как NHLRC1), находящемся на хромосоме 6p22.3. Ген EPM2A кодирует белок лафорин, а ген EPM2B — малин. Оба гена являются основными причинами болезни Лафора, однако их относительный вклад варьирует в разных популяциях. Большинство выявленных мутаций приводят к потере функции белков и включают в себя мутации в сайтах сплайсинга, миссенс-мутации, нонсенс-мутации, небольшие делеции и инсерции. Согласно современным представлениям, лафорин и малин функционируют как единый белковый комплекс. Предполагается, что лафорин направляет малин к молекулам гликогена с аномально длинными цепями глюкозы, чтобы предотвратить их дальнейший рост. Нарушение функций любого из этих белков приводит к тому, что такие длинные цепи гликогена теряют способность удерживать воду, формируют двойные спирали и выпадают в осадок, постепенно накапливаясь в виде характерных для болезни Лафора патологических включений — телец Лафора[1].
Клинические исследования показывают, что определённые мутации в гене EPM2A могут ассоциироваться с более поздним началом заболевания и замедленным прогрессированием. Например, мутации F321C и G279C вызывают менее выраженные функциональные дефекты белков и связаны с более мягким течением болезни. Это позволяет использовать генетическую информацию для прогнозирования течения заболевания и в перспективе — для разработки персонализированных терапевтических подходов. В отдельных случаях медленно прогрессирующей болезни Лафора была обнаружена мутация N163D в гене EPM2A, которая значительно нарушает взаимодействие лафорина с его белковыми партнёрами. Это указывает на то, что мягкое течение заболевания может быть обусловлено либо особыми биохимическими свойствами мутантного белка, либо влиянием других генетических факторов. Поскольку болезнь Лафора вызвана дефектами в ферментах, критически важных для метаболизма гликогена, у пациентов во всех тканях организма образуются аномальные нерастворимые включения гликогена, по своей структуре напоминающие растительный крахмал, а не человеческий гликоген. Ген PRDM8 также иногда ассоциирован с этим заболеванием. Он кодирует белок, ответственный за перенос лафорина и малина в ядро клетки. Мутации в этом гене приводят к дефициту лафорина и малина в цитоплазме и связаны с ранним началом болезни Лафора[1].
Патогенез
Синтез гликогена критически важен для утилизации избытка глюкозы, обеспечивая организм энергией при физических нагрузках и в другие ключевые периоды. Нарушения метаболизма гликогена, вызванные мутациями в ферментах, могут приводить к дисфункции печени, мышц, сердца, почек и головного мозга. При прогрессирующей болезни Лафора в различных тканях накапливаются включения, содержащие аномальный гликоген с повышенным фосфорилированием, удлинёнными цепями и нерегулярным ветвлением. Это накопление оказывает токсическое действие на нейроны и вызывает гибель клеток. Нарушение гликогенолиза в нервной системе также характерно для данного заболевания и может быть выявлено с помощью анализа ДНК или электронной микроскопии биоптатов печени и скелетных мышц[1].
У здоровых людей малин, убиквитинлигаза E3, взаимодействует с лафорином, протеинфосфатазой двойной специфичности, участвуя в защитном клеточном механизме, предотвращающем накопление полиглюкозидов. Мутации в генах EPM2A и EPM2B (NHLRC1), кодирующих эти белки, вызывают болезнь Лафора. Считается, что дефекты систем клеточного клиренса и аутофагии приводят к накоплению в цитоплазме частиц гликогена, известных как тельца Лафора. Эти недостаточно разветвлённые и длинноцепочечные формы гликогена формируют нерастворимые полиглюкозные тельца, что вызывает нейровоспаление, нейродегенерацию и эпилепсию[1].
Характерным морфологическим признаком болезни Лафора является наличие полиглюкозных телец в тканях головного мозга, миокарда, печени и эпителии потовых желез. Диагноз подтверждается генетическим анализом, например, выявлением гомозиготной мутации в гене EPM2A. Исследования показали, что тельца Лафора присутствуют также в астроцитах. Блокирование синтеза гликогена в астроцитах предотвращает накопление этих телец и снижает проявление нейродегенерации, нарушений аутофагии и метаболических изменений, что указывает на важную роль астроцитов в патогенезе заболевания, а не только нейронов[1].
Исследования демонстрируют, что при отсутствии функционального комплекса лафорин-малин снижается уровень фосфатидилинозитол-3P, вероятно, из-за нарушения регуляции аутофагического комплекса PI3KC3. Комплекс лафорин-малин физически взаимодействует и колокализуется с основными компонентами комплекса PI3KC3, такими как beclin1, vps34 и vps15, что приводит к их полиубиквитинированию. Также наблюдается полиубиквитинирование ATG14L и UVRAG. Сверхэкспрессия комплекса лафорин-малин повышает активность PI3KC3[1].
Исследования на фибробластах человека с использованием разобщителей митохондриального дыхания и ингибиторов дыхательной цепи выявили частичное нарушение деградации повреждённых митохондрий (митофагии) при болезни Лафора. Это связано с частичным дефектом аутофагического ответа, а не с нарушением канонических сигнальных путей митофагии[1].
В рамках тематического исследования для диагностики и подтверждения генетического спектра болезни Лафора в одной семье было проведено полноэкзомное секвенирование. Результаты выявили новую гетерозиготную мутацию в гене NHLRC1, что подтвердило полезность генетического анализа для диагностики данного заболевания как альтернативы биопсии тканей[1].
Эпидемиология
Болезнь Лафора встречается в любой популяции. Наиболее часто заболевание регистрируется в средиземноморских странах (Испания, Италия, Франция), странах Северной Африки, Ближнего Востока и некоторых регионах Южной Индии, где существует высокая степень кровнородственных браков. По данным литературы, общая частота различных форм прогрессирующих миоклонус-эпилепсий составляет около 1 % от всех форм эпилепсии и до 10 % от всех форм миоклонических эпилепсий[3].
Диагностика
Болезнь Лафора манифестирует в возрасте от 6 до 20 лет, при этом средний возраст начала составляет около 14 лет. Дебют заболевания обычно характеризуется генерализованными тонико-клоническими приступами, которые чаще всего возникают в первые часы после пробуждения. В течение последующих 8 месяцев — 1,5 лет к приступам присоединяется корковый эпилептический миоклонус, проявляющийся массивными хаотичными подёргиваниями в конечностях с последующим вовлечением аксиальной мускулатуры, преимущественно мышц-разгибателей. В развёрнутой стадии болезни у пациентов появляются атонические и атонически-астатические приступы, которые лишают больного возможности самостоятельно передвигаться. Атонические приступы особенно заметны при обследовании пациента в положении стоя с вытянутыми вперёд руками, когда наблюдаются хаотичные движения кистей по типу «хлопающего тремора», опускание рук (чаще асимметричное) с возможным выпадением предметов. Характерным проявлением являются фокальные приступы без утраты сознания со зрительными нарушениями, включающими простые и сложные галлюцинации, скотомы и преходящую корковую слепоту, которые могут появляться уже в начале болезни. В развёрнутой стадии заболевания развивается быстропрогрессирующая деменция, рефрактерный эпилептический статус, психоз, мозжечковая атаксия, дизартрия, мутизм и респираторная недостаточность, которые приводят к летальному исходу. Продолжительность жизни с момента начала заболевания обычно не превышает 10 лет. При неврологическом обследовании определяется мышечная дистония, интенционный тремор, нистагм, атаксия, нарушения письма, дизартрия. С начала заболевания появляются когнитивные нарушения в виде ухудшения памяти, проблем в обучении, снижение настроения. По мере прогрессирования процесса наступает деменция[3].
На начальных стадиях заболевания электроэнцефалография может регистрировать нормальную фоновую активность, которая замедляется по мере прогрессирования патологии. Основным ЭЭГ-паттерном являются короткие разряды генерализованной пик-полипик-волновой активности, наблюдаемые как в фоне, так и при ритмической фотостимуляции. Характерной особенностью электроэнцефалограммы при болезни Лафора служит региональная эпилептиформная активность в затылочных отведениях, проявляющаяся изолированными острыми волнами или пик-полипик-волновыми комплексами, которые возникают как при фоновой записи, так и при фотостимуляции[3].
При проведении нейровизуализации на ранних этапах заболевания магнитно-резонансная томография может не выявлять патологических изменений. В развёрнутой стадии болезни возможно обнаружение мозжечковой или корковой атрофии. МР-спектроскопия демонстрирует метаболические изменения в мозжечке, базальных ганглиях и лобной коре головного мозга[3].
Дифференциальная диагностика
На начальных стадиях клинические проявления болезни Лафора и идиопатической генерализованной эпилепсии, такой как ювенильная миоклоническая эпилепсия, идентичны. Поэтому при ранней диагностике идиопатических генерализованных эпилепсий возникновение лекарственной устойчивости и замедление основной активности на ЭЭГ должны вызывать подозрение на болезнь Лафора. Основной дифференциальный диагноз проводится с другими формами прогрессирующих миоклонус-эпилепсий: болезнью Унферрихта — Лундборга, нейрональным липофусцинозом, миоклонической эпилепсией с рваными красными волокнами (MERRF) и сиалидозом. Болезнь Лафора отличается от болезни Унферрихта-Лундборга более поздним дебютом и наличием фокальных приступов со зрительными нарушениями. К отличительным особенностям также относятся: отсутствие подкоркового неэпилептического миоклонуса, наличие атонических приступов, выраженные экстрапирамидные нарушения, развитие деменции, замедление основной активности фона на ЭЭГ, региональная эпилептиформная активность и быстрое прогрессирование заболевания с летальным исходом[3].
Лечение
Болезнь Лафора неизлечима. Лечение носит поддерживающий характер и направлено на купирование приступов и улучшение функционального состояния пациента. Учитывая разнообразие типов приступов (например, генерализованные тонико-клонические приступы), обычно назначают широкий спектр противоэпилептических препаратов, включая леветирацетам, вальпроат натрия, топирамат и бензодиазепины[1].
Вальпроат служит препаратом выбора для монотерапии, однако его не следует назначать пациентам с подозрением на митохондриальные нарушения из-за ингибирования цитохром-С-оксидазы. Клоназепам эффективен для лечения миоклонических припадков как дополнительная терапия. Фенобарбитал применяется для детей и взрослых, но требует осторожности при комбинации с вальпроатом. Пирацетам демонстрирует эффективность при миоклонусе с хорошей переносимостью. Леветирацетам, производное пирролидона, доказал эффективность. Бриварацетам обладает сходным механизмом действия, но в 10 раз высшим сродством к синаптическим везикулам. Перампанел продемонстрировал эффективность как в монотерапии, так и в комбинации с другими препаратами, обеспечивая снижение частоты приступов и улучшение неврологических функций. Топирамат показывает эффективность преимущественно как дополнительная терапия, хотя возможно снижение эффективности со временем. Зонисамид применяется для лечения рефрактерных форм эпилепсий, включая прогрессирующую миоклоническую эпилепсию. Ламотриджин может усугублять миоклонус, поэтому при прогрессирующих миоклонических эпилепсиях его следует избегать, как и других блокаторов натриевых каналов. Среди альтернативных методов лечения стимуляция блуждающего нерва показывает эффективность, в то время как кетогенная диета не доказала результативности при болезни Лафора. Метформин демонстрирует нейропротекторные свойства, причём раннее начало лечения ассоциируется с лучшими неврологическими исходами. Перспективными направлениями терапии являются разработка антительных конъюгатов для доставки ферментов и создание катионных липосом для генной терапии, демонстрирующих хорошую эффективность трансфекции и низкую цитотоксичность в доклинических исследованиях[1].
Прогноз
Прогноз при болезни Лафора является крайне неблагоприятным. Это заболевание характеризуется неуклонно прогрессирующим течением и относится к числу наиболее агрессивных форм прогрессирующих миоклонических эпилепсий. Основным аспектом прогноза является быстрое нарастание симптоматики. После манифестации заболевания, обычно в подростковом возрасте, происходит стремительное присоединение тяжёлых неврологических и когнитивных расстройств, включая деменцию, атаксию, дизартрию, а также потерю возможности самостоятельно передвигаться и обслуживать себя. Важным прогностическим фактором является резистентность к терапии. Эпилептические приступы, в особенности миоклонус и тонико-клонические припадки, практически не поддаются контролю с помощью стандартных и даже комбинированных схем противоэпилептической терапии[4].
Летальный исход является неизбежным следствием заболевания. Продолжительность жизни после появления первых симптомов в большинстве случаев не превышает 10 лет. Непосредственными причинами смерти становятся эпилептический статус, аспирационная пневмония или дыхательная недостаточность, развивающиеся на терминальной стадии заболевания. Современные исследования направлены на поиск патогенетической терапии, воздействующей на основную причину болезни — накопление патологического полиглюкозана. Перспективными считаются такие подходы, как фермент-заместительная терапия, использование ингибиторов синтеза гликогена (метформин) и генная терапия[4].
Диспансерное наблюдение
Диспансерное наблюдение при болезни Лафора представляет собой комплексный и пожизненный процесс, направленный на контроль симптомов, профилактику осложнений и обеспечение паллиативной поддержки. Основная цель заключается в максимальном улучшении качества жизни пациента и его семьи в условиях неизлечимого прогрессирующего заболевания. Наблюдение осуществляется у невролога или эпилептолога с частотой не менее одного раза в квартал или по мере необходимости при учащении приступов. Специалист проводит коррекцию противоэпилептической терапии, подбирая препараты, их дозировки и комбинации для борьбы с рефрактерными приступами, а также оценивает неврологический статус, отслеживая прогрессирование миоклонуса, атаксии и дизартрии. Важным компонентом является регулярный мониторинг когнитивных функций с привлечением нейропсихолога или психиатра для оценки степени деменции и психиатрических осложнений, таких как депрессия и психозы. Это необходимо для решения вопросов опекунства и социальной адаптации. Поддержка других органов и систем включает наблюдение у пульмонолога для профилактики и лечения аспирационных пневмоний, возникающих из-за дисфагии и попадания слюны в дыхательные пути. Гастроэнтеролог или диетолог решают проблемы нарушения глотания, подбирают питание и при необходимости рекомендуют установку назогастрального зонда или гастростомы для предотвращения истощения и аспирации. Физиотерапевт помогает поддерживать мобильность, предотвращать контрактуры суставов и подбирает ортопедические приспособления, такие как инвалидные коляски и корсеты. На поздних стадиях заболевания респираторный терапевт оценивает функцию дыхания и решает вопросы респираторной поддержки. Паллиативная помощь является неотъемлемой частью диспансерного наблюдения с момента постановки диагноза и направлена на облегчение страданий пациента и поддержку его семьи на всех этапах заболевания[5].
Профилактика
Поскольку болезнь Лафора является наследственным аутосомно-рецессивным заболеванием, вызванным мутациями в генах EPM2A или NHLRC1, профилактика заключается в медико-генетическом консультировании семей из группы риска и применении репродуктивных технологий[5].
- Генетическое консультирование и тестирование: семьям, в которых уже есть случаи болезни Лафора, или парам из этнических групп с повышенной частотой носительства (например, среди населения Средиземноморья или Южной Азии), рекомендуется пройти консультацию у генетика. Проводится тестирование на выявление мутаций у будущих родителей для определения риска рождения больного ребёнка.
- Пренатальная диагностика: в случае если оба родителя являются носителями патогенной мутации, существует 25 % риск рождения ребёнка с болезнью Лафора. Таким парам предлагается пренатальная диагностика (например, хорионбиопсия или амниоцентез) для анализа ДНК плода на наличие двух мутантных копий гена. Это позволяет принять информированное решение о продолжении беременности.
- Предимплантационная генетическая диагностика (ПГД): для пар, которые проходят процедуру экстракорпорального оплодотворения (ЭКО), доступна возможность проведения ПГД. Эмбрионы тестируются на наличие мутаций, и для имплантации отбираются только те, которые не унаследовали две патогенные копии гена[5].
Примечания
Литература
- Гамирова Р. Г., Шаймарданова Р. М. Болезнь Лафоры - трудный пациент в работе невролога // Российский вестник перинатологии и педиатрии. — 2018. — № 5.
- Ibrahim F., Murr N. Lafora Disease (англ.). StatPearls Publishing (29 февраля 2024). Дата обращения: 4 октября 2025.