Синдром Драве
Синдро́м Дра́ве (СД; тяжёлая миоклони́ческая эпиле́псия младе́нчества) — миоклоническая эпилепсия младенчества из группы эпилептических энцефалопатий. Заболевание манифестирует на первом году жизни, чаще всего в возрасте 5—6 месяцев, с фебрильных и афебрильных генерализованных и фокальных эпилептических приступов, а в типичных случаях обязательно включает миоклонические приступы. Для СД характерны резистентность к стандартной противоэпилептической терапии и отставание в психическом развитии, которое с течением времени трансформируется в комплекс сопутствующих патологий: выраженную задержку психомоторного развития, когнитивные нарушения, интеллектуальную недостаточность, расстройства аутистического спектра, дефицит внимания и двигательную дисфункцию. В основе патологии у подавляющего большинства пациентов (около 80 %) лежит мутация в гене SCN1A[1].
Что важно знать
История
СД был впервые описан в 1978 году Шарлоттой Драве как тяжёлая миоклоническая эпилепсия младенчества, а в 1989 году закрепился как синдром Драве. Генетическая основа СД была открыта в 2001 году[2].
Классификация
СД относится к группе эпилептических энцефалопатий[3].
Этиология
СД является генетически обусловленным заболеванием. В подавляющем большинстве случаев он вызван de novo мутацией в гене SCN1A, локализованном на хромосоме 2q24.3. Ген SCN1A кодирует α1-субъединицу потенциал-зависимого натриевого канала нейронов (ПЗНКН). Мутация приводит к нарушению функции этих каналов, что вызывает дисбаланс возбуждающей и тормозной передачи сигналов в головном мозге, преимущественно затрагивая ГАМК-ергические интернейроны. В редких случаях патогенный вариант в гене SCN1A может быть унаследован по аутосомно-доминантному типу от родителя, который может иметь стёртые клинические проявления, такие как фебрильные судороги без сопутствующей когнитивной патологии. Также описан механизм соматического мозаицизма, при котором патогенный вариант присутствует только в части клеток организма — носители такого мозаицизма могут иметь лёгкие симптомы или быть фенотипически здоровыми, но способны передавать мутацию потомству, что приводит к развитию СД у ребёнка. Хотя мутации в SCN1A являются основной причиной синдрома (около 80—90 % случаев), к возможным мутациям, вызывающим развитие СД, также относятся мутации в генах GABRG2, GABRA1, SCN1B, SCN2A, STXBP1 и PCDH19[4][5].
Патогенез
Патогенез СД связан с дисфункцией потенциал-зависимого натриевого канала нейронов. Функциональная значимость ПЗНКН заключается в его ключевой роли для генерации потенциалов действия в быстроразряжающихся ГАМК-ергических интернейронах, в частности, в интернейронах, экспрессирующих парвальбумин (PV+). Мутации в SCN1A (описано свыше 2500 вариантов), составляющие причину около 80 % случаев СД, преимущественно приводят к потере функции канала. Следствием этого является снижение натриевых токов и нарушение способности тормозных интернейронов эффективно высвобождать ГАМК. Возникающий дисбаланс между возбуждающей и тормозной нейротрансмиссиями в нейронных сетях коры головного мозга, гиппокампа и мозжечка лежит в основе патологической гипервозбудимости и повышенной судорожной готовности. Этот механизм получил название «натрий-канальная интернейронопатия». Приступы при СД часто провоцируются внешними факторами, такими как лихорадка или сенсорная стимуляция, что объясняется дополнительной нагрузкой на и без того ослабленную тормозную систему[6].
Генотип-фенотипические корреляции указывают на то, что тяжесть клинической картины СД часто коррелирует со степенью функционального дефекта канала. Транслирующие мутации, ведущие к синтезу укороченного неработоспособного белка, обычно ассоциированы с более тяжёлым фенотипом по сравнению с некоторыми миссенс-мутациями, встречающимися при более лёгких формах. Описаны редкие случаи мутаций с приобретением функции, приводящих к инактивационным дефектам и стойкому натриевому току, что также вызывает гипервозбудимость, но через иной молекулярный механизм. Кроме того, на экспрессию и функцию канала влияют дополнительные генетические факторы (гены-модификаторы, такие как SCN9A), соматический мозаицизм и возраст-зависимая экспрессия ПЗНКН, что объясняет вариабельность начала заболевания, тяжести симптомов и ответа на терапию. Дисфункция специфических популяций интернейронов является причиной не только эпилептических приступов, но и сопутствующих СД коморбидных состояний: интеллектуальных нарушений, расстройств аутистического спектра и дефицита моторных функций. Таким образом, патогенез СД представляет собой сложный каскад событий, инициированный дисфункцией ПЗНКН в тормозных интернейронах, что приводит к системному нарушению баланса возбуждения и торможения в головном мозге[6].
Эпидемиология
Данные свидетельствуют о том, что глобальная распространённость СД составляет примерно 6,5 случая на 100 000 живорождений. Однако эти показатели могут существенно варьироваться в зависимости от этнической принадлежности и географического региона. Например, популяционное исследование в США показало, что распространённость СД составляет 1 случай на 15 700 живорождений. В Дании распространённость оценивается в 1 случай на 22 000 живорождений. В Германии 10-летняя распространённость СД была оценена в 4,7 случая на 100 000 населения. Во Франции оценочная распространённость составляет 1 случай на 20 000—30 000 человек, а в Швеции — 1 случай на 45 700 детей в возрасте до 18 лет. В Великобритании заболеваемость СД с подтверждённой мутацией SCN1A составляет не менее 1 случая на 40 900 рождений, а в Шотландии — 1 случай на 15 500 живорождений. Несмотря на редкость, на СД приходится приблизительно 2—5 % всех случаев эпилепсии у детей. Мальчики и девочки страдают этим заболеванием с равной частотой[6].
Распространённость СД на территории Российской Федерации не определена. Имеются единичные публикации с описанием клинических наблюдений[1][7].
Диагностика
Заболевание манифестирует, как правило, на первом году жизни, с пиком дебюта в возрасте 5—6 месяцев. Начало болезни иногда совпадает с периодом острой респираторной вирусной инфекции или следует за вакцинацией. В течении СД традиционно выделяют три последовательные стадии[1]:
- первая стадия (дебют, до 1 года) характеризуется преимущественно фебрильными клоническими приступами;
- вторая стадия («катастрофическая», 1—4 года) является наиболее тяжёлой. В этот период учащаются как фебрильные, так и афебрильные приступы разнообразной семиологии. К ним относятся фокальные моторные, миоклонические, тонико-клонические приступы, атипичные абсансы и альтернирующие гемиклонии. Ключевым элементом клинической картины становится эпилептический миоклонус (активный и негативный). Для всех типов приступов характерна тенденция к затяжному, статусному течению (длительностью 30 минут и более). Параллельно с учащением пароксизмов наблюдаются выраженная задержка и последующий регресс ранее приобретённых психоречевых навыков, тогда как моторное развитие в этот период значимо не страдает;
- третья стадия (стабилизация, после 4—5 лет) наступает по мере взросления пациента. Частота эпилептических приступов постепенно снижается, однако на первый план выходят стойкие и грубые неврологические дефициты, включая тяжёлые когнитивные нарушения и интеллектуальную недостатчность.
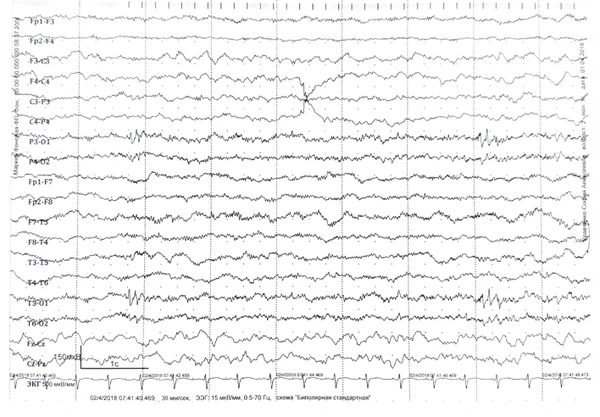
При проведении электроэнцефалографии (ЭЭГ) у пациентов с СД выявляется ряд характерных изменений: регистрируется замедление основной фоновой активности с доминированием тета-ритма частотой 4—5 Гц. В межприступном периоде у 70 % пациентов отмечается патологическая эпилептиформная активность, которая может носить как диффузный, так и региональный (фокальный) характер. Примерно у половины больных наблюдается фотосенситивность — способность световых стимулов провоцировать эпилептиформные разряды на ЭЭГ и иногда сами приступы, в редких случаях возможна аутоиндукция пароксизмов ярким светом. Провоцирующим фактором для эпилептиформной активности также может служить закрывание глаз. Характерной особенностью является усиление данной патологической активности во время сна[1].
Магнитно-резонансная томография головного мозга: при нейровизуализации у большинства пациентов с СД не выявляется грубых аномалий, и первоначальная картина в раннем детстве часто оценивается как нормальная. Однако с течением заболевания и возрастом у части пациентов могут развиваться неспецифические, но характерные изменения. К ним относятся диффузное глобальное снижение объёмов как серого, так и белого вещества головного мозга с прогрессирующим уменьшением общего внутричерепного объёма. Локальные структурные изменения могут включать склероз гиппокампа, нарушение чёткости дифференцировки серого и белого веществ в височных долях, а также признаки церебральной или мозжечковой атрофии. В редких случаях описаны мальформации кортикального развития[6].
Молекулярно-генетический анализ крови методом секвенирования по Сэнгеру: характерно выявление мутации в гене SCN1A. Также возможно выявление мутаций в генах GABRG2, GABRA1, SCN1B, SCN2A, STXBP1 и PCDH19[5].
Основными критериями диагностики СД являются[1]:
- дебют приступов на первом году жизни;
- фебрильные приступы, альтернирующие гемиконвульсии;
- миоклонические приступы, которые проявляются после 2 лет;
- атипичные абсансы, тяжёлые тонико-клонические приступы, фокальные приступы;
- высокая частота приступов, фебрильно провоцируемые приступы, эпилептический статус;
- выраженные когнитивные расстройства;
- замедление основной фоновой активности на ЭЭГ, сочетание диффузной и региональной эпилептиформной активностей, ранние проявления фотосенситивности;
- лёгкие диффузные изменения на магнитно-резонансной томографии;
- выявленная мутация в гене SCN1A (отсутствие мутации не исключает СД).
Дифференциальная диагностика
Дифференциальная диагностика СД проводится со следующими состояниями[5]:
- синдром Веста;
- синдром Леннокса — Гасто;
- абсансные формы эпилепсии;
- неонатальные судороги;
- синдром Ландау — Клеффнера;
- атипичная доброкачественная парциальная эпилепсия.
Осложнения
СД характеризуется широким спектром осложнений и коморбидных патологий, затрагивающих практически все системы организма. К ним относятся[6]:
- неврологические и психиатрические нарушения: практически у всех пациентов наблюдается интеллектуальная недостаточность (от 67 до 100 % случаев), часто в тяжёлой степени. Высока распространённость расстройств аутистического спектра (0—100 %, по разным данным) и синдрома дефицита внимания и гиперактивности (до 66 %). Часты нарушения сна, отмечаемые у 75 % пациентов, которые могут быть как причиной, так и следствием плохо контролируемых приступов. У взрослых пациентов описаны паркинсонические симптомы;
- двигательные расстройства включают атаксию (в 62 % случаев), нарушения походки и гемипарез (около 5 %). Существует повышенный риск остеопении и, как следствие, переломов, что характерно для пациентов с фармакорезистентной эпилепсией;
- вегетативная дизавтономия затрагивает сердечную регуляцию, приводя к изменчивости сердечного ритма и аритмиям, что рассматривается как один из факторов риска внезапной неожиданной смерти при эпилепсии. Также дисфункция терморегуляции может провоцировать гипертермию и, как следствие, судорожные приступы;
- сердечно-сосудистые осложнения связаны с тем, что мутация в гене SCN1A может влиять на работу натриевых каналов не только в нейронах, но и в кардиомиоцитах, потенциально приводя к структурным и функциональным изменениям сердца;
- гастроэнтерологические осложнения: более чем у половины пациентов отмечаются такие симптомы, как запор и потеря аппетита, а у трети — нарушения жевания и глотания, попёрхивание, слюнотечение;
- эндокринные нарушения встречаются реже, но могут включать снижение темпов роста и веса, низкий уровень тиреотропного гормона, инсулиноподобного фактора роста 1 и тестостерона. Описаны случаи как задержки, так и преждевременного полового созревания;
- гематологические нарушения, такие как тромбоцитопения, дефицит витамина D и железа, выявляются примерно у трети пациентов;
- инфекционные осложнения: у пациентов часто отмечаются хронические бронхиты, пневмонии и отиты;
- зрительные нарушения: характерно прогрессирующее нарушение зрительно-моторной координации и функций зрения, что может предшествовать когнитивному снижению.
Лечение
Основной целью терапии при СД является максимальное снижение частоты и тяжести эпилептических приступов, а также предотвращение развития угрожающего жизни эпилептического статуса. В связи с характерной для синдрома фармакорезистентностью, стратегия лечения требует тщательного подбора и часто комбинации нескольких противоэпилептических препаратов[8].
Стандартная стартовая терапия базируется на применении вальпроевой кислоты или топирамата. В дальнейшем спектр используемых лекарственных средств может включать леветирацетам, зонисамид, барбитураты (например, фенобарбитал), сукцинимиды (этосуксимид), бензодиазепины и даже исторические препараты, такие как соли брома. Особенно эффективной при СД считается комбинированная схема, включающая вальпроат, стирипентол и клобазам. Стирипентол является одним из ключевых препаратов с доказанной высокой эффективностью для СД. Для пациентов в возрасте от двух лет и старше в терапии может быть использован очищенный каннабидиол. Также для снижения частоты судорожных приступов при СД может быть использован фенфлурамин[8].
Важное место в терапии занимает кетогенная диета, которая демонстрирует положительный эффект в снижении частоты приступов у ряда пациентов с резистентным течением[8].
Прогноз
СД характеризуется тяжёлым, чаще всего неблагоприятным прогнозом. Достижение стойкой ремиссии эпилептических приступов наблюдается крайне редко и, как правило, носит кратковременный характер, приводя к глубокой инвалидизации подавляющего большинства пациентов. С возрастом, в подростковом периоде, частота судорожных приступов может снижаться. Однако на первый план в клинической картине выходят тяжёлые и необратимые неврологические и психические нарушения: выраженные экстрапирамидные расстройства и грубый когнитивный дефицит, определяющие качество жизни. Заболевание сопряжено с высоким риском летальности. В младенческом и раннем детском возрасте смертность достигает около 20 %. У взрослых пациентов одной из наиболее частых непосредственных причин смерти является синдром внезапной смерти при эпилепсии, на втором месте по значимости находится смерть вследствие развития эпилептического статуса[1].
Диспансерное наблюдение
Профилактика
Не разработана.
Примечания
Литература
- Абусуева Б. А., Шанавазова М. Д., Аскевова М. А. и др. Случай атипичного течения тяжёлой миоклонической эпилепсии младенчества (синдрома Драве) // Эпилепсия и пароксизмальные состояния. — 2024. — Т. 16, № 2. — С. 130—136. — doi:10.17749/2077-8333/epi.par.con.2024.180.
- Fan H. C., Yang M. T., Lin L. C. et al. Clinical and Genetic Features of Dravet Syndrome: A Prime Example of the Role of Precision Medicine in Genetic Epilepsy (англ.) // International Journal of Molecular Sciences. — 2024. — Vol. 25, no. 1. — P. 31. — doi:10.3390/ijms25010031.
- Anwar A., Arumaithurai K., Malik P. et al. Dravet Syndrome: An Overview (англ.) // Cureus. — 2019. — Vol. 11, no. 6. — P. e5006. — doi:10.7759/cureus.5006.