Неонатальные судороги
Неоната́льные су́дороги (НС) — приступы, возникающие в течение четырёх недель после рождения у доношенных детей или в течение 44 недель постменструального возраста у недоношенных младенцев, и представляют собой наиболее распространённое неврологическое состояние в этом периоде, ассоциированное с высокой летальностью, достигающей 20 %. Данное состояние может приводить к отдалённым неблагоприятным исходам, таким как эпилепсия, детский церебральный паралич, задержки развития и психомоторные нарушения, в зависимости от этиологии и клинического течения. Большинство НС являются острыми, симптоматическими и провоцируются тяжёлыми повреждениями головного мозга, такими как гипоксически-ишемическая энцефалопатия или внутричерепные кровоизлияния, однако часть случаев может быть связана с дебютом эпилепсии неонатального периода, обусловленной структурными, метаболическими или генетическими заболеваниями[1][2].
Классификация
Классификация НС включает следующие типы[3]:
- клонические судороги характеризуются ритмичными подёргиваниями, обычно с частотой 1—3 раза в секунду, наиболее часто ассоциированы с электроэнцефалографическим (ЭЭГ) паттерном эпилептического приступа и могут затрагивать одну конечность или одну сторону тела;
- тонические судороги могут быть фокальными (с вовлечением одной конечности и обычно сопровождающимися ЭЭГ-разрядом) или генерализованными, которые проявляются тоническим разгибанием конечностей и часто напряжением мышц туловища по типу опистотонуса, имитируя децеребрационную позу. Большинство генерализованных тонических проявлений не имеют ЭЭГ-коррелята и считаются неэпилептическими;
- миоклонические судороги могут быть фокальными (в одной конечности) или мультифокальными (в нескольких частях тела), при этом они, как правило, также не сопровождаются эпилептической активностью на ЭЭГ и рассматриваются как неэпилептические проявления, отражающие тяжёлую энцефалопатию.
Этиология
Этиология неонатальных судорог многогранна и подразделяется на несколько ключевых категорий, различающихся по частоте, времени манифестации и прогнозу[2][3]:
- Острые симптоматические (реактивные) судороги составляют подавляющее большинство случаев и возникают как ответ на острые церебральные повреждения или системные нарушения. Наиболее частой причиной является гипоксически-ишемическая энцефалопатия, на которую приходится 35—45 % всех неонатальных судорог, с пиком начала в первые 12—24 часа жизни. Вторая по распространённости группа — цереброваскулярные события, такие как ишемический инсульт (часто вследствие эмболии) и внутричерепные кровоизлияния. Острые метаболические нарушения (гипогликемия, гипокальциемия, дисэлектролитемия) также способны провоцировать судороги. Наконец, инфекции центральной нервной системы (бактериальные, такие как стрептококк группы B, или вирусные, например, герпетический энцефалит) могут вызывать судороги в любой момент неонатального периода.
- Неонатальные эпилепсии, на которые приходится около 13 % причин развития НС, представляют собой эпилептические синдромы, дебютирующие в неонатальном периоде. К ним относятся саморазрешающиеся (доброкачественные) формы, такие как саморазрешающаяся семейная неонатальная эпилепсия (аутосомно-доминантные каналопатии, связанные с генами KCNQ2, KCNQ3, SCN2A) и саморазрешающиеся неонатальные судороги («судороги пятого дня»), характеризующиеся благоприятным исходом. С другой стороны, выделяются тяжёлые эпилептические энцефалопатии с неблагоприятным прогнозом: ранняя младенческая эпилептическая энцефалопатия (синдром Отахары), ранняя миоклоническая энцефалопатия (с миоклоническими приступами и аналогичным ЭЭГ-паттерном) и эпилепсия младенчества с мигрирующими фокальными приступами (рефрактерные судороги с миграцией очага по коре).
- Структурные аномалии развития мозга (мальформации коры), такие как лиссэнцефалия, гемимегалэнцефалия, фокальная корковая дисплазия, туберозный склероз и полимикрогирия, могут быть причиной НС. Они возникают из-за нарушений пролиферации, миграции или организации нейронов и часто связаны с генетическими мутациями (например, в генах ARX, TSC1/TSC2, DCX), реже — с внутриутробными инфекциями или ишемией.
- Врождённые нарушения метаболизма являются редкой, но важной причиной трудно поддающихся лечению судорог, составляя до 30 % случаев фармакорезистентных НС. К наиболее значимым и потенциально курабельным формам относятся: пиридоксин-зависимая эпилепсия (мутации ALDH7A1), эпилепсия, отвечающая на пиридоксаль-5'-фосфат (дефицит PNPO), дефицит биотинидазы, фолиево-кислотная эпилепсия, дефицит транспортёра глюкозы I типа (мутации SLC2A1) и глициновая энцефалопатия.
Патогенез
Патогенез НС обусловлен уникальными возрастными особенностями незрелого мозга, которые создают условия для повышенной судорожной готовности. Фундаментальным механизмом является нейрофизиологическое состояние, при котором возбуждающие нейронные цепи созревают рано, а тормозные — поздно. Эта относительная гипервозбудимость является важным физиологическим условием для активности процессов развития, таких как нейрогенез, миграция и дифференцировка клеток, синаптогенез и формирование нейронных сетей. Конкретные молекулярные основы включают[2]:
- усиление возбуждающей нейропередачи и недостаточность тормозных механизмов вследствие изменений в функциях рецепторов глутамата и гамма-аминомасляной кислоты;
- возрастные изменения нейрональных ионных каналов и нейропептидов;
- раннюю, зависящую от возраста активацию микроглии в развивающейся центральной нервной системе.
Дополнительные структурные особенности усугубляют эту предрасположенность. Из-за неполной арборизации аксонов и дендритных отростков, а также недостаточной миелинизации, электрическая активность в мозге распространяется медленнее и фрагментированно. Это объясняет, почему НС обычно носят фокальный характер, часто бывают кратковременными, а генерализованные тонико-клонические приступы встречаются редко или отсутствуют[2].
Ещё одной важной характеристикой является более развитое состояние лимбической системы в её связи со средним мозгом и стволом мозга по сравнению с организацией коры головного мозга. Это приводит к высокой частоте таких проявлений судорог, как сосательные движения, девиация глаз и апноэ, а также способствует феномену диссоциированных (неполных) электро-клинических приступов, когда противосудорожная терапия может купировать клинические проявления, но электроэнцефалографическая судорожная активность сохраняется. Указанные физиологические особенности более выражены у недоношенных детей, чем у доношенных: чем меньше гестационный возраст, тем короче приступы и выше доля субклинических или исключительно электроэнцефалографических судорог[2].
Эпидемиология
Частота встречаемости НС окончательно не установлена, однако, по имеющимся оценкам, она составляет 80—120 случаев на 100 000 новорождённых в год. При этом заболеваемость судорогами в неонатальном периоде выше, чем в любой другой период жизни. Что касается специфических синдромов неонатальной эпилепсии, их известная распространённость варьируется: саморазрешающаяся неонатальная эпилепсия встречается с частотой примерно 5,3 случая на 100 000 живорождений, ранняя младенческая эпилептическая энцефалопатия развития является редким заболеванием с оценочной распространённостью около 0,11 на 100 000 детей, пиридоксин-зависимая эпилепсия встречается с вариабельной частотой — от 1 случая на 65 000 до 1 случая на 783 000 родов[3].
Диагностика
НС обычно начинаются фокально, но могут распространяться на всё тело. Генерализованное начало приступов встречается редко. Клиническое распознавание судорог у новорождённых затруднено, так как судорожные движения у младенцев часто имеют сложный, нерегулярный или тонкий (субтильный) характер[1].
При физикальном обследовании ключевое значение имеет оценка психического статуса новорождённого, так как его изменения могут указывать на наличие эпилептических энцефалопатий. Измерение размера головы является критически важным: микроцефалия может быть следствием врождённых или внутриутробных повреждений мозга, а также генетических нарушений, в то время как макроцефалия может указывать на гидроцефалию или определённые врождённые нарушения метаболизма. Выбухающий родничок также может быть признаком гидроцефалии, потенциально вызванной внутрижелудочковым кровоизлиянием и указывающим на острые провоцированные судороги[4].
Специфические кожные проявления часто указывают на факоматозы: гипопигментированные «пепельные» пятна ассоциированы с туберозным склерозом, пятна цвета портвейна в распределении первой и второй ветвей тройничного нерва — с синдромом Стерджа — Вебера, а дерматомальные пузыри — с недержанием пигмента (incontinentia pigmenti). Мышечный тонус представляет собой критический компонент неврологической оценки новорождённого, поскольку его оценка помогает определить временные рамки повреждения мозга (гипотония характерна для острой фазы, а гипертонус — для хронической), а также может указывать на лежащую в основе судорог генетическую или структурную причину[4].
Магнитно-резонансная томография является методом выбора для нейровизуализации у всех новорождённых с НС, который позволяет выявить структурные изменения и пороки развития головного мозга. При подозрении на артериальный ишемический инсульт или венозный тромбоз проводится дополнительная последовательная визуализация с использованием магнитно-резонансной ангиографии. Магнитно-резонансная спектроскопия может быть полезна при подозрении на лежащее в основе метаболическое расстройство[4].
Ультразвуковое исследование головы: используется для оценки наличия внутрижелудочкового кровоизлияния или гидроцефалии у клинически тяжёлых младенцев[4].
Эхокардиография: позволяет исключить снижение сократительной способности сердца как следствие генерализованной гипоксии[3].
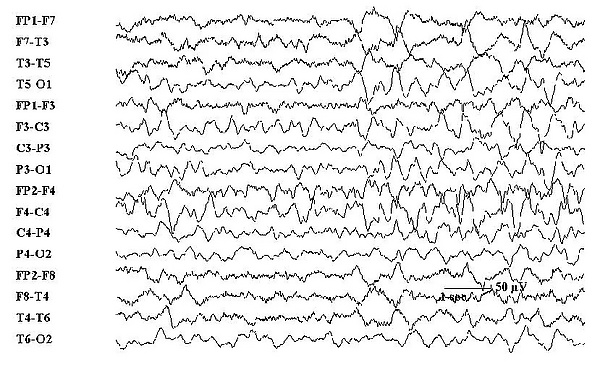
Электроэнцефалография: играет ключевую роль в точной идентификации НС и их дифференциации от неэпилептических событий. ЭЭГ-характеристики неонатальных судорог существенно отличаются от таковых у детей старшего возраста и взрослых. Межприступные (интериктальные) эпилептиформные разряды у новорождённых встречаются редко. Основную диагностическую ценность несёт фоновая (базисная) активность, оценка которой помогает определить степень и объём повреждения мозга, предположить диагноз и прогноз. Иктальная (судорожная) активность на ЭЭГ характеризуется устойчивой ритмической активностью с разнообразной морфологией, амплитудой и частотой. У недоношенных детей такая активность встречается реже, чем у доношенных. Все эпилептические судороги у новорождённых начинаются фокально, за исключением генерализованной активности, связанной с некоторыми типами миоклонических подёргиваний или эпилептических спазмов. Наиболее частыми зонами возникновения являются центральная или височная область одного полушария, а также срединная центральная область; реже — затылочная и лобная области. Зона коркового вовлечения определяет моторные проявления клинических судорог. Хотя начало, морфология, частота или паттерны распространения электрической активности, как правило, не связаны с конкретной этиологией, известны некоторые характерные ЭЭГ-паттерны, ассоциированные с определёнными причинами[2]:
- фокальные разряды могут наблюдаться при сосудистых нарушениях или электролитном дисбалансе;
- мультифокальные разряды характерны для витамин-зависимых нарушений;
- паттерн «вспышка-подавление» типичен для тяжёлых эпилептических энцефалопатий[3].
Для оценки общего состояния пациента и исключения сопутствующей патологии выполняются клинический анализ крови, коагулограмма, биохимический анализ крови и клинический анализ мочи[1].
Молекулярно-генетический анализ крови методом секвенирования по Сэнгеру: используется для определения генетических мутаций, ведущих к развитию НС. К возможным мутациями относятся: KCNQ2, KCNQ3, SCN2A, ARX, TSC1, TSC2, DCX, ALDH7A1, PNPO и SLC2A1[2][3].
Дифференциальная диагностика
Дифференциальная диагностика НС проводится со следующими заболеваниями:
- мозжечковое кровоизлияние;
- синдром Драве;
- неонатальный менингит;
- вирусный энцефалит;
- субдуральная гематома;
- субарахноидальное кровоизлияние;
- туберозный склероз;
- синдром Сандифера;
- гиперэкплексия;
- изолированное апноэ.
Осложнения
Неонатальные судороги представляют серьёзную угрозу для развивающегося мозга, способную нарушить процесс синаптогенеза и привести к стойким неврологическим дефицитам. Наиболее частыми отдалёнными последствиями являются когнитивные нарушения различной степени выраженности и повышенный риск развития детского церебрального паралича, особенно у глубоко недоношенных детей с экстремально низкой массой тела. Специфика осложнений напрямую зависит от этиологии судорог и типа диагностированного эпилептического синдрома, варьируя от умеренных трудностей обучения до тяжёлых форм глобальной задержки психомоторного развития, резистентной к лечению эпилепсии и сокращения продолжительности жизни. Хотя изолированные кратковременные приступы могут не оказывать выраженного негативного влияния, нелеченые или плохо контролируемые судороги способны индуцировать структурные повреждения мозга, такие как гиппокампальный склероз[1][3].
Лечение
Лечение НС требует агрессивного и комплексного подхода. Первостепенной задачей является корректировка выявленных метаболических нарушений: электролитный дисбаланс, гипогликемия и гипокальциемия. При подозрении на врождённое нарушение метаболизма энтеральное питание временно прекращают и переходят на парентеральное. После стабилизации метаболического статуса начинают противосудорожную терапию. Препаратом первой линии является фенобарбитал. При его неэффективности в качестве второй линии терапии добавляют фенитоин или леветирацетам. При рефрактерных судорогах могут применяться внутривенные бензодиазепины (лоразепам, мидазолам) или лидокаин[3].
В остром периоде необходим мониторинг концентраций противосудорожных препаратов в крови. При отсутствии повторных приступов терапию, как правило, постепенно отменяют в возрасте 3—6 месяцев. Отмену препаратов проводят постепенно, особенно если пациент получал два препарата (их отменяют последовательно). В случае рецидива судорог терапию возобновляют. Учитывая долгосрочные побочные эффекты фенобарбитала и сложности поддержания терапевтического уровня фенитоина, при необходимости длительного лечения могут рассматриваться альтернативные препараты, такие как леветирацетам, окскарбазепин или топирамат[3].
Прогноз
Прогноз при неонатальных судорогах является неоднородным и определяется комплексом факторов, включая этиологию, возраст дебюта, продолжительность судорожной активности и ответ на противосудорожную терапию. Своевременное распознавание и начало лечения остаются краеугольным камнем для предотвращения неблагоприятных последствий и оптимизации долгосрочных исходов. Прогноз варьируется от благоприятного течения, характерного для саморазрешающихся эпилептических синдромов, которые спонтанно ремиттируют, несмотря на частые неонатальные приступы, до крайне неблагоприятного прогноза при тяжёлых эпилептических энцефалопатиях развития, обусловленных диффузным поражением мозга или генетическими мутациями, которые ассоциированы с фармакорезистентностью, глубокой задержкой развития и высокой инвалидизацией[1].
Диспансерное наблюдение
После перенесённых неонатальных судорог все пациенты нуждаются в длительном, многопрофильном диспансерном наблюдении для контроля терапии, оценки развития и своевременной реабилитации[3][5]:
- Наблюдение у врача-невролога является основным. Невролог определяет продолжительность и тактику противосудорожной терапии, решает вопрос о её постепенной отмене на основе данных анамнеза, клинического состояния и результатов ЭЭГ-мониторинга.
- Оценка психомоторного развития обязательна для раннего выявления возможных физических или когнитивных дефицитов.
- Ортопедический и физиотерапевтический мониторинг необходим пациентам с нарушениями мышечного тонуса для профилактики формирования контрактур и деформаций суставов. Показаны консультации врача физической и реабилитационной медицины, а также регулярные курсы лечебной физкультуры и физиотерапии.
Профилактика
Не разработана.
Примечания
Литература
- Kim E. H., Lee B. K., Shin J. Neonatal seizures: diagnostic updates based on new definition and classification (англ.) // Clinical and Experimental Pediatrics. — 2022. — Vol. 65, no. 8. — P. 387—397. — doi:10.3345/cep.2021.01361.
- Yozawitz Е. Neonatal Seizures (англ.) // New England Journal of Medicine. — 2023. — Vol. 388, no. 18. — P. 1692—1700. — doi:10.1056/NEJMra2300188.