Синдром Панайотопулоса
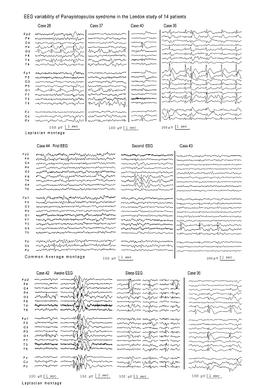
Синдро́м Панайотопу́лоса (доброка́чественная де́тская заты́лочная эпиле́псия ти́па Панайотопу́лоса, ра́нняя доброка́чественная де́тская заты́лочная эпиле́псия) — распространённое идиопатическое детское судорожное расстройство, которое встречается исключительно у здоровых в остальном детей (идиопатическая эпилепсия) и проявляется в основном вегетативными эпилептическими припадками и вегетативным эпилептическим статусом. Согласно существующему экспертному консенсусу, синдром Панайотопулоса определяется как доброкачественное фокальное эпилептическое расстройство, связанное с возрастом и манифестирующее у детей младшего и среднего возраста. Ключевыми клиническими проявлениями являются пролонгированные приступы с выраженными вегетативными симптомами. Электроэнцефалографической особенностью синдрома служит наличие перемежающихся и/или мультифокальных паттернов, наиболее часто регистрируемых в затылочных отведениях[2].
История
История открытия и изучения синдрома неразрывно связана с именем греческого невролога, профессора Стилианоса Панайотопулоса (1939—2023). Его работа в 1970-х годах позволила выделить этот специфический эпилептический синдром из общей группы детских эпилепсий. Профессор Панайотопулос обратил внимание на уникальную и стереотипную клиническую картину у определённой группы юных пациентов: приступы у них начинались в возрасте 3—6 лет и проявлялись не типичными судорогами, а прежде всего выраженными вегетативными симптомами — тошнотой, рвотой и побледнением, часто сопровождавшимися тоническим отклонением глаз и головы в сторону. Эти состояния были необычно длительными, могли длиться часами и часто возникали во сне, что приводило к ошибочным диагнозам мигрени, энцефалита или острого гастроэнтерита[2].
Ключевым вкладом Панайотопулоса стало не просто описание симптомов, а комплексный анализ иктальных и интериктальных данных ЭЭГ, а также долгосрочное наблюдение за естественным течением заболевания. Он установил, что, несмотря на пугающую картину приступов, прогноз у этого синдрома в большинстве случаев благоприятный: у подавляющего большинства детей приступы самостоятельно проходили с возрастом, а интеллектуальное развитие оставалось в норме. Его настойчивость и тщательный анализ увенчались успехом в 1989 году, когда синдром был официально признан и включён в Международную классификацию эпилепсий и эпилептических синдромов (ILAE) под названием «ранняя доброкачественная окципитальная эпилепсия детского возраста». Позже, в 2001 году, благодаря дальнейшим исследованиям, которые показали, что эпилептогенный очаг не всегда строго ограничен затылочной долей, синдром был переименован в честь своего первооткрывателя, получив своё современное название — синдром Панайотопулоса[2].
Этиология
Синдром Панайотопулоса относится к идиопатическим формам эпилепсии. Это означает, что он возникает у практически здоровых детей без структурных повреждений головного мозга, метаболических нарушений или предшествующих провоцирующих заболеваний[3].
- Генетическая предрасположенность: синдром считается мультигенным заболеванием, при котором комбинация вариантов в нескольких генах повышает восприимчивость к фокальной корковой гипервозбудимости. Описаны семейные случаи, а также ассоциация с другими идиопатическими эпилепсиями у родственников.
- Возраст-зависимая гипервозбудимость коры: основной патофизиологический механизм — это повышенная возбудимость коры головного мозга, которая является следствием нарушения баланса между возбуждающими (глутаматергическими) и тормозными (ГАМКергическими) процессами в мозге ребёнка. Эта гипервозбудимость носит транзиторный характер и самостоятельно регрессирует по мере созревания мозга, что объясняет доброкачественное течение и самокупирующийся характер синдрома.
- Провоцирующие факторы: У предрасположенных детей приступы могут быть спровоцированы внешними факторами, такими как:
- Инфекции (часто на фоне лихорадки).
- Внезапное пробуждение ото сна.
- Эмоциональный стресс.
Патогенез
Патогенез синдрома Панайотопулоса, несмотря на его чёткую клиническую картину, остаётся предметом активных исследований, однако ключевым механизмом признаётся возраст-зависимая корковая гипервозбудимость, имеющая генетическую основу. В отличие от симптоматических эпилепсий, при этом синдроме отсутствуют структурные повреждения головного мозга, такие как пороки развития, опухоли или последствия гипоксии, а все нарушения носят исключительно функциональный и преходящий характер, что и объясняет его благоприятный прогноз[4].
Основу патогенеза составляет генетическая предрасположенность, которая определяет повышенную готовность мозга к гиперсинхронным разрядам. Синдром относится к идиопатическим формам эпилепсии, что подразумевает полигенный тип наследования. Это означает, что за его реализацию отвечает не одна мутация, а комбинация вариантов (полиморфизмов) в нескольких генах, регулирующих нейрональную возбудимость. Среди генов-кандидатов рассматриваются гены, ассоциированные с функциями ионных каналов (например, CHRNA4, SCN1A) и ГАМК-ергических рецепторов (GABRG2), однако точный генетический профиль синдрома ещё не установлен[4].
Клинические проявления напрямую связаны с нарушением баланса между возбуждающими (глутаматергическими) и тормозными (ГАМК-ергическими) системами в созревающем мозге ребёнка. В определённый период развития (пик манифестации приходится на 3—6 лет) у предрасположенных детей формируется состояние повышенной эксайтотоксичности на фоне относительной функциональной незрелости тормозных механизмов. Это приводит к тому, что нормальные процессы возбуждения в коре перерастают в патологические, распространяющиеся разряды[4].
Важной особенностью является мультифокальный характер этой гипервозбудимости. Хотя синдром исторически относили к затылочным эпилепсиям из-за частого наличия очагов в затылочных долях и зрительных симптомов, данные ЭЭГ показывают, что эпилептогенные очаги могут возникать практически в любой области коры — теменной, лобной, височной. Эта «миграция» фокусов и их мультифокальность объясняют, почему клиническая картина приступов так разнообразна и включает не только зрительные феномены, но и преимущественно вегетативные симптомы (рвота, бледность), моторные (тоническое отклонение глаз, гемиклонии) и длительные нарушения сознания[4].
Таким образом, патогенез синдрома Панайотопулоса представляет собой сложное взаимодействие генетической предрасположенности и возраст-специфических функциональных особенностей работы мозга. По мере созревания центральной нервной системы, тормозные механизмы активируются, баланс возбуждения и торможения восстанавливается, что приводит к спонтанной ремиссии — самостоятельному прекращению приступов, характерному для этого доброкачественного состояния[4].
Эпидемиология
Типичный синдром Панайотопулоса был выявлен в 6,1% случаев всех случаев эпилепсии у детей в возрасте от 1 до 14 лет[5].
Диагностика
Клиническая картина синдрома Панайотопулоса отличается выраженным полиморфизмом и характерными особенностями, что позволяет дифференцировать его от других форм эпилепсии. Основу проявлений составляют длительные вегетативные пароксизмы с нарушением сознания, возникающие преимущественно в ночное время[4].
Заболевание дебютирует в возрасте от 1 до 14 лет с пиком манифестации между 3 и 6 годами. Типичный приступ начинается внезапно, часто во время ночного сна, и характеризуется триадой основных симптомов: вегетативными нарушениями, отклонением глаз и изменением сознания. Вегетативная симптоматика доминирует в клинической картине: у 70—80 % пациентов наблюдается тошнота и повторная рвота, сопровождающиеся бледностью кожных покровов, гипергидрозом, мидриазом и нарушениями терморегуляции. Важным диагностическим признаком является тоническое отклонение глазных яблок (обычно в сторону), которое может прогрессировать до генерализованных клонических судорог[4].
Особенностью приступов при синдроме Панайотопулоса является их исключительная продолжительность — от 5—15 минут до нескольких часов, в среднем составляет 30—60 минут. На протяжении всего эпизода отмечаются нарушения сознания различной степени выраженности: от лёгкого оглушения до глубокого сопора. В межприступном периоде неврологический статус пациентов остаётся неизменным, отсутствуют когнитивные нарушения и поведенческие отклонения, что подчёркивает доброкачественную природу заболевания[4].
Видео-ЭЭГ мониторинг, выявляющий мультифокальные высокоамплитудные спайки и острые волны, часто с затылочной акцентуацией, но не ограничивающиеся одной областью. Характерно, что эпилептиформная активность значительно усиливается во время фазы медленного сна, что объясняет преимущественно ночную манифестацию приступов[4].
Дифференциальная диагностика
Дифференциальная диагностика синдрома Панайотопулоса проводится с широким спектром неврологических, соматических и психиатрических заболеваний вследствие полиморфной клинической картины, доминирования вегетативных симптомов и длительности эпизодов. Ключевыми задачами являются исключение острых жизнеугрожающих состояний, других форм эпилепсии и неэпилептических пароксизмов[3].
- Другие формы эпилепсии:
- Задняя идиопатическая затылочная эпилепсия Гасто: характеризуется преимущественно кратковременными зрительными приступами (простые феномены, иктальная слепота) с минимальными вегетативными нарушениями. В отличие от синдрома Панайотопулоса, приступы короче, а на ЭЭГ очаг стабильно локализован в затылочной области.
- Височная эпилепсия: может проявляться вегетативными симптомами (эпигастральный дискомфорт, тошнота), но для неё более характерны психические феномены (дежавю), нарушение сознания с автоматизмами, а не изолированная рвота и девиация глаз.
- Фебрильные судороги: Возникают исключительно на фоне лихорадки у детей определённого возраста (6 мес. — 5 лет), в то время как приступы при синдроме Панайотопулоса являются афебрильными.
- Структурные метаболические эпилепсии: эпилептические энцефалопатии (например, синдром Драве, синдром Леннокса — Гасто) сопровождаются задержкой психомоторного развития, полиморфными приступами, выраженными изменениями на ЭЭГ (например, паттерн «вспышка-подавление») и резистентностью к терапии, что нехарактерно для доброкачественного течения синдрома Панайотопулоса.
- Неэпилептические пароксизмальные состояния:
- Пароксизмальное головокружение: проявляется кратковременными эпизодами неустойчивости, страха и нистагма без нарушения сознания и вегетативных симптомов в полном объёме.
- Доброкачественный пароксизмальный тортиколлис: характеризуется эпизодами наклона головы без рвоты, нарушения сознания и изменений на ЭЭГ.
- Синдром циклической рвоты: проявляется стереотипными эпизодами тяжёлой рвоты без отклонения глаз, нарушений сознания и эпилептиформной активности на ЭЭГ.
- Острые соматические и неврологические заболевания:
- Энцефалит (особенно герпетический): может имитировать длительный эпилептический статус, но сопровождается стойкой лихорадкой, выраженным угнетением сознания, плеоцитозом в ликворе и очаговыми изменениями при нейровизуализации.
- Острый гастроэнтерит: проявляется рвотой и вялостью, но без нарушения сознания, девиации глаз и стереотипности эпизодов.
- Мигрень (особенно базилярная): может включать тошноту, рвоту, нарушение сознания и зрительные нарушения, однако ей предшествует аура, а сам приступ часто сопровождается головной болью, что нехарактерно для синдрома Панайотопулоса.
- Интоксикации, метаболические нарушения: требуют исключения с помощью токсикологического скрининга и оценки биохимических показателей крови.
- Психиатрические расстройства:
- Психогенные неэпилептические приступы (ПНЭП): могут имитировать различные пароксизмы, однако для них характерна эмоциональная провокация, отсутствие эпилептиформной активности на ЭЭГ во время приступа и наличие других конверсионных симптомов.
Основой дифференциальной диагностики является тщательный анализ анамнеза, видео-ЭЭГ мониторинг (особенно с записью приступа), а в сомнительных случаях — проведение МРТ головного мозга для исключения структурной патологии[3].
Лечение
Тактика ведения пациентов с синдромом Панайотопулоса имеет свои особенности, обусловленные доброкачественным течением заболевания с высокой частотой спонтанной ремиссии. Основные принципы терапии включают:
- Тактика наблюдения. Учитывая благоприятный прогноз, пациентам с редкими и короткими приступами может быть рекомендовано наблюдение без назначения противоэпилептических препаратов (ПЭП). Это связано с тем, что риски от побочных эффектов терапии могут превышать потенциальную пользу.
- Купирование длительных приступов. Приступы при синдроме Панайотопулоса часто продолжительные, что требует неотложной помощи:
- Бензодиазепины: препараты первой линии для купирования статусных эпизодов (диазепам, лоразепам per rectum или интраназально).
- Внутривенная терапия: при тяжёлых случаях — внутривенное введение лоразепама или вальпроевой кислоты.
- Профилактическая терапия ПЭП. Назначается при частых, пролонгированных или тяжёлых приступах:
- Вальпроевая кислота: препарат первого выбора благодаря эффективности при фокальных и генерализованных приступах.
- Леветирацетам: альтернативный вариант с хорошим профилем переносимости.
- Карбамазепин/окскарбазепин: могут использоваться, но с осторожностью из-за потенциального риска аггравации приступов у части пациентов.
- Образовательная поддержка семьи:
- Информирование родителей о доброкачественной природе синдрома.
- Обучение правилам оказания первой помощи при пролангированных приступах.
- Рекомендации по ведению дневника приступов.
- Отмена терапии. У большинства пациентов приступы полностью исчезают к 12—14 годам. Отмена ПЭП рассматривается после двух лет ремиссии и подтверждения благоприятного течения по данным ЭЭГ[6].
Прогноз
В отличие от многих других форм эпилепсии, синдром Панайотопулоса характеризуется благоприятным прогнозом — у 90—95 % пациентов наблюдается спонтанная ремиссия с полным прекращением приступов к подростковому возрасту[7].
Диспансерное наблюдение
Диспансерное наблюдение за детьми с синдромом Панайотопулоса является важным компонентом терапии и требует индивидуального подхода, ориентированного на благоприятный прогноз и низкий риск осложнений. Основная цель наблюдения — контроль течения заболевания, своевременная коррекция терапии при необходимости и обеспечение нормального нервно-психического развития ребёнка. После постановки диагноза осмотры детским неврологом проводятся с частотой 1 раз в 3—6 месяцев для оценки клинической динамики и возможных побочных эффектов противоэпилептической терапии. При достижении стойкой ремиссии частота наблюдений сокращается до 1 раза в 6—12 месяцев. После отмены терапии рекомендованы осмотры через 3, 6 и 12 месяцев для подтверждения сохранения ремиссии[4].
Ключевыми компонентами диспансерного наблюдения являются: оценка частоты и характеристик приступов с обязательным ведением дневника пароксизмов родителями; мониторинг эффективности и переносимости противоэпилептических препаратов при их назначении; регулярное проведение видео-ЭЭГ мониторинга для объективной оценки динамики эпилептиформной активности; оценка психомоторного развития и когнитивных функций ребёнка; а также образовательная поддержка семьи, включающая разъяснение доброкачественной природы заболевания и обучение правилам оказания первой помощи при пролонгированных приступах. Важно отметить, что, учитывая высокую вероятность спонтанной ремиссии, тактика активного наблюдения без назначения медикаментозной терапии является предпочтительной для пациентов с редкими и короткими приступами[4].
Профилактика
В связи с тем, что синдром Панайотопулоса является генетически обусловленным идиопатическим заболеванием, первичная профилактика (направленная на предотвращение его возникновения) не разработана. Отсутствуют известные методы предотвращения дебюта заболевания у генетически предрасположенных лиц[3].