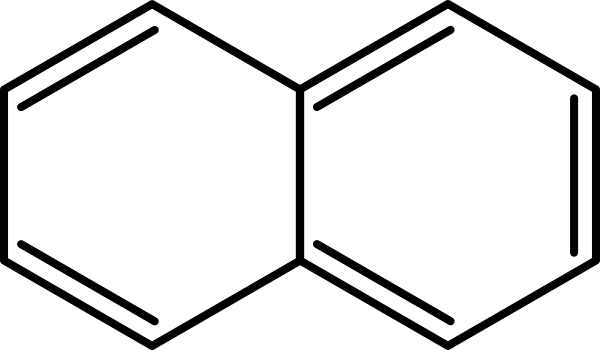
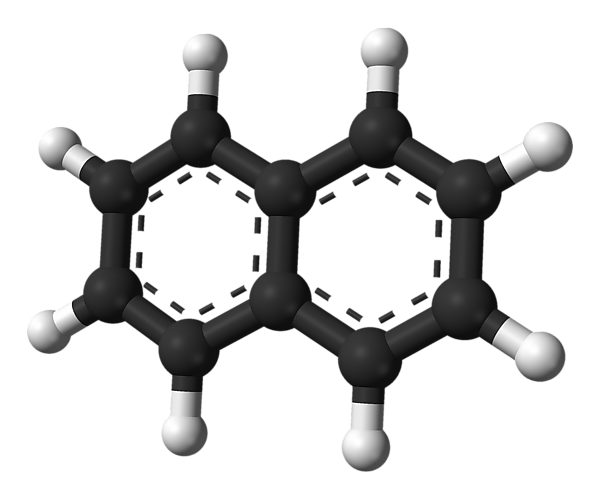
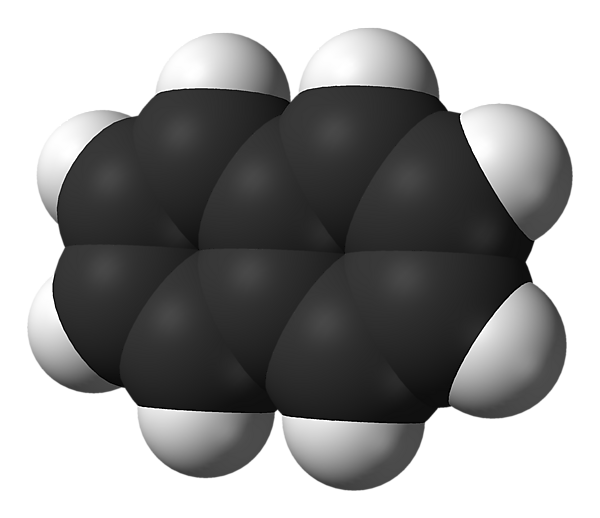
Нафталин
Нафтали́н (бицикло-[4.4.0]-дека-1,3,5,7,9-пентаен, гексален, антимит) — органическое соединение состава C10H8. Представляет собой твёрдое кристаллическое вещество с характерным запахом. В воде мало растворим. Хорошо растворим в бензоле, эфире, спирте, хлороформе.
Общие сведения
| Нафталин | |
|---|---|
| Общие | |
| Систематическое наименование |
Нафталин |
| Традиционные названия | Нафталин, антимит, гексален |
| Хим. формула | С10Н8 |
| Рац. формула | С10Н8 |
| Физические свойства | |
| Молярная масса | 128,17052 г/моль |
| Плотность |
1,14 г/см3 (15,5 °C); 1,0253 г/см3 (20 °C); 0,9625 г/см3 (100 °C)[1] |
| Энергия ионизации | 8,12 ± 0,01[2] |
| Термические свойства | |
| Температура | |
| • плавления | 80,26 °C |
| • кипения | 217,97[1] °C |
| • вспышки | 79—87 °C |
| Пределы взрываемости | 0,9 ± 0,1[2] |
| Мол. теплоёмк. | 165,72[1] Дж/(моль·К) |
| Энтальпия | |
| • образования | 78,53[1] кДж/моль |
| Давление пара | 0,08 ± 0,01[2] |
| Оптические свойства | |
| Показатель преломления | 1,5898[1] |
| Классификация | |
| Рег. номер CAS | 91-20-3 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 931 |
| UNII | 2166IN72UN |
| CompTox Dashboard EPA | DTXSID8020913 |
| Рег. номер EINECS | 202-049-5 |
| SMILES | |
| InChI | |
| RTECS | QJ0525000 |
| ChEBI | 16482 |
| ChemSpider | 906 |
| ECHA InfoCard | 100.001.863 |
| Безопасность | |
| Предельная концентрация | 20 мг/м³ |
| ЛД50 | 5000-12376 мг/кг |
| Токсичность | Зарегистрированные препараты нафталина относятся к 4-му классу опасности для человека, оказывают общетоксическое действие. |
| NFPA 704 | |
Химические свойства
Нафталин по химическим свойствам сходен с бензолом: легко нитруется, сульфируется, взаимодействует с галогенами. Отличается от бензола тем, что легче вступает в реакции[3].
Физические свойства
Плотность 1,14 г/см³, температура плавления 80,26 °C, температура кипения 217,7 °C, растворимость в воде примерно 30 мг/л, температура вспышки 79—87 °C, температура самовоспламенения 525 °C, молярная масса 128,17052 г/моль, давление пара (при температуре 80 °C) 1040 Па.
Кристаллический нафталин имеет заметную электропроводность при комнатной температуре с удельным сопротивлением около 1012 Ом·м. При плавлении удельное сопротивление уменьшается более чем в тысячу раз, примерно до 4·108 Ом·м.
Как в жидком, так и в твёрдом виде сопротивление зависит от температуры приблизительно как , где (Ом·м) и (эВ) — некоторые постоянные параметры, — постоянная Больцмана (8,617·10−5 эВ/K), а — абсолютная температура (K). Параметр равен 0,73 эВ в твёрдом нафталине. В твёрдом виде имеет полупроводниковый тип проводимости при температуре даже ниже 100 К[4][5].
Получение
Нафталин получают из каменноугольной смолы.
Также нафталин можно выделять из тяжёлой смолы пиролиза (закалочное масло), которая применяется в процессе пиролиза на этиленовых установках. Ещё одним способом промышленного получения нафталина является деалкилирование его алкилпроизводных.
В природе нафталин выделяют термиты вида Coptotermes formosanus, чтобы защитить свои гнёзда от муравьёв, грибков и нематод[6].
В Восточной Европе нафталин производится различными интегрированными металлургическими комплексами (Северсталь, Евраз, Мечел, ММК) в России, специализированными производителями нафталина и фенола ИНКОР, Енакиевским металлургическим заводом на Украине и АрселорМиттал Темиртау в Казахстане.
Применение
Важное сырьё химической промышленности: применяется для синтеза фталевого ангидрида, тетралина, декалина, разнообразных производных нафталина.
Производные нафталина применяют для получения красителей и взрывчатых веществ, в медицине, как инсектицид моли в быту.
Крупные монокристаллы применяются в качестве сцинтилляторов для регистрации ионизирующих излучений.
Может использоваться для создания синтетических аналогов каннабиноидов.
Влияние на здоровье
При остром отравлении нафталин вызывает головные боли, тошноту, рвоту, раздражение слизистых оболочек. Длительное воздействие нафталина может вызвать повреждение или разрушение красных кровяных телец (эритроцитов). Хроническое воздействие нафталина также приводит к нарушению работы печени и поджелудочной железы, вызывает развитие атрофического ринита и фарингита.
Международное агентство по изучению рака (IARC) классифицировало нафталин как возможный канцероген людей и животных (Group 2B).
В человеческом организме чаще всего концентрируется в жировой ткани, где может накапливаться до тех пор, пока жировая ткань не начнёт сжигаться, и данное вещество (нафталин) не попадёт в кровь, после чего наступает отравление организма (кровотечения, возникновение опухолей и т. д.).
Исследование в 2022 году показало, что в комнате с компьютером уровни содержания в воздухе полициклических ароматических углеводородов (ПАУ) были в 2—2,5 раз выше, чем на открытом воздухе или в помещении без компьютера. Преобладающими были такие токсичные вещества как нафталин и фенантрен.[7]
Производные
Примечания
Литература
- Новый справочник химика и технолога. Радиоактивные вещества. Вредные вещества. Гигиенические нормативы / Редкол.: Москвин А. В. и др.. — СПб.: АНО НПО «Профессионал», 2004. — 1142 с.

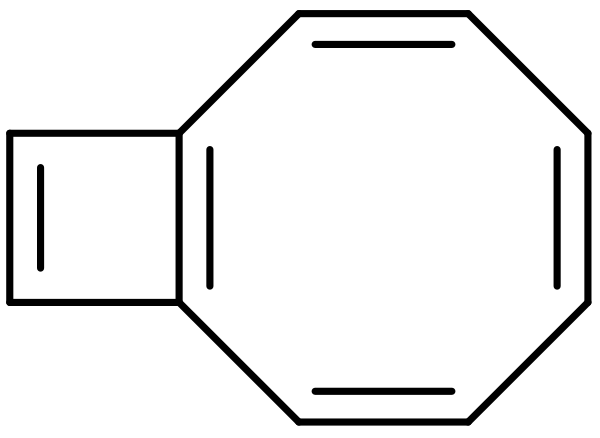
![{\displaystyle \rho =\rho _{0}\ \exp[E/(kT)]}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/567576e8080598839bf3164a83eb3f79ea2500a8)