Бутан (вещество)
Бута́н (C4H10) — органическое соединение, углеводород класса алканов. В химии название используется в основном для обозначения н-бутана. Такое же название имеет смесь н-бутана и его изомера изобутана CH(CH3)3. Название происходит от корня «бут-» (французское название масляной кислоты — acide butyrique, от др.-греч. βούτῡρον, масло[3]) и суффикса «-ан» (принадлежность к алканам). Вдыхание бутана вызывает дисфункцию лёгочно-дыхательного аппарата. Содержится в природном газе, образуется при крекинге нефтепродуктов, при разделении попутного нефтяного газа, «жирного» природного газа. Как представитель углеводородных газов пожаро- и взрывоопасен, малотоксичен, имеет специфический характерный запах, обладает наркотическими свойствами. По степени воздействия на организм газ относится к веществам 4-го класса опасности (малоопасные) по ГОСТ 12.1.007-76[4]. Вредно воздействует на нервную систему[5]. При использовании в токсикомании может вызывать сильное привыкание.
Что важно знать
| Бутан | |
|---|---|
| Общие | |
| Хим. формула | C4H10 |
| Физические свойства | |
| Молярная масса | 58,12 г/моль |
| Плотность |
газ (при 0 °C) 2558 (нормальные условия) кг/м³[1] 0,6010 г/см³ |
| Энергия ионизации | 10,63 |
| Термические свойства | |
| Температура | |
| • плавления | −138,4 °C |
| • кипения | −0,5 °C |
| • вспышки | −76[2] и −60[2] |
| • самовоспламенения | 372 °C |
| Пределы взрываемости | 1,6 |
| Энтальпия | |
| • сгорания |
124 МДж/м³ 47,9 МДж/кг[1] 2778 кДж/моль |
| Давление пара | 2,05 |
| Химические свойства | |
| Растворимость | |
| • в воде | 6,1 мг в 100 мл |
| Классификация | |
| Рег. номер CAS | 106-97-8 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 7843 |
| UNII | 6LV4FOR43R |
| CompTox Dashboard EPA | DTXSID7024665 |
| Рег. номер EINECS | 203-448-7 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E943a |
| RTECS | EJ4200000 |
| ChEBI | 37808 |
| Номер ООН | 1011 |
| ChemSpider | 7555 |
| ECHA InfoCard | 100.003.136 |
| Безопасность | |
| Предельная концентрация | 300 мг/м³ |
| NFPA 704 | |
Изомерия
Физические свойства
- Бутан — бесцветный горючий газ, со специфическим запахом, при нормальном давлении легко сжижаем от −0,5 °C, замерзает при −138 °C; при повышенном давлении и обычной температуре — легколетучая жидкость. Критическая температура +152 °C, критическое давление 3,797 МПа.
- Растворимость в воде — 6,1 мг в 100 мл (для н-бутана, при 20 °C), значительно лучше растворяется в органических растворителях[6]). Может образовывать азеотропную смесь с водой при температуре около 100 °C и давлении 10 атм.
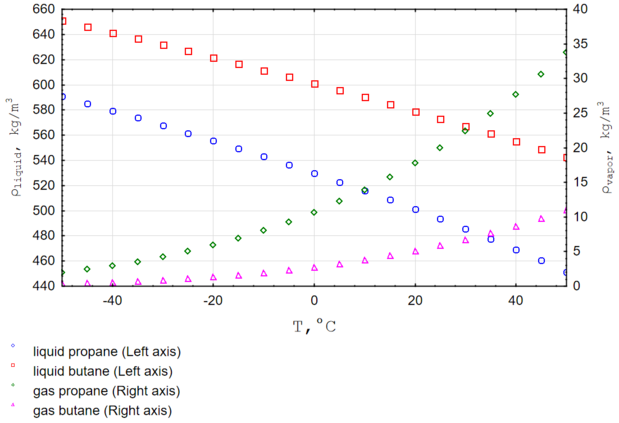
- Плотность жидкой фазы — 580 кг/м³[7]
- Плотность газовой фазы при нормальных условиях — 2,703 кг/м³.
- Теплота сгорания 45,8 МДж/кг (2657 кДж/моль (см.[8]).
Плотность бутана существенно зависит от температуры[9].
Нахождение и получение
- Можно получить путём электролиза пропионовой кислоты:
Сероочистка (демеркаптанизация) бутановой фракции
Прямогонную бутановую фракцию необходимо очищать от сернистых соединений, которые в основном представлены метил- и этил- меркаптанами. Метод очистки бутановой фракции от меркаптанов заключается в щёлочной экстракции меркаптанов из углеводородной фракции и последующей регенерации щёлочи в присутствии гомогенных или гетерогенных катализаторов кислородом воздуха с выделением дисульфидного масла.
Применение и реакции
При свободно радикальном хлорировании образует смесь 1-хлор- и 2-хлорбутана. Их соотношение хорошо объясняется разницей в прочности связей С—Н в позиции 1 и 2 (425 и 411 кДж/моль).
При полном сгорании на воздухе образует углекислый газ и воду. Бутан применяется в смеси с пропаном в зажигалках, в газовых баллонах в сжиженном состоянии. Температура кипения бутана −0,5 °C, значительно выше, чем у пропана (−42 °C), поэтому в чистом виде его можно использовать только в теплом климате. Иногда используются «зимние» и «летние» смеси с различным составом (в летних бутана до 50%, в зимних — не больше 15%). Теплота сгорания 1 кг — 45,7 МДж (12,72 кВт·ч).
При недостатке кислорода образуется сажа, угарный газ или их смесь:
Фирмой DuPont разработан метод получения малеинового ангидрида из н-бутана при каталитическом окислении:
н-Бутан — сырьё для получения бутилена, 1,3-бутадиена, компонент бензинов с высоким октановым числом. Бутан высокой чистоты и особенно изобутан может быть использован в качестве хладагента в холодильных установках. Производительность таких систем немного ниже, чем фреоновых, но бутан безопасен для окружающей среды, в отличие от фреоновых хладагентов.
В пищевой промышленности бутан зарегистрирован в качестве пищевой добавки E943a, а изобутан — E943b, как пропеллент.
Безопасность
Легковоспламеним. Пределы взрываемости 1,4—9,3 % в воздухе по объёму. ПДК в воздухе рабочей зоны — 300 мг/м³.
См. также
Примечания
Литература
- Львов М. Д. Бутан, углеводород // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.