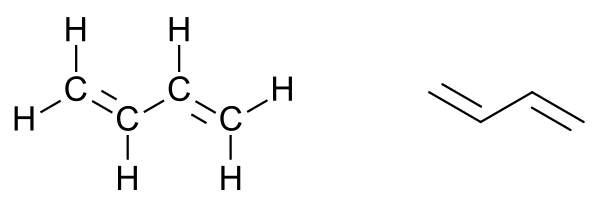
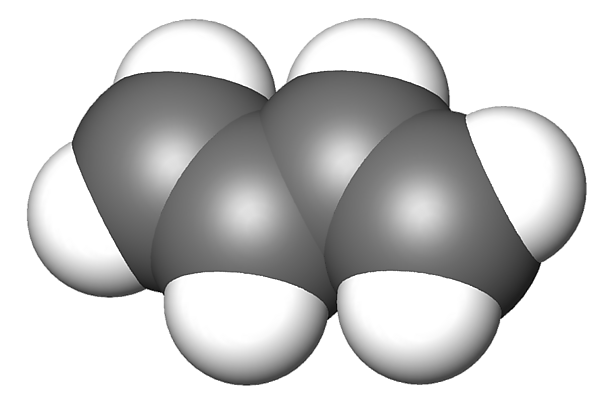
Бутадиен
Бутадие́н-1,3 (дивини́л, бу́та-1,3-дие́н) — ненасыщенный углеводород, простейший представитель сопряжённых диеновых углеводородов.
Общие сведения
| Бутадиен | |
|---|---|
| Общие | |
| Систематическое наименование |
бута-1,3-диен |
| Традиционные названия | дивинил, бутадиен |
| Хим. формула | C4H6 |
| Физические свойства | |
| Молярная масса | 54,09 г/моль |
| Плотность | 0,6211 (при температуре кипения) |
| Энергия ионизации | 9,07[1] |
| Термические свойства | |
| Температура | |
| • плавления | −108,9 °C |
| • кипения | −4,41 °C |
| • вспышки | −105[1] |
| Пределы взрываемости | 2[1] |
| Давление пара | 2,4[1] |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,735 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4292 |
| Классификация | |
| Рег. номер CAS | 106-99-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 7845 |
| UNII | JSD5FGP5VD |
| CompTox Dashboard EPA | DTXSID3020203 |
| Рег. номер EINECS | 203-450-8 |
| SMILES | |
| InChI | |
| RTECS | EI9275000 |
| ChEBI | 39478 |
| ChemSpider | 7557 |
| ECHA InfoCard | 100.003.138 |
| Безопасность | |
| NFPA 704 | |
Физические свойства
Бутадиен — газ с характерным неприятным запахом. Малорастворим в воде, хорошо растворим в бензоле, диэтиловом эфире, плохо растворим в метаноле и этаноле.
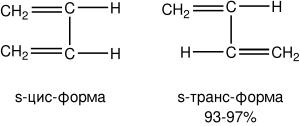
Молекулы 1,3-бутадиена могут находиться в s-цис- и s-транс-конформациях, причём последняя является преобладающей (93—97 %):
Химические свойства
Бутадиен склонен к полимеризации, легко окисляется воздухом с образованием перекисных соединений, ускоряющих полимеризацию. В воздухе с концентрацией 1,6—10,8 % об. образует взрывоопасную смесь.
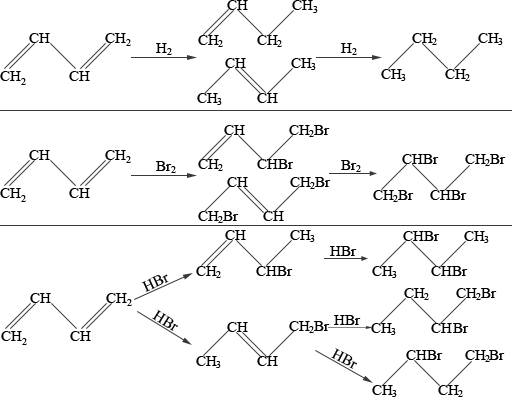
1,3-бутадиен является типичным бутадиеновым углеводородом и обладает высокой реакционной способностью. Легко вступает в реакции полимеризации, в том числе с другими непредельными соединениями — реакции сополимеризации (стиролом, эфирами и нитрилами акриловой и метакриловой кислот, изопреном, изобутиленом и др.). По двойной связи бутадиен присоединяет молекулы водорода, галогенов и галогеноводородов.
Получение
Бутадиен можно синтезировать по реакции, изученной Сергеем Лебедевым пропусканием этилового спирта через катализатор из оксидов металлов при температуре 400—450 °C[2]:
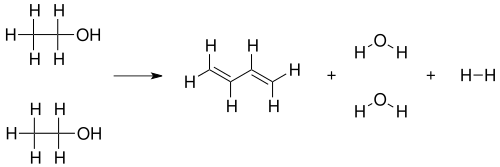 2 CH3CH2OH → CH2=CH−CH=CH2 + 2 H2O + H2
2 CH3CH2OH → CH2=CH−CH=CH2 + 2 H2O + H2
Другой способ получения бутадиена с использованием в качестве сырья этилового спирта — реакция, предложенная Иваном Остромысленским, взаимодействием уксусного альдегида (ацетальдегида) и этилового спирта на пористом катализаторе, покрытым танталом[2] при температуре 325—350 °C, сам ацетальдегид получают также из этилового спирта на предварительной стадии:
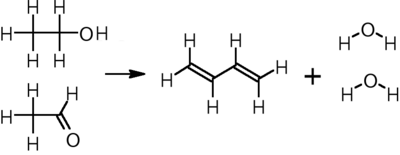 CH3CH2OH + CH3CHO → CH2=CH−CH=CH2 + 2 H2O
CH3CH2OH + CH3CHO → CH2=CH−CH=CH2 + 2 H2O
Оба способа теперь в промышленности применяются ограниченно, в нефтехимической промышленности основной способ получения бутадиена — дегидрирование бутана на оксидных алюмохромовых катализаторах либо его пиролиз:
Применение
- Полимеризацией бутадиена получают синтетические каучуки.
- Сополимеризацией бутадиена с акрилонитрилом и стиролом получают АБС-пластик.
См. также
Примечания
Литература
- Абляционные материалы — Дарзана // Химическая энциклопедия в 5 томах. — М.: Большая Российская Энциклопедия, 1988. — Т. 1. — 623 с.


![{\displaystyle {\mathsf {CH_{3}{\text{-}}CH_{2}{\text{-}}CH_{2}{\text{-}}CH_{3}{\xrightarrow[{}]{Cr_{2}O_{3}}}CH_{2}{\text{=}}CH{\text{-}}CH{\text{=}}CH_{2}+2H_{2}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/61562c980b77d2133e89d7f2ff7d853ce4784be1)