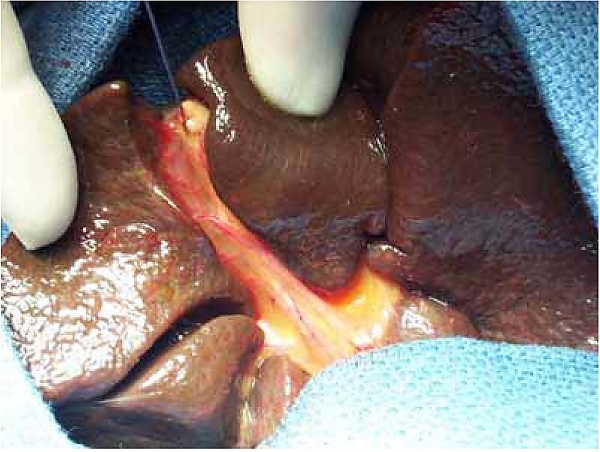
Билиарная атрезия
Билиа́рная атрези́я (БА; атрези́я желчевыводя́щих путе́й) — редкое деструктивное воспалительное заболевание, при котором прогрессирующий фиброз билиарного дерева у ребёнка приводит к обструкции желчных протоков и последующему циррозу печени. При отсутствии лечения прогрессирующий цирроз печени заканчивается летальным исходом к двум годам[3].
Общие сведения
История
В 1817 году БА впервые описана как неизлечимое состояние. В 1928 году выполнена первая успешная операция при корригируемом типе БА. Для некорригируемого типа различные хирургические попытки до конца 1950-х годов успеха не имели. В 1957 году Морио Касаи впервые выполнил портоэнтеростомию при некорригируемом типе, что стало началом современной хирургии этого заболевания. В 1960-х годах метод опубликован в международных журналах, поначалу встречен со скепсисом, но к концу 1970-х годов признан во всём мире стандартом лечения. С начала 1980-х годов благодаря новым схемам иммуносупрессии активно развивается трансплантация печени, которая становится резервным методом при неэффективности операции Касаи. С конца 1980-х годов получила развитие трансплантация от живого родственника, особенно в Японии. В 1990-е годы сложные реконструктивные методы и повторные операции Касаи были в значительной степени оставлены из-за их негативного влияния на исходы будущей трансплантации[4].
Классификация
Существуют три типа БА в зависимости от уровня поражения[3]:
- тип I — обструкция общего желчного протока (непроходимость на уровне общего желчного протока). Составляет около 5 % случаев;
- тип II — обструкция на уровне общего печёночного протока. Составляет около 2 % случаев;
- тип III — обструкция на уровне ворот печени.
Выделяют следующие формы БА[3]:
- несиндромальная БА;
- синдромальная БА — сочетается с дефектами латерализации и аномалиями селезёнки, около 10 % случаев;
- БА с другими пороками развития — имеется по крайней мере один дополнительный порок развития, но без дефектов латерализации и аномалий селезёнки.
Фенотипическая классификация БА[5]:
- синдром БА с аномалиями селезёнки — около 10 %. Характеризуется дефектами латерализации, сосудистыми аномалиями (предуоденальная воротная вена, прерванная нижняя полая вена), пороками сердца и кишечной мальротацией;
- БА, ассоциированная с пороками сердца, — отдельная прогностическая подгруппа, определяемая наличием значимых структурных аномалий сердца (например, дефекты перегородок, тетрада Фалло). Эти случаи могут включать или не включать другие признаки синдрома БА с аномалиями селезёнки и связаны с худшими исходами;
- другие синдромальные ассоциации — редкие связи с синдромом кошачьего глаза и синдромом Кабуки;
- кистозная БА — около 10 %. Характеризуется кистозным расширением в воротах печени;
- БА, положительная по IgM к цитомегаловирусу, — отдельный воспалительный подтип с худшим прогнозом;
- изолированная БА — около 70 %. Наиболее распространённая форма, без врождённых аномалий, имеет многофакторную этиологию.
Этиология
Достоверные этиологические факторы БА не установлены. Однако заболевание не выявляется у мертворождённых и недоношенных детей, что говорит о его развитии на поздних сроках гестации. К возможным факторам развития БА относятся[5][6]:
- внутриутробная инфекция: ни один отдельный агент не идентифицирован как причина БА. Цитомегаловирус выявлен почти у 25 % больных, но ещё чаще встречается при идиопатическом неонатальном гепатите, что подтверждает концепцию единого патологического спектра (инфантильная обструктивная холангиопатия). Исследования реовируса типа 3 дали противоречивые результаты. Материнские кишечные и мочеполовые инфекции в третьем триместре беременности значительно повышают риск развития билиарной атрезии у младенца;
- генетические факторы: фетальная и перинатальная формы, часто ассоциированные с другими желудочно-кишечными и сердечными аномалиями, предполагают нарушение онтогенеза. У мышей выявлены специфические мутации в генах C-JUN (протоонкогенный транскрипционный фактор) и генах семейства гомеобокс. Недостаточная экспрессия белка SOX17 в эпителии желчного пузыря и желчных протоков у мышей приводит к БА. В исследовании на людях показано, что БА ассоциирована с распространёнными и редкими мутациями в 102 генах, участвующих в цилиогенезе и полярности клеток;
- другие причины: нарушения синтеза жёлчных кислот являются одной из возможных причин развития БА. Жёлчные кислоты почти наверняка способствуют повреждению гепатоцитов и желчных протоков, однако их первичная роль в развитии БА не установлена. Чётких корреляций с тератогенами и иммунологическими факторами не определено.
Патогенез
БА рассматривается как результат повреждения, происходящего внутриутробно, и последующего ответа на это повреждение, который разворачивается как в пренатальном, так и в постнатальном периодах. К факторам, способствующим начальному повреждению, относятся генетические аномалии, воздействие инфекционных агентов и токсинов, а также врождённая возрастная уязвимость внепечёночных желчных протоков новорождённого. Ключевую роль в патогенезе играет нарушенный иммунный ответ. У генетически предрасположенного ребёнка повреждение желчных протоков запускает каскад неадекватных реакций как врождённого, так и адаптивного иммунитета. В процесс вовлекаются Т-клетки, В-клетки, естественные киллеры, макрофаги и нейтрофилы, которые вместо восстановления тканей вызывают прогрессирующее воспаление и аутоиммунное повреждение холангиоцитов. Дополнительный вклад вносит дисфункция регуляторных Т-клеток, что приводит к потере толерантности к собственным антигенам. Параллельно развивается патологическое рубцевание с изменением состава внеклеточного матрикса, отложением коллагена и β-амилоида. Итогом такого сочетания повреждающих факторов и неадекватного воспалительно-репаративного ответа становится прогрессирующий фиброз и облитерация желчных протоков, что клинически проявляется обструкцией желчеоттока и развитием цирроза печени. Таким образом, патогенез билиарной атрезии представляет собой единый континуум: от пренатального повреждения желчных путей через постнатальную иммунную дисрегуляцию к необратимому фиброзу и печёночной недостаточности[7].
К типичным гистологическим находкам при БА относятся расширение портальных трактов с различной степенью фиброза, выраженная пролиферация желчных протоков, наличие желчных пробок в просвете протоков, каналикулярный и гепатоцеллюлярный холестаз, а также смешанная воспалительная клеточная инфильтрация. По мере прогрессирования заболевания эти изменения могут эволюционировать в мостовидный фиброз и сформировавшийся билиарный цирроз. Среди всех этих признаков пролиферация желчных протоков считается одним из наиболее характерных гистопатологических проявлений БА[5].
Эпидемиология
БА — редкое заболевание, встречающееся в большинстве этнических групп с разной частотой. В западных странах распространённость составляет от 1 на 14 000 до 1 на 22 000 живорождённых. В Восточной Азии распространённость выше — от 1 на 5000 до 1 на 9000. В Новой Зеландии у населения маори распространённость составляет 1 на 5000, а у детей европейского происхождения — 1 на 16 000. Распространённость выше у женщин, соотношение риска — примерно 1,4 в большинстве западных и азиатских стран, достигая 1,8 в Японии[7].
Диагностика
Независимо от этиологии, клиническая картина неонатального холестаза при БА у большинства детей сходна. Типичные симптомы включают желтуху различной степени выраженности, тёмную мочу и светлый стул. При БА большинство детей доношенные, хотя может наблюдаться более высокая частота низкой массы тела при рождении. В большинстве случаев ахоличный стул отмечается не с рождения, а развивается в течение первых нескольких недель жизни. Аппетит, рост и прибавка веса могут оставаться нормальными[6].
При физикальном обследовании нет патогномоничных признаков. Гепатомегалия может определяться рано, печень часто плотная или твёрдая при пальпации. Спленомегалия встречается часто, что указывает на прогрессирующий цирроз с портальной гипертензией. У некоторых пациентов в эпигастрии может пальпироваться срединно расположенная печень. Наличие сердечных шумов указывает на ассоциированные пороки сердца[6].
Биохимический анализ крови: характерно повышение концентрации прямого и непрямого билирубина, повышение активности щелочной фосфатазы, гамма-глутамилтрансферазы, аспартатаминотрансферазы и аланинаминотрансферазы[6].
Иммуноферментный анализ: возможно повышение активности биомаркера матриксной металлопротеиназы 7-го типа в крови[5].
Гистологическое исследование биоптата печёночной ткани: позволяет выявить характерные фибротические изменения печени[7].
Ультразвуковое исследование: к возможным находкам относятся отсутствие или гипоплазия желчного пузыря и отсутствие постпрандиального сокращения желчного пузыря. Симптом треугольного тяжа, представляющий собой эхогенный фиброзный остаток в воротах печени, обладает высокой специфичностью, но вариабельной чувствительностью и заметной межиндивидуальной вариабельностью. Антенатальное исследование позволяет выявлять аномалии желчного пузыря при синдромальных формах[5].
Гепатобилиарная сцинтиграфия с использованием производных иминодиуксусной кислоты, меченных технецием, позволяет оценить желчевыделение. Выведение индикатора в кишечник с высокой достоверностью исключает билиарную атрезию[5].
Эндоскопическая ретроградная холангиопанкреатография: метод позволяет напрямую визуализировать анатомию желчевыводящих путей и подтвердить или исключить БА[5].
Магнитно-резонансная томография и магнитно-резонансная холангиопанкреатография обеспечивают детальную неинвазивную визуализацию желчевыводящих путей и паренхимы печени[5].
Дифференциальная диагностика
Дифференциальная диагностика БА проводится со следующими заболеваниями[5][6]:
- синдром Алажилля;
- дефицит альфа-1-антитрипсина;
- TORCH-синдром;
- болезнь Кароли;
- идиопатический неонатальный гепатит;
- нарушения метаболизма липидов;
- болезнь Байлера;
- холестаз;
- галактоземия (дефицит галактозо-1-фосфат-уридилилтрансферазы);
- врождённые нарушения синтеза жёлчных кислот;
- неонатальный гемохроматоз;
- краснуха;
- муковисцидоз;
- неонатальный сифилис;
- токсоплазмоз.
Осложнения
К возможным осложнениям БА относятся[5]:
- холангит;
- портальная гипертензия;
- кровотечения из варикозно расширенных вен пищевода и желудка;
- асцит;
- внутрипечёночные билиарные кисты («жёлчные озёра»);
- гепатопульмональный синдром;
- малигнизация (развитие гепатоцеллюлярной карциномы и холангиокарциномы).
Лечение
Единственным эффективным методом лечения БА является хирургический. Стандартная операция — портоэнтеростомия по Касаи с формированием петли по Ру, которая заключается в иссечении фиброзного остатка внепечёночных желчных протоков и наложении анастомоза между воротами печени и тощей кишкой. Открытая операция остаётся предпочтительным методом в крупных центрах. В послеоперационном периоде широко применяется урсодезоксихолевая кислота. Трансплантация печени является окончательным методом лечения при неэффективности операции Касаи или развитии декомпенсированного цирроза. Показания включают персистирующий холестаз, рецидивирующий холангит, портальную гипертензию, задержку роста и печёночную недостаточность. Современная стратегия рассматривает оба метода как взаимодополняющие: сначала выполняется своевременная операция Касаи для максимального продления жизни нативной печени, а при прогрессировании заболевания проводится раннее направление на трансплантацию[5][6].
Прогноз
Прогноз при БА определяется прежде всего возрастом выполнения операции Касаи: оптимальным считается возраст до 8—10 недель жизни, что значительно снижает риск необходимости ранней трансплантации печени. Частота достижения желчеоттока после операции составляет 60—80 %, а бестрансплантационная выживаемость через 1 и 2 года — 53,7 и 46,7 % соответственно. У трети пациентов желчеотток оказывается недостаточным, и они нуждаются в трансплантации печени в возрасте до двух лет[6].
Диспансерное наблюдение
Профилактика
Неонатальный скрининг БА проводится посредством информирования родителей и раздачи им цветовых карточек стула с последующей оценкой при бледном стуле. Применение цветовых карточек стула привело к более ранней диагностике БА и улучшению выживаемости нативной печени. Эффективные методы профилактики заболевания не разработаны[7].
Примечания
Литература
- Волынец Г. В., Хавкин А. И., Никитин А. В. Современный взгляд на билиарную атрезию у детей // Экспериментальная и клиническая гастроэнтерология. — 2020. — № 1 (173). — С. 40—55. — doi:10.31146/1682-8658-ecg-173-1-40-55.
- Tam P. K. H., Wells R. G., Tang C. S. M., et al. Biliary atresia (англ.) // Nature Reviews Disease Primers. — 2024. — Vol. 10. — P. 47. — doi:10.1038/s41572-024-00533-x.
- Nio M., Ohi R. Historical Overview of Biliary Atresia (англ.). — Springer, 2021. — ISBN 978-981-16-2160-4. — doi:10.1007/978-981-16-2160-4_1.