Синдром Конради — Хюнермана
Синдро́м Ко́нради — Хю́нермана (Х-сце́пленная домина́нтная то́чечная хондродисплази́я) — редкое наследственное заболевание с Х-сцепленным доминантным типом наследования, обусловленное мутациями в гене EBP, нарушающими синтез холестерина. Клиническая картина отличается выраженным полиморфизмом: от тяжёлых пороков развития, приводящих к внутриутробной гибели плода, до стёртых форм без заметных нарушений. Типичными проявлениями синдрома являются хондродисплазия с точечными обызвествлениями эпифизов, позвонков, трахеи и рёбер, асимметричное укорочение конечностей, сколиоз и задержка роста[1][2][3].
Что важно знать
История
Синдром Конради — Хюнермана впервые был описан немецким педиатром Эрихом Конради, ассистентом детской клиники в Кёльне, в 1914 году. В 1931 году Карл Хюнерман, также работавший ассистентом в кёльнской детской клинике, представил более подробное клиническое описание заболевания, уточнив спектр симптомов и характер наследования[4]. В 1979 году немецкий дерматовенеролог Рудольф Хаппле опубликовал серию статей, в которых систематизировал данные о клинических проявлениях, особенностях наследования и патогенетических механизмах болезни[1][5].
Этиология
Этиология синдрома Конради — Хюнермана связана с мутациями в гене EBP, расположенном на Х‑хромосоме. Этот ген кодирует фермент 3-бета-гидроксистероид-8,7-изомераза, участвующий в финальных этапах биосинтеза холестерина. Патогенные варианты могут возникать спорадически или наследоваться по Х‑сцепленному доминантному типу. Заболевание встречается преимущественно у женщин, что объясняется наличием у них двух Х‑хромосом. У мужчин, обладающих одной Х‑хромосомой, мутации в гене EBP обычно приводят к тяжёлым формам заболевания, часто несовместимым с жизнью и приводящим к внутриутробной гибели[1].
Патогенез
При синдроме Конради — Хюнермана патологические процессы обусловлены сбоями в заключительных стадиях синтеза холестерина. Дефект фермента 3-бета-гидроксистероид-8,7-изомеразы приводит к накоплению промежуточных соединений стерольного ряда, таких как 8-дегидрохолестерол и 8(9)-холестенол, обладающих токсическим действием. Недостаток холестерина нарушает молекулярные механизмы межклеточной сигнализации, что отражается на процессах развития конечностей плода[1][6].
Эпидемиология
Синдром Конради — Хюнермана относится к редким наследственным заболеваниям. Распространённость варьирует от от 1 случая на 100 000—200 000 новорождённых до 1 случая на 400 000 новорождённых. Заболевание преимущественно поражает лица женского пола. Более чем в 95 % случаев синдром диагностируется у девочек, что связано с Х‑сцепленным доминантным типом наследования[1][7].
Диагностика
Синдром Конради — Хюнермана характеризуется значительной вариабельностью проявлений. У части новорождённых отмечается недостаточная прибавка массы тела и роста, что в дальнейшем может приводить к низкорослости во взрослом возрасте. У некоторых детей наблюдается склонность к рецидивирующим инфекциям[1].
Костные изменения являются наиболее типичными. У новорождённых выявляются множественные участки кальцификации в зонах роста трубчатых костей и других хрящевых структурах скелета. Кальцификаты могут локализоваться в позвоночнике, костях таза, передних концах рёбер, грудине, лопатках, ключицах, а в редких случаях — в гортани и трахее. Часто определяется асимметричное укорочение длинных трубчатых костей, преимущественно плечевых и бедренных, что приводит к диспропорции конечностей, обычно более выраженной с одной стороны. Наблюдаются искривления позвоночника в виде сколиоза или кифосколиоза. В отдельных случаях формируются контрактуры суставов, ограничивающие их подвижность. Описаны дисплазия тазобедренных суставов и косолапость[1].
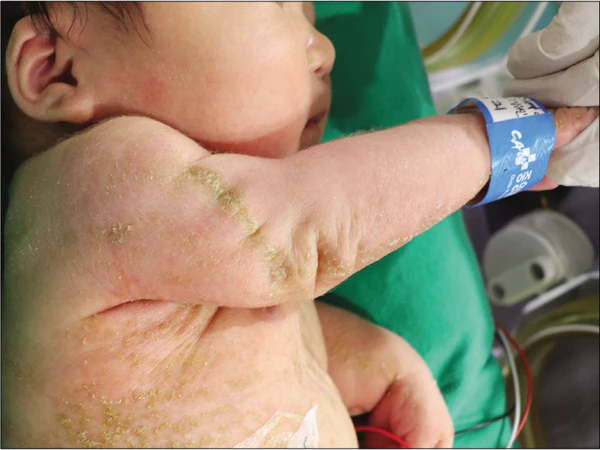
Характерные внешние признаки включают выступающий лоб, уплощённые скуловые кости, низкую переносицу, вздёрнутые ноздри и диспластичные ушные раковины. В ряде случаев отмечается нарушение слуха. Кожные проявления в неонатальном периоде включают эритему и ихтиозиформную эритродермию с утолщением, сухостью и шелушением кожи. Обычно они регрессируют в младенческом возрасте, однако позже может развиваться фолликулярная атрофодермия с формированием крупных пор. Возможны участки гипопигментации и гиперпигментации, а также рубцовая алопеция с очаговым выпадением волос. Сохраняющиеся волосы часто бывают редкими, жёсткими и тусклыми[1].
В некоторых случаях встречаются сужения гортани и трахеи, короткая шея, а также дистрофия ногтей (платонихия, онихошизия)[1][6].
- Биохимический анализ крови — выявляется повышение концентрации 8(9)-холестенола и 8-дегидрохолестерола[1].
- Гистологическое исследование биопсийного материала кожи — выявляется фолликулярный гиперкератоз с отложением солей кальция в устьях волосяных фолликулов[1][8].
- Молекулярно-генетическое исследование — секвенирование гена EBP для выявления патогенных вариантов[1].
- Рентгенологическое исследование — определяется наличие мелких, обычно правильно сгруппированных кальцификатов в хрящевых отделах скелета, особенно выраженные в эпифизах длинных костей, что формирует характерную картину «пунктирных эпифизов»[2].
Дифференциальная диагностика
- CHILD — синдром (врождённая гемидисплазия с ихтиозиформным невусом и дефектами конечностей);
- Аутосомно-доминантная точечная хондродисплазия;
- Дисплазия Гринберга;
- Варфариновая эмбриопатия;
- Аутоиммунные заболевания матери;
- Синдром Кейтеля;
- Ризомелическая точечная хондродисплазия;
- Синдром Смита — Лемли — Опица;
- Синдром Антли — Бикслера;
- Десмостеролоз;
- Латостеролоз;
- Дефицит стерол‑С4‑метилоксидазоподобного фермента;
- Эпифизарные некрозы;
- Врождённый сифилис;
- Синдрома Герена — Стерна;
- Синдром Цельвегера.
Лечение
Терапия синдрома Конради — Хюнерманна является симптоматической. Ведение пациентов требует мультидисциплинарного подхода с участием педиатров, ортопедов, дерматовенерологов, оториноларингологов, генетиков и других профильных врачей[1].
Ортопедическая помощь включает хирургические вмешательства при сколиозе, асимметрии конечностей, краниофациальных аномалиях и других скелетных деформациях. Объём и характер операций определяются тяжестью и сочетанием анатомических нарушений, а также выраженностью клинических проявлений. При нарушении слуха проводится стандартное лечение по показаниям оториноларинголога с последующим подключением реабилитационных и образовательных программ для детей. Дерматологическое лечение направлено на смягчение проявлений ихтиоза и других кожных изменений. Рекомендуется регулярное применение смягчающих и кератолитических средств, позволяющих поддерживать гидролипидный барьер и эластичность кожи. Респираторные осложнения, возникающие на фоне выраженного сколиоза, требуют наблюдения и терапии у пульмонолога[1][3].
Прогноз
Прогноз при синдроме Конради — Хюнермана определяется выраженностью скелетных деформаций и их влиянием на функцию жизненно важных органов. У пациентов с лёгкими формами заболевания продолжительность жизни соответствует среднестатистической, при условии сохранности сердечно-лёгочной функции и отсутствия тяжёлых деформаций позвоночника, в частности выраженного сколиоза, который может приводить к развитию дыхательной недостаточности и кардиальных осложнений. Когнитивные функции и интеллект у большинства пациентов с данным синдромом обычно не нарушаются[1][9].
Профилактика
Специфических мер профилактики синдрома Конради — Хюнермана не разработано. Основное значение имеет медико-генетическое консультирование семей, в которых выявлен данный синдром[3][10].
Диспансерное наблюдение
Пациентам с подтверждённым диагнозом рекомендуется регулярное наблюдение у профильных специалистов. Дерматологическое наблюдение необходимо для оценки выраженности ихтиоза и других кожных изменений. Ортопедическое обследование проводится с целью своевременного выявления и коррекции сколиоза, контрактур и нарушений роста конечностей. Консультации офтальмолога позволяют своевременно диагностировать катаракту, аудиологическое обследование показано при подозрении на нарушения слуха. При наличии изменений со стороны мочевыделительной системы целесообразно регулярное ультразвуковое исследование почек. Пациентам с кожными проявлениями рекомендуется адекватная фотозащита, так как длительное пребывание на солнце может приводить к перегреванию и обезвоживанию[3][10].
Примечания
Литература
- Kumble S., Savarirayan R. Chondrodysplasia Punctata 2, X-Linked // GeneReviews. — 2020. — 1 сентября.
- Happle R. X-Linked dominant chondrodysplasia punctata // Human Genetics. — 1979. — Т. 53, вып. 1. — С. 65–73. — ISSN 1432-1203 0340-6717, 1432-1203.
- Kolb-Mäurer A., Grzeschik K. H., Haas D., Bröcker E. B., Hamm H. Conradi-Hünermann-Happle Syndrome (X-linked Dominant Chondrodysplasia Punctata) Confirmed by Plasma Sterol and Mutation Analysis // Acta Dermato-Venereologica. — 2008. — Т. 88, вып. 1. — С. 47–51. — ISSN 0001-5555.
- Алиев Р. Р., Раджабов Х. М., Погосян А. С. Синдром конради-хюнермана у девочки // Российский педиатрический журнал. — 2022. — № 6.
- Meshram R. M., Dandale A. A., Rohadkar L. A., Chirag R. N. Conradi–Hunermann syndrome: A rare case of chondrodysplasia punctata // Indian Journal of Pediatric Dermatology. — 2019. — Т. 20, вып. 3. — С. 255. — ISSN 2319-7250.
- Jesus S., Costa A. R., Almeida M., Garrido P., Alcafache J. Conradi-Hünerman-Happle Syndrome and Obsessive–Compulsive Disorder: a clinical case report // BMC Psychiatry. — 2023. — Т. 23, вып. 1. — ISSN 1471-244X.