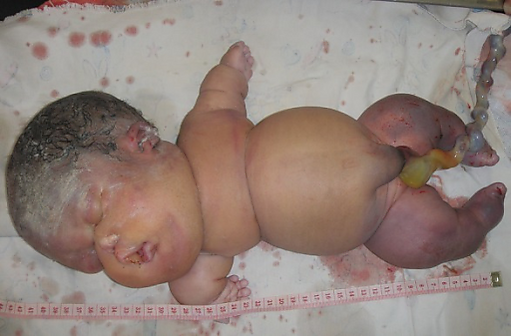
Дисплазия Гринберга
Дисплазия Гринберга (водянка-эктопическая кальцификация-изъеденная молью дисплазия скелета) — это редкая аутосомно-рецессивная остеохондродисплазия, характеризующаяся выраженной внутриутробной водянкой, выраженным укорочением всех длинных костей с рентгенологическим эффектом изъедения молью, платиспондилией, дезорганизацией костно-хрящевой кальцификации и очагами эктопического окостенения. Это состояние приводит к внутриутробной гибели плода. В фибробластах пациентов повышен уровень холестаза-8,14-диен-3-бета-ола, что указывает на нарушение метаболизма стеролов[1][2][3].
Общие сведения
История
Гринберг и соавторы в 1988 году описали случай двух сиблингов, потомков родителей, приходившихся друг другу кровными родственниками. У плодов была явно «новая» тяжёлая форма карликовости с короткими конечностями. Хрящевые и гистологические признаки были специфическими. Первый брат появился на 30 неделе беременности с тяжёлой водянкой после смерти плода; второй был обнаружен с помощью ультрасонографии на 20 неделе. Рентгенологические отклонения включали необычный вид костей, как будто они «изъедены молью», заметное укорочение длинных трубчатых костей, причудливые эктопические центры окостенения и выраженную платиспондилию с необычными центрами окостенения. У обоих плодов был обнаружен обширный экстрамедуллярный эритропоэз. Хрящевая гистология характеризовалась выраженной дезорганизацией с вкраплёнными массами хрящевой, костной и мезенхимальной ткани. Первый плод был мужского пола, второй — женского. Родители были троюродными братом и сестрой греческого происхождения[2].
Шпрангер и Марото в 1990 году сообщили о третьем случае ассоциации водянки плода с эктопическими кальцификациями и «изъеденной молью» скелетной дисплазией[4].
Читаят и соавторы в 1993 году сообщили о четвёртом случае у потомка близкородственных родителей восточноиндийского происхождения. Рентгенологические изменения включали платиспондилию с множественными дополнительными центрами окостенения, внешнюю кальцификацию в рёбрах, грудине, тазу и эпифизах, а также кости, имеющие вид "изъеденных молью". Гистопатологические изменения включали хондроциты с расширенным шероховатым эндоплазматическим ретикулумом и включениями с гомогенным материалом промежуточной электронной плотности[5].
Хорн и соавторы в 2000 году описали несколько нескелетных пороков развития при дисплазии Гринберга: омфалоцеле, порок развития кишечника, аномальные ногти и гиполобулярные лёгкие[6].
Трайковски и соавторы. в 2002 году сообщили о пренатальной ультразвуковой диагностике случая дисплазии Гринберга у плода мужского пола некровнородственной македонской пары. При ультразвуковом исследовании были отмечены многоводие, водянка плода, сильно укороченные конечности и кистозная гигрома. После прерывания беременности рентгенологическое исследование показало типичные признаки дисплазии Гринберга. У плода была большая голова с вдавленной переносицей, гипоплазией средней части лица и выступающими глазничными дугами. Световое микроскопическое исследование рёбер и длинных костей показало серьёзную дезорганизацию, отсутствие формирования хрящевых столбов и резкий переход от хряща к нормальной кости[7].
Оффиа и соавторы в 2003 сообщили о плоде, зачатом от неродственных родителей европеоидной расы, с дисплазией Гринберга. Пренатальное ультразвуковое исследование на 14 неделе беременности показало тяжёлую микромелию, и беременность была прервана. Вскрытие показало маленькую грудную клетку, гепатомегалию, сильно укороченные конечности и постаксиальную гексадактилию верхних конечностей. Дисморфические признаки включали большой лоб, лёгкую рецессию нижней челюсти, уплощённый нос и лёгкий гипертелоризм. Гистологическое исследование костей показало дезорганизацию пластинки роста без образования столбиков хондроцитов, но случайный, резкий переход между хрящом и костью. Рентгенологическое исследование показало, что длинные трубчатые кости чрезвычайно укорочены и имеют вид "изъеденных молью", а также значительную платиспондилию. Были обнаружены признаки эктопической кальцификации. Биохимический анализ мышечной ткани показал повышенный уровень 8,14-холестадиен-2-бета-ола[8].
Константиниду и соавторы в 2008 году сообщили о плоде, зачатом от кровнородственных греческих родителей, с дисплазией Гринберга. Пренатальное УЗИ на 11 неделе беременности показало аномальный плод с водянкой, микромелией, узкой грудной клеткой и гепатомегалией. Рентгенологическое исследование показало, что кости имеют вид "изъеденных молью". Световая микроскопия показала полную оссификацию диафиза бедренной кости и аномальные гетеротопические центры окостенения в позвонках и длинных костях. Метафизальная зона роста практически отсутствовала, с резким переходом от хряща к минерализованной гипоцеллюлярной кости. Была история 2 ранее поражённых плодов, обнаруженных пренатальным УЗИ. Вскрытие одного из этих плодов показало водянку плода, тяжёлое ризомелическое и мезомелическое укорочение всех длинных костей, макроцефалию, низко посаженные уши, гипертелоризм, вдавленную переносицу, узкую грудную клетку и постаксиальную полидактилию стоп. Рентгенологическое исследование показало, что кости имеют вид "изъеденных молью". Световая микроскопия показала дезорганизацию хрящевого столба и эктопическую кальцификацию[3].
Верле и соавторы в 2018 году описали плод мужского пола от кровнородственных турецких родителей. Беременность была прервана на 21 неделе и 5 днях из-за задержки внутриутробного развития и тяжёлой микромелии. Осмотр плода выявил короткую шею и туловище, узкую грудную клетку, выступающий живот и водянку. Рентгенограммы показали сильное снижение окостенения черепа, грудной клетки и конечностей. Наблюдалось сильное укорочение и расширение трубчатых костей. Окостенение позвоночника, ножек и крестца было нарушено. Лопатки были гипопластичными, а лобковые кости были недоокостенелыми. Рентгенограмма не вывила типичных отклонений длинных костей, эктопические кальцификаты также отсутствовали. Клинические и рентгенологические признаки соответствовали диагнозу ахондрогенеза-1A (200600)[9].
Джорджио и соавторы 2019 описали 2 плода с дисплазией Гринберга от родственных друг другу марокканских родителей. У обоих плодов наблюдалась водянка плода и тяжёлая микромелия. У первого плода были дисморфические черты лица (лобные бугры, микрогнатия, тяжёлая гипоплазия носа и средней части лица), узкая грудная клетка, выступающий живот с асцитом, неоднозначные гениталии и короткие пальцы с двусторонней постаксиальной гексадактилией. Рентгенограммы показали задержку и перекос окостенения, гипоплазию рёбер и укороченные, перекошенные и смещённые кости. У второго плода была тяжёлая гипоплазия носа и средней части лица, низко посаженные дисморфические уши, гипопластическая грудная клетка и женские гениталии. Рентгенограммы показали глобальную гипоминерализацию, узкую грудную клетку с короткими гипопластическими рёбрами, недостаточную оссификацию позвоночника с платиспондилией и перекошенные длинные кости с сильно укороченными и изогнутыми диафизами. Рентгенологические признаки длинных трубчатых костей и эктопические кальцификаты не описаны. Гистологическое исследование костей и хрящей показало серьёзное нарушение развития хрящевой ткани. У родителей поражённых плодов не было выявлено аномалии Пельгера-Хьюэта[10].
Этиология
Характер передачи дисплазии Гринберга в семьях, случаи которых описали Гринберг, Читаят и другие авторы, соответствовал аутосомно-рецессивному типу наследования[11].
Уотерхэм и др. в 2003 провели химические и молекулярные исследования клеток плода с гемоскелетной дисплазией. Плод был получен от здоровых кровнородственных родителей турецкого происхождения, у которых на 17-й неделе беременности при ультразвуковом исследовании плода, проведённом 24-летней матери, была выявлена задержка внутриутробного развития. У плода была сильная водянка и дисплазия скелета с характерным укорочением конечностей. Исследование околоплодных вод показало кариотип 46,XY. Внутриутробная смерть наступила на 18 неделе беременности, и роды были индуцированы. Вскрытие плода показало сильную отёчность, чрезвычайно короткие отёчные конечности и постаксиальную полидактилию на обеих кистях. Рентгенологическое исследование показало выраженную плоскостопие, короткие рёбра неправильной формы, имеющие вид «изъеденных молью» лопаточные и тазовые кости, а также очень короткие трубчатые кости с угловатыми диафизами. Уотерхэм и соавторы обнаружили повышенные уровни холеста-8,14-диен-3-бета-ола в культуре фибробластов кожи, что соответствует дефициту фермента биосинтеза холестерина 3-бета-гидроксистерол дельта(14)-редуктазы. Анализ последовательностей 2 генов-кандидатов, кодирующих предполагаемые стерол-дельта(14)-редуктазы человека, TM7SF2 (603414) и LBR, выявил гомозиготность по замене на 7 п.о. в экзоне 13 гена LBR (600024.0003), что привело к образованию усечённого белка. Функциональная комплементация гемоцитов путём трансфекции контрольной кДНК LBR подтвердила, что LBR кодирует дефектную стерин-дельта(14)-редуктазу. У здоровой матери в 60 % гранулоцитов были обнаружены гиполобулированные ядра. Уотерхэм и др. предположили, что классическая аномалия Пелгера-Хьюэта (PHA; 169400), которая также вызвана мутацией в гене LBR, представляет собой гетерозиготное состояние с дефицитом 3-бета-гидроксистерол дельта(14)-редуктазы[12].
У плода, зачатого от кровнородственных родителей греческого происхождения, с гемоскелетной дисплазией, Константиниду и др. выявили гомозиготную миссенс-мутацию в гене LBR (N547D; 600024.0008)[3].
У 3 неродственных плодов с гемоскелетной дисплазией Клейтон и соавт. в 2010 выявили гомозиготные или сложные гетерозиготные мутации в гене LBR (600024.0008-600024.0011)[13]. Один из плодов был описан в работе Оффия и др.[8]. У родителей, которые были гетерозиготны по миссенс-мутации в домене стеролредуктазы, не было аномалий в клетках периферической крови, в то время как было показано, что эта миссенс-мутация приводит к потере активности стеролредуктазы. Клеточные исследования показали локализацию LBR за пределами ядерной мембраны, где он взаимодействует с маркерами эндоплазматического ретикулума. Неядерный LBR также экспрессировался в лимфобластоидных клетках, дифференцированных остеокластах и клетках остеосаркомы, а также в различных тканях развивающихся мышиных эмбрионов. Эти данные позволили Клейтону и соавт. предположить, что гемоскелетная дисплазия является результатом дефектов в стеролредуктазной активности LBR, а не структурной функции LBR как части ядерной мембраны. Разобщение метаболических и структурных функций LBR объяснило, как мутации в одном и том же гене могут вызывать различные нарушения. Полученные данные также показали, что функция стеролредуктазы имеет важное значение для внутриутробного развития человека[13].
У плода с предполагаемым диагнозом ахондрогенеза-1А (200600) Верле и соавт. (2018) провели секвенирование по Сэнгеру гена TRIP11 (604505) и не продемонстрировали молекулярного подтверждения клинического и рентгенологического диагноза. Затем они провели секвенирование всего экзома и идентифицировали новую гомозиготную мутацию сайта сплайсинга в гене LBR (600024.0019). Мутация, которая была подтверждена с помощью секвенирования по Сэнгеру, была обнаружена в гетерозиготном состоянии у незатронутых родителей. МРНК LBR в фибробластах, полученных от пациентов, была едва обнаружима с помощью ПЦР в реальном времени, что соответствовало нонсенс-опосредованному распаду. Вестерн-блот-анализ и иммунофлуоресценция показали, что эмбриональные клетки были полностью лишены белка LBR[9].
С помощью секвенирования всего экзома у 2 плодов-сиблингов с дисплазией Гринберга Джорджио и соавт. в 2019 идентифицировали гомозиготную миссенс-мутацию в гене LBR (D460R; 600024.0020). Родители были гетерозиготны по этой мутации[10].
Диагностика
Дисплазия Гринберга вызывает аномальное развитие костей плода. Это приводит к тому, что кости имеют вид «изъеденных молью» при осмотре на рентгеновском снимке. Могут возникать микромелия, полидактилия и эктопическая кальцификация, или накопление кальция в мягких тканях тела. У восьмидесяти-девяноста девяти процентов пострадавших будут аномально окостеневшие позвонки, аномальное окостенение костей таза, кальцификация передних рёберных точек и брахидактилия[14].
Вторым определяющим признаком дисплазии скелета, вызванной этим заболеванием, является водянка плода[15].
Пренатальная ультразвуковая диагностика на 20-й неделе беременности обычно выявляет многоводие, водянку плода, сильное укорочение конечностей и кистозную гигрому.
Анализ стеролового профиля может быть полезным диагностическим инструментом и использоваться для пренатальной диагностики, как и молекулярный анализ, если известна мутация в семье[15].
Лечение
Лечение отсутствует. При обнаружении заболевания пренатально, целесообразно прерывание беременности[15].