Танатофорная дисплазия
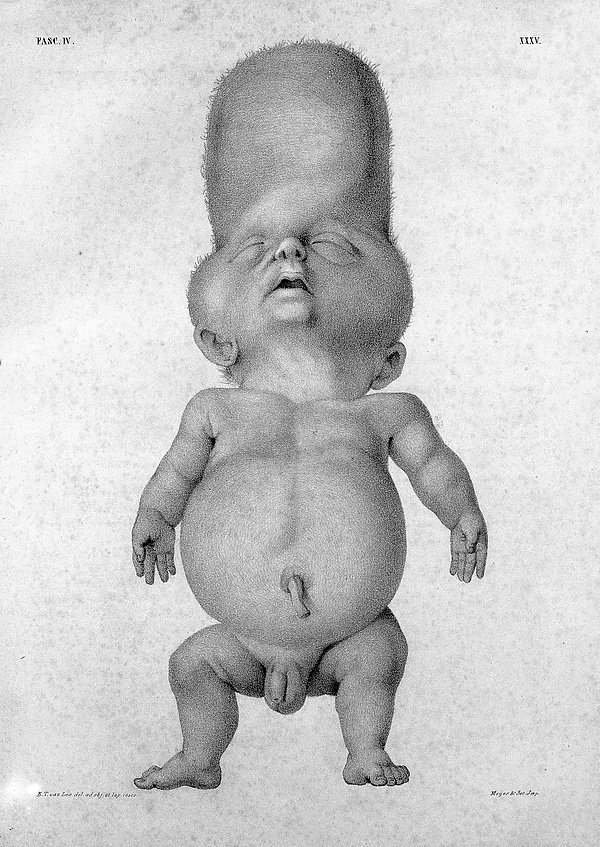
Танатофо́рная дисплази́я (танатофо́рная ка́рликовость) — редкое аутосомно-доминантное заболевание, характеризующееся выраженным укорочением конечностей при нормальной длине туловища, узкой грудной клеткой, укороченными рёбрами, укороченными и расширенными костями таза, а также уплощением тел позвонков. В основе патогенеза заболевания лежат гетерозиготные мутации в гене FGFR3, приводящие к нарушению процессов эндохондрального окостенения. В большинстве случаев танатофорная дисплазия приводит к летальному исходу в перинатальном периоде вследствие тяжёлой дыхательной недостаточности[2][3].
Общие сведения
История
Танатофорная дисплазия впервые была описана К. Майгриером в 1898 году. В 1967 г. П. Марото и М. Лами представили детальное клиническое и рентгенологическое описание заболевания у новорождённых с выраженным укорочением конечностей и узкой грудной клеткой, умерших в первые часы жизни. Для обозначения данной формы хондродистрофии они предложили термин «танатофорная карликовость». В 1971 г. Ж. Гутьер впервые описал церебральные аномалии при танатофорной дисплазии. В 1977 году на Второй международной конференции по номенклатуре скелетных дисплазий термин был изменён на «танатофорная дисплазия»[4]. В 1987 г. В. Лангер предложил классификацию, основанную на морфологии бедренных костей, что позволило выделить тип I и тип II. В 1991 г. был картирован ген FGFR3, а в последующие годы подтверждена его ключевая роль в патогенезе заболевания[2][5].
Классификация
Танатофорная дисплазия подразделяется на два клинических подтипа[3][6]:
- подтип I — характеризуется микромелией с изогнутыми бедренными костями, при этом в отдельных случаях может наблюдаться деформация черепа в виде трилистника различной степени выраженности;
- подтип II — характеризуется микромелией с прямыми бедренными костями и обязательным наличием умеренно или резко выраженной деформации черепа в виде трилистника, обусловленной краниосиностозом.
Этиология
Танатофорная дисплазия обусловлена патогенными вариантами гена FGFR3, кодирующего рецептор фактора роста фибробластов 3, относящийся к семейству рецепторов тирозинкиназы. Этот белок играет ключевую роль в регуляции процессов роста и развития скелета, обеспечивая взаимодействие с лигандами — факторами роста фибробластов — и участвуя в регуляции эндохондрального окостенения. Для танатофорной дисплазии I типа в большинстве случаев характерны миссенс-мутации, приводящие к замене аминокислот на цистеин. Такие замены формируют новые несвязанные остатки цистеина, способствующие димеризации рецептора без участия лиганда[2][3][6].
Танатофорная дисплазия II типа во всех описанных случаях связана с мутацией FGFR3 Lys650Glu, расположенной в петле активации тирозинкиназного домена[2][3].
Патогенез
В основе патогенеза танатофорной дисплазии лежит конститутивная активация рецептора фактора роста фибробластов 3, приводящая к нарушению механизмов регуляции эндохондрального окостенения. Постоянная передача сигнала от FGFR3 при отсутствии связывания с лигандом вызывает преждевременный переход хондроцитов из пролиферативной зоны эпифизарной пластинки в прегипертрофическую стадию. Это сопровождается ускоренной дифференцировкой и истощением пула делящихся клеток, что приводит к резкому замедлению продольного роста трубчатых костей[3][6].
Для танатофорной дисплазии I типа характерна активация внутриклеточных сигнальных каскадов, запускаемых при димеризации рецептора, что усиливает апоптоз хондроцитов и нарушает их упорядоченность в эпифизарной пластинке[3][6].
При танатофорной дисплазии II типа мутация Lys650Glu в петле активации тирозинкиназного домена приводит к особенно высокой тирозинкиназной активности. Этот вариант связан с нарушением созревания FGFR3 и его накоплением в эндоплазматическом ретикулуме. Рецептор в такой форме продолжает передавать сигнал из внутриклеточных компартментов, что дополнительно угнетает пролиферацию и дифференцировку хондроцитов и способствует формированию более тяжёлого клинического фенотипа[3][6].
Эпидемиология
Танатофорная дисплазия является одной из наиболее часто встречающихся форм летальных скелетных дисплазий. Распространённость танатофорной дисплазии оценивается как 1 случай на 20 000-50 000 новорождённых. Тип I регистрируется значительно чаще, чем тип II[2][7].
Диагностика
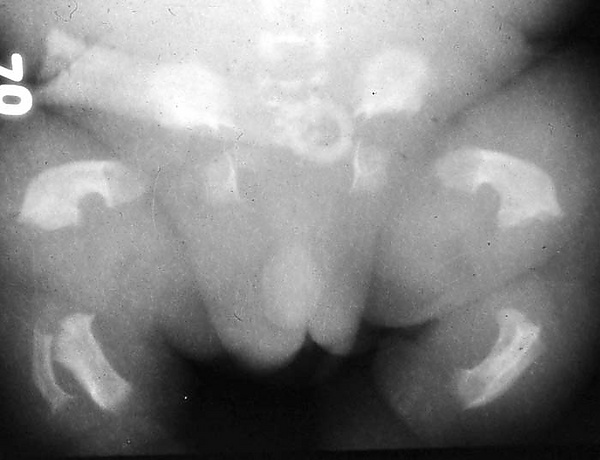
Танатофорная дисплазия проявляется при рождении выраженными диспропорциями скелета и характерными черепно-лицевыми, неврологическими и соматическими особенностями. У новорождённых отмечается относительная макроцефалия с крупным родничком, выступающим лбом, уплощённой переносицей и иногда экзофтальмом. Длина туловища обычно остаётся в пределах нормы, при этом конечности резко укорочены с избыточными кожными складками. Грудная клетка узкая с укороченными рёбрами и выпяченным животом. Пальцы рук короткие. Для I типа характерны изогнутые бедренные кости, для II типа — более прямые бедренные кости и череп в форме трилистника вследствие краниосиностоза[2][6].
У большинства пациентов выявляется генерализованная гипотония. В ряде случаев наблюдается арефлексия[2]. Неврологические осложнения включают сужение большого затылочного отверстия с компрессией ствола мозга, гидроцефалию, мальформации височных долей, судорожный синдром. Наблюдаются тяжёлые задержки психомоторного развития, ограничение моторных функций, поздняя потеря ранее приобретённых навыков[6].
Ведущая причина ранней летальности — дыхательная недостаточность, обусловленная малым объёмом грудной клетки с гипоплазией лёгких и компрессией ствола мозга вследствие узкого большого затылочного отверстия[6].
В отдалённом периоде у выживших пациентов могут развиваться кифоз, остеопения, контрактуры и гипермобильность суставов. Наблюдаются кожные изменения в виде выраженного чёрного акантоза, иногда с развитием себорейных кератозов во взрослом возрасте. У некоторых пациентов встречаются нарушения слуха. Среди редких сопутствующих аномалий — пороки сердца, почечные нарушения, энцефалоцеле, энтеропатия[6].
- Молекулярно-генетическое исследование — направлено на выявление патогенных или вероятно патогенных вариантов в гене FGFR3. Материалом служат ДНК, выделенные из клеток плода, полученных при амниоцентезе или биопсии ворсин хориона[2][6].
- Гистологическое исследование биопсийного материала хрящевой ткани — дезорганизация колонок хондроцитов, снижение пролиферации, латеральный рост метафизов, фиброзные тяжи на периферии метафизов, повышенная васкуляризация зоны покоя хряща[3].
- Пренатальная ультразвуковая диагностика — в I триместре выявляется выраженное укорочение трубчатых костей, макроцефалия, расширение воротникового пространства, гипоплазия грудной клетки, двусторонняя косолапость. Во II—III триместре наблюдается задержка роста, узкая грудная клетка с короткими рёбрами, платиспондилия, вогнутые (по типу «телефонной трубки») бедренные кости, череп в форме трилистника, гидроцефалия, аномалии височных долей, относительная макроцефалия[3][8][9].
- Рентгенологическое исследование — наблюдается ризомелическое укорочение костей, неровные метафизы, платиспондилия, сужение большого затылочного отверстия, вогнутые бедренные кости или клеверообразная форма черепа, признаки компрессии ствола мозга[3][6].
- Магнитно-резонансная томография головного мозга — выявление аномалий головного мозга, включая мальформации височных долей, гидроцефалию, гипоплазию ствола мозга, нарушения миграции нейронов[3][6].
Дифференциальная диагностика
- гомозиготная ахондроплазия;
- синдром Эллиса — ван Кревельда;
- синдром коротких рёбер;
- асфиктическая дисплазия грудной клетки;
- несовершенный остеогенез II типа;
- синдром SADDAN (тяжёлая ахондроплазия с задержкой развития и чёрным акантозом);
- ахондрогенез типов IA, IB и II;
- спондилометафизарная дисплазия, тип Седагатьяна;
- платиспондилярная дисплазия, тип Торранс;
- диссегментальная дисплазия, тип Сильверман — Хандмакер;
- опсисмодисплазия;
- кампомелическая дисплазия;
- гипофосфатазия;
- ризомелическая точечная хондродисплазия.
Лечение
Этиотропной и патогенетической терапии танатофорной дисплазии не существует. Тактика ведения определяется тяжестью состояния и в большинстве случаев направлена на поддержание жизненно важных функций, профилактику и коррекцию осложнений, а также улучшение качества жизни[2].
Симптоматическая терапия включает комплекс мероприятий, реализуемых мультидисциплинарной командой специалистов[6]:
- респираторная поддержка — включая неинвазивную и инвазивную вентиляцию с применением трахеостомии; постоянный мониторинг дыхательной функции, в отдельных случаях — длительное респираторное сопровождение;
- хирургическая коррекция гидроцефалии — установка вентрикулоперитонеального шунта при подтверждённом повышении внутричерепного давления и прогрессировании вентрикуломегалии;
- декомпрессия при сдавлении ствола мозга;
- контроль судорожного синдрома — назначение противоэпилептических препаратов с учётом индивидуальной переносимости;
- использование слуховых аппаратов при тугоухости;
- ортопедическая коррекция при контрактурах, гипермобильности суставов, профилактика вторичных деформаций опорно-двигательного аппарата;
- индивидуальные реабилитационные программы для развития моторных и когнитивных навыков.
Прогноз
Танатофорная дисплазия является преимущественно летальным состоянием, приводящим к смерти в первые часы или дни жизни вследствие тяжёлой дыхательной недостаточности[3]. Основными причинами раннего летального исхода служат гипоплазия грудной клетки и сужение большого затылочного отверстия с компрессией ствола головного мозга. В большинстве случаев прогноз крайне неблагоприятный. Подавляющее число новорождённых погибает в перинатальном периоде. Развитие технологий интенсивной терапии позволило добиться выживания отдельных пациентов. Долгосрочное выживание при танатофорной дисплазии встречается крайне редко[6].
Профилактика
Профилактика танатофорной дисплазии как наследственного заболевания в настоящее время отсутствует. Основным направлением является медико-генетическое консультирование семей с отягощённым анамнезом, а также проведение пренатальной диагностики при выявлении подозрительных признаков на ультразвуковом исследовании плода[6].
Примечания
Литература
- Гамисония А. М. Танатофорная карликовость // ГЕНОКАРТА Генетическая энциклопедия : сайт. — 2020. — 27 апреля.
- Пашук С. Н., Новикова И. В., Лазаревич А. А., Гусина А. А., Венчикова Н. А. Танатофорная дисплазия: поиск частых мутаций гена FGFR3 // Российский педиатрический журнал. — 2022. — Т. 3, № 1. — С. 237.
- Эсетов М. А., Эсетов А.М., Бекеладзе Г. М. Возможности ультразвуковой пренатальной диагностики танатофорной дисплазии // SonoAce Ultrasound. — 2018. — № 31. — С. 7—16.
- Liboi E., Lievens P. Thanatophoric dysplasia // Orphanet encyclopedia. — 2004. — Сентябрь.
- Schultz R., Mayoral É. E. Thanatophoric dysplasia: case report of an autopsy complemented by postmortem computed tomographic study // Autopsy and Case Reports. — 2014. — Т. 4, вып. 2. — С. 35—41. — ISSN 2236-1960.
- French T., Savarirayan R. Thanatophoric Dysplasia // GeneReviews. — 2023. — 18 мая.