Ксенон
Ксено́н (химический символ — Xe, от лат. Xenon) — химический элемент 18-й группы (по устаревшей классификации — главной подгруппы восьмой группы, VIIIA), пятого периода периодической системы химических элементов русского учёного физикохимика Д. И. Менделеева, с атомным номером 54.
Простое вещество ксенон — это тяжёлый благородный одноатомный газ без цвета, вкуса и запаха.
В Российской Федерации действует Постановление Правительства РФ от 24 июля 2021 года N 1259 «Об утверждении перечня одурманивающих веществ». Запрещаются производство, закупка, поставка, хранение, перевозка, пропаганда использования ксенона не в целях производства и промышленного применения[7].
Общие сведения
| Ксенон | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ← Иод | Цезий → | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешний вид простого вещества | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Свечение ксенона в газоразрядной трубке |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Свойства атома | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Название, символ, номер | Ксено́н / Xenon (Xe), 54 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа, период, блок |
18 (устар. 8), 5, p-элемент |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомная масса (молярная масса) |
131,293(6)[1] а. е. м. (г/моль) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электронная конфигурация | [Kr] 4d105s25p6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус атома | ? (108)[2] пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Химические свойства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 130[2] пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Радиус иона | 190[2] пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электроотрицательность | 2,6 (шкала Полинга) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электродный потенциал | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Степени окисления | 0, +1, +2, +4, +6, +8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Энергия ионизации (первый электрон) |
1170,35 (12,1298)[3] кДж/моль (эВ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Термодинамические свойства простого вещества | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Плотность (при н. у.) |
3,52 (при −107,05 °C); |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура плавления | 161,3 К (-111,85 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура кипения | 166,1 К (-107,05 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Уд. теплота плавления | 2,27 кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Уд. теплота испарения | 12,65 кДж/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярная теплоёмкость | 20,79[4] Дж/(K·моль) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярный объём | 22,4⋅103 см³/моль | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
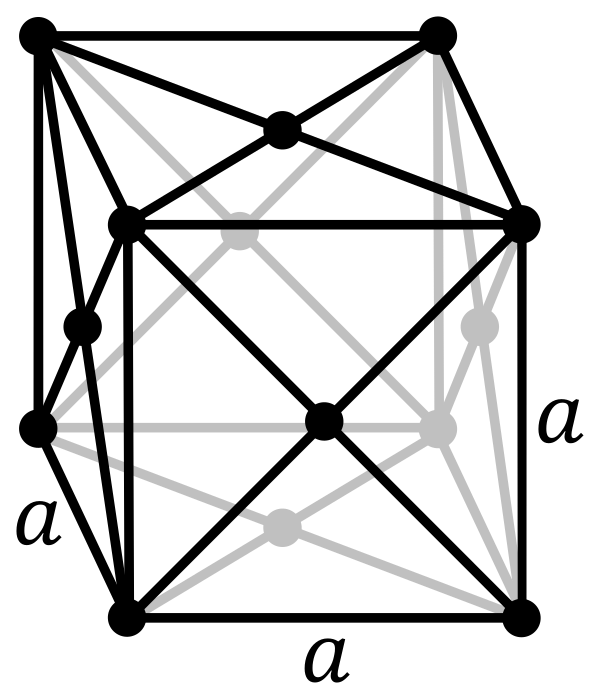
| Кристаллическая решётка простого вещества | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Структура решётки |
Кубическая гранецентрированая кубическая атомна |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Параметры решётки | 6,200[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Прочие характеристики | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплопроводность | (300 K) 0,0057 Вт/(м·К) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7440-63-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Эмиссионный спектр | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Наиболее долгоживущие изотопы | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
История
Ксенон был обнаружен как небольшая примесь к криптону[8][9]. За открытие инертных газов (в частности ксенона) и определение их места в периодической таблице Менделеева Уильям Рамзай получил в 1904 году Нобелевскую премию по химии.
Рамзай предложил в качестве названия элемента древнегреческое слово ξένον, которое является формой среднего рода единственного числа от |ξένος — «чужой, странный». Название связано с тем, что ксенон был обнаружен как примесь к криптону, и с тем, что его доля в атмосферном воздухе чрезвычайно мала.
| 54 | Ксенон
|
| 4d105s25p6 | |
Ксенон — весьма редкий элемент. При нормальных условиях в кубометре воздуха содержится 0,086[4]—0,087[10] см3 ксенона.
Распространение
Ксенон относительно редок в атмосфере Солнца, на Земле, в составе астероидов и комет. Концентрация ксенона в атмосфере Марса аналогична земной: 0,08 миллионной доли[11], хотя содержание изотопа 129Xe на Марсе выше, чем на Земле или Солнце. Поскольку данный изотоп образуется в процессе радиоактивного распада, полученные данные могут свидетельствовать о потере Марсом первичной атмосферы, возможно, в течение первых 100 миллионов лет после формирования планеты[12][13]. В атмосфере Юпитера, напротив, концентрация ксенона необычно высока — почти в два раза выше, чем в фотосфере Солнца[14].
Ксенон содержится в земной атмосфере в крайне незначительных количествах, 0,087 ± 0,001 миллионной доли по объёму (мкл/л), или 1 часть на 11,5 млн[10]. Он также встречается в газах, выделяемых водами некоторых минеральных источников. Некоторые радиоактивные изотопы ксенона, например 133Xe и 135Xe, получаются в результате нейтронного облучения ядерного топлива в реакторах.
Качественно ксенон обнаруживают с помощью эмиссионной спектроскопии (характеристические линии с длиной волны 467,13 нм и 462,43 нм). Количественно его определяют масс-спектрометрически, хроматографически, а также методами абсорбционного анализа[4].
Физические свойства
Полная электронная конфигурация атома ксенона: 1s22s22p63s23p63d104s24p64d105s25p6
При нормальном давлении температура плавления 161,40 К (−111,75 °C), температура кипения 165,051 К (−108,099 °C). Молярная энтальпия плавления 2,3 кДж/моль, молярная энтальпия испарения 12,7 кДж/моль, стандартная молярная энтропия 169,57 Дж/(моль·К)[4].
Плотность в газообразном состоянии при стандартных условиях (0 °C, 100 кПа) 5,894 г/л (кг/м3), в 4,9 раза тяжелее воздуха. Плотность жидкого ксенона при температуре кипения 2,942 г/см3. Плотность твёрдого ксенона 2,7 г/см3 (при 133 К)[4], он образует кристаллы кубической сингонии (гранецентрированная решётка), пространственная группа Fm3m, параметры ячейки a = 0,6197 нм, Z = 4[4].
Критическая температура ксенона 289,74 К (+16,59 °C), критическое давление 5,84 МПа, критическая плотность 1,099 г/см3[4].
Тройная точка: температура 161,36 К (−111,79 °C), давление 81,7 кПа, плотность 3,540 г/см3[4].
В электрическом разряде светится синим цветом (462 и 467 нм). Жидкий ксенон является сцинтиллятором.
Слабо растворим в воде (0,242 л/кг при 0 °C, 0,097 л/кг при +25 °C)[4].
При стандартных условиях (273 К, 100 кПа): теплопроводность 5,4 мВт/(м·К), динамическая вязкость 21 мкПа·с, коэффициент самодиффузии 4,8·10−6 м2/с, коэффициент сжимаемости 0,9950, молярная теплоёмкость при постоянном давлении 20,79 Дж/(моль·К)[4].
Ксенон диамагнитен, его магнитная восприимчивость −4,3·10−5. Поляризуемость 4,0·10−3 нм3[4]. Энергия ионизации 12,1298 эВ[3].
Химические свойства
Ксенон стал первым инертным газом, для которого были получены настоящие химические соединения. Примерами соединений могут быть дифторид ксенона, тетрафторид ксенона, гексафторид ксенона, триоксид ксенона, ксеноновая кислота и другие[15].
Первое соединение ксенона было получено Нилом Барлеттом реакцией ксенона с гексафторидом платины в 1962 году. В течение двух лет после этого события было получено уже несколько десятков соединений, в том числе фториды, которые являются исходными веществами для синтеза всех остальных производных ксенона.
В настоящее время описаны сотни соединений ксенона: фториды ксенона и их различные комплексы, оксиды, оксифториды ксенона, малоустойчивые ковалентные производные кислот, соединения со связями Xe-N, ксенонорганические соединения. Относительно недавно был получен комплекс на основе золота, в котором ксенон является лигандом. Существование ранее описанных относительно стабильных хлоридов ксенона не подтвердилось (позже были описаны эксимерные хлориды с ксеноном).
Фториды ксенона были одними из первых полученных соединений ксенона. Они были получены уже в 1962 году, сразу после установления возможности химических реакций для благородных газов. Фториды ксенона служат в качестве исходных веществ для получения всех остальных ковалентных соединений ксенона. Известны дифторид ксенона, тетрафторид ксенона, гексафторид ксенона и большое число их комплексов (преимущественно с фторированными кислотами Льюиса). Сообщение о синтезе октафторида ксенона не было подтверждено более поздними исследованиями.
- Реакции со фтором[16]:
- при комнатной температуре и УФ-облучении или при 300—500 ºC под давлением;
- при 400 ºC под давлением; примеси XeF2, XeF6;
- при 300 ºC под давлением; примесь XeF4.
Оксид ксенона(VI) впервые был получен осторожным гидролизом тетрафторида ксенона и гексафторида ксенона. При подкислении водных растворов перксенатов образуется желтый летучий взрывчатый тетраоксид ксенона.
Первые стабильные ксенонорганические соединения были получены в 1988 году реакцией дифторида ксенона с перфторарилборанами. Гексафторарсенат(V) пентафторфенилксенона(II) (C6F5Xe)[AsF6] необычайно стабилен, плавится почти без разложения при 102°С и используется как исходное соединение для синтеза других ксенонорганических соединений.
Изотопы ксенона
Известны изотопы ксенона с массовыми числами от 108 до 147 (количество протонов 54, нейтронов от 54 до 93), и 12 ядерных изомеров.
9 изотопов встречаются в природе. Из них стабильными являются семь: 126Xe, 128Xe, 129Xe, 130Xe, 131Xe, 132Xe, 134Xe. Ещё два изотопа (124Xe, T1/2 = 1,8·1022 лет и 136Xe, T1/2 = 2,165·1021 лет) имеют огромные периоды полураспада, на много порядков больше возраста Вселенной (~1,4·1010 лет).
Остальные изотопы искусственные, самые долгоживущие из них 127Xe (период полураспада 36,345 суток) и 133Xe (5,2475 суток), период полураспада остальных изотопов не превышает 20 часов.
Среди ядерных изомеров наиболее стабильны 131Xem с периодом полураспада 11,84 суток, 129Xem (8,88 суток) и 133Xem (2,19 суток)[17].
Изотоп ксенона с массовым числом 135 (период полураспада 9,14 часа) имеет максимальное сечение захвата тепловых нейтронов среди всех известных веществ — примерно 3 миллиона барн для энергии 0,069 эВ[18], его накопление в ядерных реакторах в результате цепочки β-распадов ядер теллура-135 и иода-135 приводит к эффекту так называемого отравления ксеноном (иодная яма).
Получение
Применение
Несмотря на высокую стоимость, ксенон незаменим в ряде случаев:
- Ксенон используют для наполнения ламп накаливания, мощных газоразрядных и импульсных источников света (высокая атомная масса газа в колбах ламп препятствует испарению вольфрама с поверхности нити накаливания).
- Радиоактивные изотопы (127Xe, 133Xe, 137Xe и др.) применяют в качестве источников излучения в радиографии и для диагностики в медицине, для обнаружения течи в вакуумных установках.
- Фториды ксенона используют для пассивации металлов.
- Ксенон как в чистом виде, так и с небольшой добавкой паров цезия-133, является высокоэффективным рабочим телом для электрореактивных (главным образом — ионных и плазменных) двигателей космических аппаратов. В 2020 году Роскосмос заявил о начале строительства космического аппарата «Нуклон» с ядерной силовой установкой. Ксенон будет использоваться в качестве рабочего тела реактивного двигателя.
- В конце XX века был разработан метод применения ксенона в качестве средства для наркоза и обезболивания. Первые диссертации о технике ксенонового наркоза появились в России в 1993 году. В 1999 году ксенон был разрешён к медицинскому применению в качестве средства для ингаляционного наркоза[19].
- Фториды и оксиды ксенона предложены в качестве мощнейших окислителей ракетного топлива, а также в качестве компонентов газовых смесей для лазеров[20].
- Ксенон используется для наполнения ячейки Голея в детекторах терагерцевого излучения[21].
- Для транспортировки фтора, проявляющего сильные окисляющие свойства.
- В 2014 году Всемирное антидопинговое агентство приравняло ингаляции ксенона к применению допинга[22].