Германий
| 32 | Германий
|
| 3d104s24p2 | |
Герма́ний (химический символ — Ge, от лат. Germаnium) — химический элемент 14-й группы (по устаревшей классификации — главной подгруппы четвёртой группы, IVA), четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 32.
Простое вещество германий — это типичный неметалл серо-белого цвета, с металлическим блеском. Подобно кремнию, является полупроводником.
Общие сведения
| Германий | ||||
|---|---|---|---|---|
| ← Галлий | Мышьяк → | ||||
| ||||
| Внешний вид простого вещества | ||||
 Поликристаллический образец германия |
||||
| Свойства атома | ||||
| Название, символ, номер | Герма́ний / Germanium (Ge), 32 | |||
| Группа, период, блок |
14 (устар. 4), 4, p-элемент |
|||
| Атомная масса (молярная масса) |
72,630(8)[1] а. е. м. (г/моль) | |||
| Электронная конфигурация |
[Ar] 3d104s2 4p2 1s22s22p63s23p63d104s24p2 |
|||
| Радиус атома | 122,5 пм | |||
| Химические свойства | ||||
| Ковалентный радиус | 122 пм | |||
| Радиус иона | (+4e) 53 (+2e) 73 пм | |||
| Электроотрицательность | 2,01 (шкала Полинга) | |||
| Электродный потенциал | 0 | |||
| Степени окисления | −4, −2, −3, −2, −1, 0, +2, +3, +4 | |||
| Энергия ионизации |
1‑я: 761,2 (7,89) кДж/моль (эВ)
3‑я: 3301,2 (34,21) кДж/моль (эВ) |
|||
| Термодинамические свойства простого вещества | ||||
| Плотность (при н. у.) | 5,323 г/см³ | |||
| Температура плавления | 1210,6 K | |||
| Температура кипения | 3103 K | |||
| Уд. теплота плавления | 36,8 кДж/моль | |||
| Уд. теплота испарения | 328 кДж/моль | |||
| Молярная теплоёмкость | 23,32[2] Дж/(K·моль) | |||
| Молярный объём | 13,6 см³/моль | |||
| Кристаллическая решётка простого вещества | ||||
| Структура решётки | Алмазная | |||
| Параметры решётки | 5,660 Å | |||
| Температура Дебая | 360 K | |||
| Прочие характеристики | ||||
| Теплопроводность | (300 K) 60,2 Вт/(м·К) | |||
| Номер CAS | 7440-56-4 | |||
История открытия и этимология
В своём докладе о периодическом законе химических элементов в 1869 году русский химик Дмитрий Иванович Менделеев предсказал существование нескольких неизвестных на то время химических элементов, в частности и германия. В статье, датированной 11 декабря (29 ноября по старому стилю) 1870 года, Д. И. Менделеев назвал неоткрытый элемент экасилицием (из-за его местонахождения в Периодической таблице) и предсказал его атомную массу и другие свойства[3][4].
В 1885 году в Фрайберге (Саксония) в одной из шахт был обнаружен новый минерал аргиродит. При химическом анализе нового минерала немецкий химик Клеменс Винклер обнаружил новый химический элемент. Учёному удалось в 1886 году выделить этот элемент, также химиком была отмечена схожесть германия с сурьмой. Об открытии нового элемента Винклер сообщил в двухстраничной статье, датируемой 6 февраля 1886 года и предложил в ней имя для нового элемента Germanium и символ Ge[5]. В последующих двух больших статьях 1886—1887 годов Винклер подробно описал свойства германия[6][7].
Первоначально Винклер хотел назвать новый элемент «нептунием», но это название было дано одному из предполагаемых элементов, поэтому элемент получил название в честь родины учёного — Германии.
Путём анализа тетрахлорида германия GeCl4 Винклер определил атомный вес германия, а также открыл несколько новых соединений этого металла[7].
До конца 1930-х годов германий не использовался в промышленности[8]. Во время Второй мировой войны германий использовался в некоторых электронных устройствах, главным образом в диодах[9].
Нахождение в природе
Общее содержание германия в земной коре 1,5⋅10−4 % по массе, то есть больше, чем, например, сурьмы, серебра, висмута. Германий вследствие незначительного содержания в земной коре и геохимического сродства с некоторыми широко распространёнными элементами обнаруживает ограниченную способность к образованию собственных минералов, внедряясь в кристаллические решётки других минералов. Поэтому собственные минералы германия встречаются исключительно редко. Почти все они представляют собой сульфосоли: германит Cu2(Cu, Fe, Ge, Zn)2 (S, As)4 (6—10 % Ge), аргиродит Ag8GeS6 (3,6—7 % Ge), конфильдит Ag8(Sn, Ge) S6 (до 2 % Ge) и др. редкие минералы (ультрабазит, ранерит, франкеит). Основная масса германия рассеяна в земной коре в большом числе горных пород и минералов. Так, например, в некоторых сфалеритах содержание германия достигает килограммов на тонну, в энаргитах до 5 кг/т, в пираргирите до 10 кг/т, в сульваните и франкеите 1 кг/т, в других сульфидах и силикатах — сотни и десятки г/т. Германий концентрируется в месторождениях многих металлов — в сульфидных рудах цветных металлов, в железных рудах, в некоторых окисных минералах (хромите, магнетите, рутиле и др.), в гранитах, диабазах и базальтах. Кроме того, германий присутствует почти во всех силикатах, в некоторых месторождениях каменного угля и нефти. Концентрация германия в морской воде 6⋅10−5 мг/л[10].
Получение
Германий встречается в виде примеси к полиметаллическим, никелевым, вольфрамовым рудам, а также в силикатах. В результате сложных и трудоёмких операций по обогащению руды и её концентрированию германий выделяют в виде оксида GeO2, который восстанавливают водородом при 600 °C до простого вещества:
Получение чистого германия происходит методом зонной плавки, что делает его одним из самых химически чистых материалов[11].
Производство германия в промышленных масштабах в СССР началось в 1959 году, когда на Медногорском медно-серном комбинате (ММСК) был введён в действие цех переработки пыли[12][13]. Специалисты комбината под руководством А. А. Бурбы в сотрудничестве с проектным институтом «Унипромедь» разработали и внедрили в производство уникальную химико-металлургическую технологию получения германиевого концентрата путём комплексной переработки пылей шахтных металлургических печей медеплавильного производства и золы от сжигания энергетических углей, служивших топливом для электростанции[14]. После этого СССР смог полностью отказаться от импорта германия. Впервые в мировой практике было выполнено извлечение германия из медноколчеданных руд. Пуск промышленного цеха переработки пыли на ММСК относят к крупнейшим внедрениям в цветной металлургии XX века[15].
В 1962 году по инициативе и при участии А. А. Бурбы аналогичное производство было создано также на Ангренском химико-металлургическом заводе (АХМЗ) в городе Ангрен в Узбекистане (ныне предприятие «Ангренэнергоцветмет»)[16][17]. Практически весь объём производства концентрата германия в СССР приходился на ММСК и АХМЗ[18]. Создание крупномасштабного производства германия внесло значительный вклад в обеспечение экономической и оборонной безопасности страны. Уже в 1960-е годы Советский Союз смог отказаться от импорта германия, а в 1970-е годы начать его экспорт и стать мировым лидером по производству германия[19].
Для переработки выпускавшегося на ММСК и АХМЗ германиевого концентрата в конечные продукты (чистый германий и его соединения) в 1961—1962 годах на Красноярском аффинажном заводе (с 1967 года — Красноярский завод цветных металлов, затем — ОАО «Красцветмет») был создан цех по производству германия (с 1991 года — ОАО «Германий»)[20][21]. В 1962—1963 годах цех производил 600 кг монокристаллического германия в год[22]. В 1968—1969 годах, когда внутренние потребности в германии были обеспечены, СССР впервые начал экспортировать диоксид германия, а в 1970 году начался также экспорт поликристаллического зонноочищенного германия[23]. СССР удерживал мировое лидерство по производству германия, увеличив выпуск металла настолько, что до 40 % производства уходило на экспорт[24].
После распада СССР, вплоть до 2010 года, ММСК оставался единственным производителем германиевого концентрата в России[25]. С 2010 года производство германия в концентрате на ММСК приостановлено, а оборудование законсервировано. Одновременно с этим начато производство германия в концентрате на ООО «Германий и приложения» в Новомосковске Тульской области[26][27]. В 2000-х годах для получения германия в России используются германиеносные угли следующих месторождений: Павловское (Михайловский район Приморского края), Новиковское (Корсаковский городской округ Сахалинской области), Тарбагатайское (Петровск-Забайкальский район Забайкальского края). Германиеносные угли этих месторождений в среднем содержат 200 граммов германия на тонну[28][29].
Физические свойства
Германий — хрупкий, серебристо-белый неметалл. Кристаллическая решётка устойчивой при нормальных условиях аллотропной модификации — кубическая типа алмаза.
Температура плавления 938,25 °C, температура кипения 2850 °C, плотность германия 5,33 г/см3.
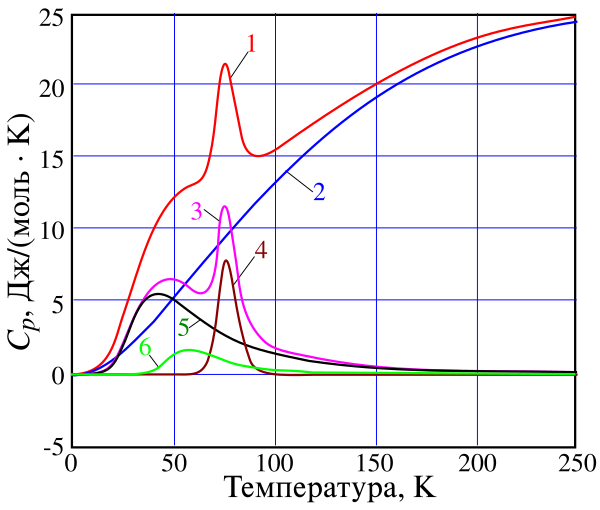
Теплоёмкость германия имеет аномальный вид, а именно, содержит пик над уровнем нормальной (колебательной) составляющей[30][31], который, как пишет Ф. Зейтц: «не может быть объяснён никакой теорией, предполагающей гуковский закон сил, ибо никакая суперпозиция эйнштейновских функций не даёт кривой с максимумом»[32] и объясняется, как и аномальность поведения теплоёмкостей гафния, алмаза и графита, больцмановским фактором, контролирующим диффузионную (диссоциационную) компоненту[33].
Германий является одним из немногих аномальных веществ, которые увеличивают плотность при плавлении. Плотность твёрдого германия 5,327 г/см3 (25 °С), жидкого — 5,557 г/см3 (при 1000 °С). Другие вещества, обладающие этим свойством — вода, кремний, галлий, сурьма, висмут, церий, плутоний.
Германий по электрофизическим свойствам является непрямозонным полупроводником.
- Основные полупроводниковые свойства нелегированного монокристаллического германия
- Статическая диэлектрическая проницаемость ε = 16,0.
- Ширина запрещённой зоны (при 300 К) Eg = 0,67 эВ
- Собственная концентрация ni = 2,33⋅1013 см−3[34].
- Эффективная масса[35]:
- Энергия сродства к электрону: χ = 4,0 эВ[36].
Легированный галлием германий в виде тонкой плёнки переходит при низких температурах в сверхпроводящее состояние[37].
Природный германий состоит из смеси пяти изотопов: 70Ge (20,55 % атомов), 72Ge (27,37 %), 73Ge (7,67 %), 74Ge (36,74 %), 76Ge (7,67 %).
Первые четыре изотопа стабильны, пятый (76Ge) весьма слабо радиоактивен и испытывает двойной бета-распад с периодом полураспада 1,58⋅1021 лет.
Искусственно получено 27 радиоизотопов с атомными массами от 58 до 89. Наиболее стабильным из радиоизотопов является 68Ge, с периодом полураспада 270,95 суток. А наименее стабильным — 60Ge, с периодом полураспада 30 мс.
Химические свойства
В химических соединениях германий обычно проявляет степени окисления +4 или +2. Сочетает свойства металла и неметалла. При этом соединения со степенью окисления +2 неустойчивы и стремятся перейти в степень окисления +4. При нормальных условиях германий устойчив к действию воздуха и воды, разбавленных щелочей и кислот. Медленно растворяется в горячих концентрированных растворах серной и азотной кислот:
Растворяется в щелочах лишь в присутствии окислителей (например, или ):
Растворим в расплавах щелочей с образованием германатов. Германий окисляется на воздухе до при температуре красного каления, взаимодействие с или парами серы приводит к образованию . Реакции с и дают соответственно и , а реакция с — смесь и .
Растворим в царской водке и в смеси концентрированных плавиковой и азотной кислот:
- Кластерные германиды (например, )
- Германиды (состава , , где — щелочной металл)
- Гидриды
- Гидрогалогениды германия ( )
- Галогениды германия
- Халькогениды
- Нитрид германия(IV)
- Оксиды
- Гидроксиды
- Соли
- *Катионные
- Анионные
- Германаты (например, германат натрия )
- Гидроксогерманаты (например, гексагидроксогерманат натрия )
- Галогенгерманаты
- Гексафторогерманаты (например, гексафторогерманат натрия )
- Гексахлорогерманаты (например, гексахлорогерманат цезия )
- Тиогерманаты (например, тиогерманат натрия )
- Различные сложные комплексные соединения
Германийорганические соединения — металлоорганические соединения содержащие связь германий — углерод. Иногда ими называются любые органические соединения, содержащие германий.
Первое германоорганическое соединение — тетраэтилгерман — было синтезировано немецким химиком Клеменсом Винклером в 1887 году.
Применение
В 2007 году основными потребителями германия были: 35 % волоконная оптика; 30 % тепловизорная оптика; 15 % химические катализаторы; 15 % электроника; небольшие количества германия потребляет металлургия[38].
- Благодаря прозрачности в инфракрасной области спектра металлический германий сверхвысокой чистоты имеет стратегическое значение в производстве оптических элементов инфракрасной оптики: линз, призм, оптических окон датчиков[39][40]. Наиболее важная область применения — оптика тепловизионных камер, работающих в диапазоне длин волн от 8 до 14 мкм. Это диапазон для наиболее популярных инфракрасных матриц на микроболометрах, используемых в системах пассивного тепловидения, военных системах инфракрасного наведения, приборах ночного видения, противопожарных системах. Германий также используется в ИК-спектроскопии в оптических приборах, использующих высокочувствительные ИК-датчики[40]. Германий проигрывает по пропускающей способности света в диапазоне от 8 до 14 мкм сульфиду цинка.[41] Однако германий, в отличие от сульфида цинка, продолжает пропускать порядка 25 % инфракрасного излучения до длины волны 23 мкм, поэтому является одним из основных материалов для длинноволновой инфракрасной оптики, обычно используемой в военных прицелах[42].
- Оптические детали из Ge обладают очень высоким показателем преломления (4,0) и обязательно требует использования просветляющих покрытий. В частности, используется покрытие из очень твёрдого алмазоподобного углерода, с показателем преломления 2,0[43][44].
- Наиболее заметные физические характеристики оксида германия (GeO2) — его высокий показатель преломления и низкая оптическая дисперсия. Эти свойства находят применение в изготовлении широкоугольных объективов камер, микроскопии, и производстве оптического волокна.
- Тетрахлорид германия используется в производстве оптоволокна, так как образующийся в процессе разложения этого соединения диоксид германия удобен для данного применения благодаря своему высокому показателю преломления и низкому оптическому рассеиванию и поглощению.
- Сплав GeSbTe используется при производстве перезаписываемых DVD. Сущность перезаписи заключается в изменении оптических свойств этого соединения при фазовом переходе под действием лазерного излучения[45].
- До 1970-х годов германий был основным полупроводниковым материалом электронной промышленности и широко использовался в производстве транзисторов и диодов. Впоследствии германий был полностью вытеснен кремнием. Германиевые транзисторы и диоды обладают характеристиками, отличными от кремниевых, ввиду меньшего напряжения отпирания p-n-перехода в германии — 0,35…0,4 В против 0,6…0,7 В у кремниевых приборов[46][47]. Кроме того, обратные токи у германиевых приборов имеют сильную зависимость от температуры, и на несколько порядков больше таковых у кремниевых — скажем, в одинаковых условиях кремниевый диод будет иметь обратный ток 10 пА, а германиевый — 100 нА, что в 10 000 раз больше. Также у германиевых приборов значительно выше шум и ниже температура, при которой происходит разрушение p-n-переходов[48]. По советскому ГОСТ 10862-64 (1964 г.) и более поздним стандартам германиевые полупроводниковые приборы имеют обозначение, начинающиеся с буквы Г или цифры 1, например: ГТ313, 1Т308 — высокочастотные маломощные транзисторы, ГД507 — импульсный диод. До того транзисторы имели индексы, начинающиеся с букв С, Т или П (МП), а диоды — Д, и определить материал прибора по индексу было сложнее. Диоды и транзисторы с индексами меньше 100 были германиевыми, от 100 до 199 — кремниевыми. Далее индексы зависели от частоты и мощности, причём у транзисторов и диодов правила отличались. До конца 1960-х годов германиевые полупроводниковые приборы использовались повсеместно, в настоящее время германиевые диоды и транзисторы практически полностью вытеснены кремниевыми, как имеющими значительно лучшие эксплуатационные характеристики.
- Сейчас в электронике германий используется в СВЧ-электронике, для создания гетероструктурных биполярных транзисторов (HBT) в SiGe-техпроцессе, способных работать на субтерагерцовых частотах[49]. Работы Жореса Алфёрова по структурам SiGe, в частности, заложили основу этого направления.
- Теллурид германия применяется как стабильный термоэлектрический материал и компонент термоэлектрических сплавов (термо-ЭДС 50 мкВ/К).
- Германий широко применяется в ядерной физике в качестве материала для детекторов гамма-излучения.
- В ювелирном сплаве Argentium (серебро пробы 935 либо 960) германий является легирующим элементом, обеспечивающим формирование прозрачного и стойкого защитного оксидного слоя на поверхности изделий.
Экономика
Биологическая роль
Германий обнаружен в животных и растительных организмах. Малые количества германия не оказывают физиологического действия на растения, но токсичны в больших количествах. Германий нетоксичен для плесневых грибков.
Для животных германий малотоксичен. У соединений германия не обнаружено фармакологическое действие. Допустимая концентрация германия и его оксида в воздухе — 2 мг/м3, то есть такая же, как и для асбестовой пыли.
Соединения двухвалентного германия значительно более токсичны[51].
Примечания
Литература
- Германий // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Бурба А. А. Разработка и освоение технологии получения германия при шахтной плавке руд цветных металлов // В сб.: Мат-лы научн. семинара по проблеме извлеч. германия при переработке руд: Информ. Гиредмета, 1960, № 7(18).
- Сосновский Г. Н., Бурба А. А. Германий: Учебн. пособие для студентов металлургич. специальности. Иркутск: Иркут. политехн. ин-т, 1967. — 161 с.
- Бурба А. А., Чижиков Д. М. Из опыта работы Медногорского МСК по извлечению германия из металлургических пылей и зол энергетических углей // В сб.: Мат-лы совещания по обмену опытом в области производства германиевого сырья (Центр микроэлектроники, Зеленоград): Сб. Гиредмета, 1969, т. 1.
- Наумов А. В. Мировой рынок германия и его перспективы. — Известия вузов. Цветная металлургия., № 4, 2007. — С. 32—40.
- Окунев А. И., Кирр Л. Д., Чижов Е. А. Комплексная переработка медеплавильных пылей с извлечением германия и элементов-спутников // 300 лет уральской металлургии: Тр. междунар. конгресса. 4—5 окт. 2001 г. — Екатеринбург, 2001. — С. 305.
Ссылки
| Классы соединений германия |





![{\displaystyle {\ce {Ge + 2 H2SO4 ->[t] GeO2 *}}x{\ce {H2O + 2 SO2 + {}}}(2-x){\ce {H2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/78f19599bdaa9050c88ad7151854ca0089b05e64)
![{\displaystyle {\ce {Ge + 4 HNO3 ->[t] GeO2 *}}x{\ce {H2O + 4 NO2 + {}}}(2-x){\ce {H2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/c19617335c102e399ed46ddab58b99e5b98fefbf)












![{\displaystyle {\ce {3 Ge + 4 HNO3 + 18 HCl -> 3 H2[GeCl6] + 4 NO ^ + 8 H2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/3fefc9a9a119543f8b019271eca12a0d4b552a8e)
![{\displaystyle {\ce {3 Ge + 4 HNO3 + 18 HF -> 3 H2[GeF6] + 4 NO ^ + 8 H2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/7096d5a2ff38c4534a020c719e104af2516aec49)
![{\displaystyle {\ce {Na2[(En)3]Ge9}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/ce9acc2894bb81ac8cb3b35e58d28a77e1618804)



































![{\displaystyle {\ce {Na2[Ge(OH)6]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/fd86b1643fed93213616186eaf758dccc180ac8a)
![{\displaystyle {\ce {[GeF6]^{2-}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/f3a7e5c9f34827713af0eed6feea96d0017193bf)
![{\displaystyle {\ce {Na_2[GeF_6]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/b67957e702ce2fe768d5ce551f711cbde8478368)
![{\displaystyle {\ce {[GeCl6]^{2-}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/6288b851f46167f7a9e632cc8519675181dcfc5d)
![{\displaystyle {\ce {Cs2[GeCl6]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/b73aedfc7d5b33957ff9944453184ecbc747c195)





