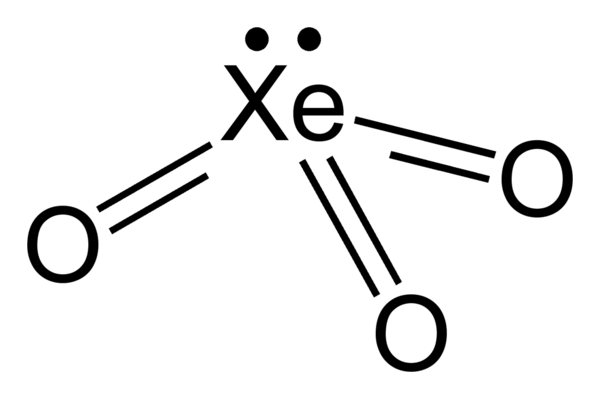
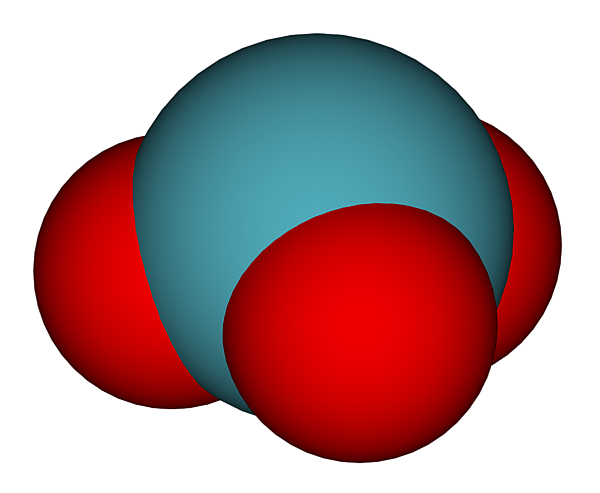
Триоксид ксенона
Триокси́д ксено́на XeO3 — белые или светло-голубые кристаллы. Получают гидролизом тетра- или гексафторида ксенона. В сухом виде чрезвычайно взрывоопасен, особенно при контакте с органикой.
Общие сведения
| Триоксид ксенона | |
|---|---|
| Общие | |
| Систематическое наименование |
Триоксид ксенона |
| Хим. формула | XeO3 |
| Физические свойства | |
| Молярная масса | 179,288 г/моль |
| Плотность | 4,55 г/см³ |
| Классификация | |
| Рег. номер CAS | 13776-58-4 |
| 3D model (JSmol) | Интерактивная схема |
| UNII | IM8XMX5O5Q |
| CompTox Dashboard EPA | DTXSID80894909 |
| SMILES | |
| InChI | |
| ChemSpider | 21106493 |
| Безопасность | |
| NFPA 704 | |
Физические свойства
Химические свойства
С водой образует ксенонистую кислоту H2XeO4, которая постепенно разлагается с выделением кислорода и ксенона. Водный раствор не взрывоопасен, является сильным окислителем. Способен окислять соли марганца до перманганата. С щелочами образует соли — ксенаты.
Получение
Триоксид ксенона получают контролируемым гидролизом тетрафторида или гексафторида ксенона при пониженной температуре.
Применение
В настоящее время, из-за нестабильности, не находит применения.
Литература
- Разумовский С. Д. Кислород — элементарные формы и свойства. — М.: Химия, 1979. — С. 148
- Успехи химии. — 1965. — Т.34, № 6. — С. 990—992
- Успехи химии. — 1974. — Т.43, № 12. — С. 2169—2170
- Химическая энциклопедия. — Т.2. — М.: Советская энциклопедия, 1990. — С. 548