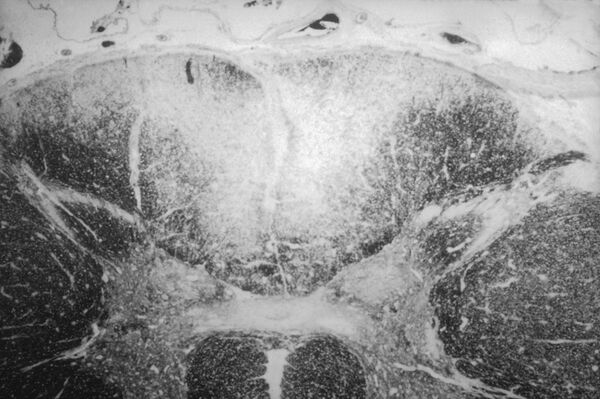
Спинная сухотка
Спинна́я сухо́тка (СС; лат. tabes dorsalis) — поздняя форма паренхиматозного нейросифилиса. Это медленно прогрессирующее заболевание, при котором поражаются задние столбы и задние корешки спинного мозга. Патологические изменения заключаются в демиелинизации, атрофии и дегенерации тканей, чаще всего в области поясничных и крестцовых сегментов. Первые неврологические проявления включают нарушение болевой чувствительности, угасание сухожильных рефлексов, ухудшение вибрационной и позиционной чувствительности, а также нарастающую атаксию. При своевременном лечении прогноз для жизни обычно благоприятный. Однако уже возникшее повреждение нервных структур является необратимым. При отсутствии терапии болезнь может привести к параличу, слепоте и слабоумию[3][4].
Общие сведения
История
Первое клинико-морфологическое описание СС выполнено М.Г. Ромбергом в 1840 году, который не связывал заболевание с сифилисом. В 1858 году Г. Дюшен представил развёрнутую клиническую характеристику под названием «прогрессирующая локомоторная атаксия», отметив наличие сифилиса в анамнезе у части пациентов, но не усмотрев причинно-следственной связи. В 1873 году Ж.-А. Фурнье выдвинул гипотезу о сифилитической этиологии на основании наблюдений: среди 30 пациентов с атаксией у 24 ранее диагностирован сифилис. В 1881 году У. Гоуэрс и В. Эрб представили эпидемиологические данные, подтверждающие связь между сифилисом и СС. В 1885 году Фурнье обосновал необходимость ранней диагностики ввиду необратимости поражения задних столбов при развитой стадии заболевания. Окончательное подтверждение этиологии получено после идентификации Treponema pallidum (Ф. Шаудин, Э. Гофман, 1905) и разработки реакции Вассермана (1906)[5].
Классификация
СС представляет собой форму третичного, или позднего, нейросифилиса[6].
Этиология
Этиология СС связана с перенесённой сифилитической инфекцией. Заболевание развивается как позднее проявление нейросифилиса у пациентов, не получавших адекватного лечения в острой стадии. Возбудителем является бактерия Treponema pallidum из семейства Spirochaetaceae[6][7].
Патогенез
Патогенез СС включает воспалительный ответ на трепонему, характеризующийся периваскулярными инфильтратами из лимфоцитов, гистиоцитов, плазматических клеток, макрофагов и Т-хелперов, а также формированием гумм и казеозного некроза в гранулёмах. Высвобождаемые из этих воспалительных клеток цитокины вызывают дополнительное повреждение клеток, способствуя нейрональной дегенерации. Прямая инвазия трепонем в крупные миелинизированные нервы также может приводить к их дегенерации и развитию нейропатии. Исследования показывают, что бледная трепонема нарушает метаболизм и гомеостаз железа путём образования активных форм кислорода, что вносит вклад в повреждение нейронов. Конечным результатом этих процессов является нейродегенерация с демиелинизацией сенсорных нервных волокон в задних корешках и задних канатиках спинного мозга, что в итоге приводит к характерным симптомам[6].
При гистологическом исследовании выявляются демиелинизация и последующая дегенерация нейронов задних корешков. Поражённые задние столбы выглядят бледными вследствие атрофии и соответствующего побледнения, обусловленного утратой аксонов задних корешков и миелиновых оболочек. Периваскулярная инфильтрация представлена преимущественно CD4+ и CD8+ Т-лимфоцитами, макрофагами и плазматическими клетками, сопровождаясь облитерацией мелких сосудов. В центральной нервной системе могут обнаруживаться гуммы в виде узелков центрального казеозного некроза, окружённых воспалительным инфильтратом с гранулёматозным характером[6].
Эпидемиология
Диагностика
Клиническая картина СС характеризуется длительным латентным периодом, который в среднем составляет 20 лет от момента первичного инфицирования до появления первых симптомов. Основные проявления заболевания включают[6]:
- интермиттирующие приступы интенсивной колющей боли, локализующейся преимущественно в спине, животе или нижних конечностях. Продолжительность болевых кризов варьирует от нескольких минут до нескольких дней. Они могут возникать спонтанно, провоцироваться стрессовыми факторами или воздействием холода. Висцеральные кризы проявляются рецидивирующими эпизодами выраженной эпигастральной боли в сочетании с тошнотой и рвотой. На ранних стадиях заболевания нередко наблюдаются задержка мочеиспускания с парадоксальной ишурией и импотенция;
- ключевым признаком являются зрачковые нарушения, среди которых почти в половине случаев встречается зрачок Аргайлла Робертсона. Данный симптом характеризуется малым неправильной формы зрачком, утрачивающим реакцию на свет, но сохраняющим живое сужение при фиксации взгляда на близких предметах;
- при оценке неврологического статуса выявляет снижение глубоких сухожильных рефлексов на нижних конечностях, ослабление болевой чувствительности и положительный симптом Ромберга. Дефицит проприоцепции обусловливает характерную походку с широко расставленными ногами, которая становится неуверенной и нецеленаправленной, сопровождаясь «шлёпающими» движениями стоп. Пациенты могут частично компенсировать этот дефект зрительным контролем. Также выявляются нарушения вибрационной и тактильной чувствительности, возможны атрофия зрительного нерва и прогрессирующая дегенерация суставов. На поздних стадиях развиваются выраженный спастический парапарез и вегетативная дисфункция;
- специфическим проявлением заболевания служат суставы Шарко с преимущественным поражением коленных и тазобедренных суставов. Особую форму представляет позвоночник Шарко (спинальная нейроартропатия) — редкое прогрессирующее разрушение костных и мягкотканных структур позвоночника вследствие длительной утраты чувствительности и проприоцепции. Клиническая картина включает деструкцию позвонков, болевой синдром, парестезии, мышечную слабость, снижение чувствительности, спастичность, угнетение сухожильных рефлексов, вегетативные нарушения и нестабильность позвоночника с формированием кифотической деформации;
- патогенетически утрата чувствительности приводит к нарушению защитных мышечных сокращений, что обусловливает повторную микротравматизацию позвоночника с развитием локальных воспалительных выпотов. Микропереломы сопровождаются попаданием костно-хрящевых фрагментов в полость выпота, что усугубляет воспалительный процесс, ведёт к формированию костных мозолей, сужению межпозвонковых дисков, повреждению связочного аппарата и образованию паравертебральных масс. Прогрессирование патологического процесса может осложняться компрессионными переломами, деструкцией позвонков и компрессией нервных корешков.
Иммуноферментный анализ крови: характерно выявление антител к Treponema pallidum[6].
Клинический анализ ликвора: характерно повышение концентрации белка в пределах от 45 до 75 миллиграммов на децилитр, плеоцитоз свыше 20 лейкоцитов на микролитр[6].
Магнитно-резонансная томография: характерны отёк и повышение интенсивности сигнала в поражённом сегменте спинного мозга после введения гадолиния с периферическим линейным усилением, а также интенсивное продольное усиление сигнала вдоль задних столбов. Может наблюдаться атрофия спинного мозга[6][8].
Дифференциальная диагностика
Дифференциальная диагностика СС проводится со следующими заболеваниями[6][7]:
- адреномиелонейропатия;
- алкогольная полинейропатия и мозжечковая дегенерация;
- аутоиммунные демиелинизирующие заболевания (рассеянный склероз, оптиконейромиелит, заболевания, ассоциированные с антителами к миелиновому олигодендроцитарному гликопротеину);
- боковой амиотрофический склероз;
- болезнь Лайма (боррелиоз);
- ВИЧ-инфекция;
- дефицит витамина В12;
- дефицит витамина E;
- дефицит меди;
- избыточное потребление цинка;
- интоксикация героином;
- интоксикация закисью азота;
- компрессия спинного мозга опухолью или грыжей диска;
- латиризм;
- митохондриальные заболевания;
- наследственная спастическая параплегия;
- опухолевая миелопатия (компрессия спинного мозга новообразованием);
- постинфекционная демиелинизация;
- саркоидоз;
- сахарный диабет;
- синдром Ади;
- сосудистая миелопатия (нарушение перфузии, инфаркт спинного мозга);
- спинальная мышечная атрофия;
- атаксия Фридрейха;
Осложнения
Лечение
Препаратом выбора при лечении СС является пенициллин, который вводится внутривенно в течение 10-14 дней. Пациентам с аллергией на пенициллин после подтверждения истинной аллергии проводится десенсибилизация; при невозможности её выполнения альтернативой служат цефтриаксон или доксициклин. Дополнительно применяется симптоматическая терапия: анальгетики для купирования болевых кризов, физическая и трудотерапия для предотвращения мышечной атрофии. При позвоночнике Шарко возможно хирургическое вмешательство со стабилизацией и спондилодезом либо консервативное ведение с использованием ортезов и постельного режима[6][7].
Прогноз
Своевременная диагностика и адекватная терапия обеспечивают благоприятный прогноз при СС. Лечение позволяет остановить прогрессирование заболевания и предотвратить развитие тяжёлых осложнений. Однако уже сформировавшееся повреждение нервной ткани является необратимым. При отсутствии терапии заболевание неуклонно прогрессирует, приводя к параличам, слабоумию и слепоте[6].
Диспансерное наблюдение
Профилактика
Основой профилактики СС является профилактика приобретённого сифилиса, которая включает несколько направлений. Индивидуальная защита обеспечивается использованием барьерных методов контрацепции, а после незащищённого полового контакта возможно применение местных антисептических средств. На популяционном уровне проводятся санитарно-просветительская работа и скрининговое обследование групп риска[9].