Синдром осмотической демиелинизации
Синдром осмотической демиелинизации (СОД, центра́льный понти́нный миелино́лиз) — это острое демиелинизирующее заболевание центральной нервной системы, с поражением моста мозга или иных областей, связанное с осмотическим стрессом. Наиболее часто развитие СОД связывают с быстрой коррекцией гипонатриемии[2].
Синонимы: центральный понтинный миелинолиз (демиелинизация в основании моста головного мозга)/ экстрапонтинный миелинолиз (демиелинизация с вовлечением таких структур как мозжечок, наружная и внутренняя капсула, латеральное коленчатое тело, таламус, базальные ганглии, гиппокамп).
Общие сведения
История
Первые описания не воспалительной демиелинизации в области моста головного мозга, сделаны в 1959 г., когда Р. Д. Адамс, М. Виктор и Э. Л. Манколл описали четырёх пациентов, злоупотребляющих алкоголем и с нарушением питания, у которых возникли псевдобульбарные нарушения и тетрапарез (слабость всех конечностей), а при вскрытии были обнаружены симметричные участки демиелинизации в основании моста головного мозга[2][3]. Внепонтинный миелинолиз (в сочетании с поражением моста или изолировано) описан в 1962 г.
К 70-м годам 20 века синдром осмотической демиелинизации связали с быстрой коррекцией сниженного уровня натрия в плазме крови. Так в 1976 г. Томлинсон описал два клинических случая развития СОД у женщин без указаний на злоупотребление алкоголем или истощение. У этих пациенток симптоматика появилась на фоне коррекции гипонатриемии[4].
Лаурено и Кляйншмидт-Де Мастерс показали в экспериментах на животных зависимость между скорость повышения натрия и развитием демиелинизации[5]. В дальнейшем появились описания случаев СОД на фоне гипернатриемии у больных с ожогами и рвотой беременных.
Эпидемиология
Абсолютно достоверных данных о распространённости данного заболевания нет. Встречаемость может быть разной в зависимости от той патологии, на фоне которой развивается это осложнение.
Согласно ретроспективному исследованию, проведённому в 2015 г. у 2,5 % пациентов, поступивших в отделения интенсивной терапии, был диагностирован синдром осмотической демиелинизации. Если оценивать только пациентов с выраженной гипонатриемией, то после её быстрой коррекции неврологическая симптоматика развивалась у 25 % пациентов. В этом исследовании отмечена большая распространённость патологии у пациентов после трансплантации печени. Клинические симптомы связанные с осмотической демиелинизацией фиксировались, как правило, в первые 10 суток после трансплантации[2]. Прогноз у пациентов с СОД после трансплантации печени хуже, чем у других пациентов (совокупный уровень смертности и инвалидности составил 77,4 % по сравнению с 44,7 % у пациентов без трансплантации печени). Зависимости частоты развития симптомов от возраста, пола и признаков употребления алкоголя не выявлено[6].
Ещё одно крупное исследование проведено в Канаде, где оценивались пациенты с гипонатриемией (с уровнем натрия менее 130 ммоль/л) и коррекцией уровня натрия со скоростью более 8 ммоль/л в сутки, поступавшие в стационары в период с 2010 по 2020 г. Синдром осмотической демиелинизации был установлен по данным медицинской документации и результатам нейровизуализации. Установлено, что быстрая коррекция уровня натрия у пациентов с гипонатриемией отмечена у 17,7 % пациентов, но СОД встречался редко — 0,05 %[7].
Встречаемость данного синдрома у детей значительно ниже, чем во взрослой популяции.
Анализ 106 случаев педиатрического СОД по литературным данным, в период с 1960 по 2018 год, показал что большая часть описанных случаев отмечалось в возрастной группе от 1 до 5 лет.[8] Считалось, что эти случаи, как и у взрослых, возникли после слишком быстрой коррекции гипонатриемии (более 12 мэкв/л в течение 24 часов). При оценке прогноза заболевания установлено, что 60 % детей имели полное или частичное выздоровление, а 39 % умерли. Но после 2000 года, количество детей погибших от синдрома осмотической демиелинизации было значительно меньше и составило 9 %. Клиническая картина у детей также была вариабельна, встречались как поражения моста, так и экстрапонтинные очаги демиелинизации. У детей описаны такие симптомы как бульбарные нарушения, глазодвигательные, двигательные нарушения и другие. Поражения вне моста головного мозга часто давали неспецифические симптомы (Например: когнитивные нарушения, судороги, нарушения походки, глухота[9]).
Этиология
Считается, что основной причиной развития осмотической демиелинизации является быстрая коррекция хронической гипонатриемии (хронической является гипонатриемия существующая более 48 часов), у людей с состояниями и заболеваниями, предрасполагающими к развитию СОД.
К группе риска по развитию осмотической демиелинизации относятся люди:
- страдающие алкоголизмом;
- пациенты после трансплантации печени;
- люди с серьёзными заболеваниями печени и почек (в том числе описаны случаи развития синдрома осмотической демиелинизации у пациентов с болезнью Вильсона-Коновалова)[10];
- после перенесённой лучевой терапии головного мозга;
- пациенты с истощением на фоне тяжёлого заболевания;
- пациенты с ожогами (за счёт гипернатриемии)[11];
- пациенты с неукротимой рвотой (в том числе рвотой беременных).
Существует теория, что у пациентов с тяжёлым поражением печени может развиваться синдром осмотической демиелинизации на фоне гипераммонемии и без гипонатриемии[12].
В отдельных описаниях клинических случаев синдром осмотической демиелинизации развивался и на фоне другой патологии
Ятрогенно обусловленные электролитные нарушения с развитием СОД на фоне применения некоторых групп препаратов и веществ: нейролептики, антидепрессанты (например: селективные ингибиторы обратного захвата серотонина (SSRI), нестероидные противовоспалительные препараты из группы коксибов, ингибиторы протонной помпы, антиконвульсанты (включая прегабалин), иммунологические, лекарственные препараты используемые в онкологии, кардиологические препараты, опиаты, экстази и другие психотропные вещества[13].
Патофизиология клеточного повреждения
В зависимости от длительности гипонатриемии, последовательно включаются два механизма поддержания осмолярности. Первый работает в течение нескольких часов и заключается в том, что из клетки выходят электролиты. Если этого недостаточно, то в дальнейшем запускается второй, отсроченный механизм. Его суть в том, что из клетки выходят органические осмолиты (миоинозитол, фосфокреатин, креатин и другие). Это более долговременный процесс и, при быстрой коррекции длительно существующей гипонатриемии, клетка не может начать вырабатывать эти осмолиты с необходимой скоростью[14][2]. В результате при быстром введении значительного количества натрия извне, вода по градиенту концентрации выходит из клеток, и они сморщиваются.
Сморщивание клетки может произойти и при быстром нарастании уровня натрия (более 170 ммоль/л), без предшествующей гипонатриемии.
Есть небольшое исследование о роли аквапориновых каналов (AQP1 и AQP4) в патогенезе развития осмотической демиелинизации[15].
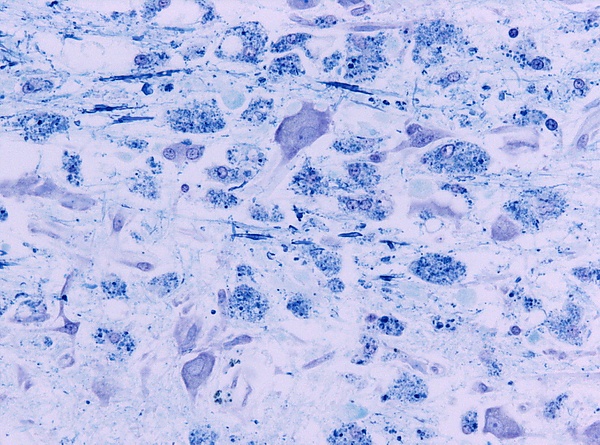
- Микроскопические изменения нервной ткани при осмотической демиелинизации
При гистологическом исследовании в очаге поражения отмечается не воспалительная демиелинизация, инфильтрация макрофагами и снижение количества олигодендроцитов за счёт их апоптоза, астроглиоз и микроглиоз. При этом структура нейронов и аксонов сохранена.
Типичная локализация поражения в области моста может объясняться морфологической структурой данного региона, особенностью которого является высокая концентрация олигодендроцитов, компактное расположение и переплетение волокон серого и белого вещества. Схожая морфология есть и у регионов, которые могут вовлекаться в процесс вне моста. Это такие области головного мозга как мозжечок (поражается в 33 % случаев экстрапонтинного миелинолиза), наружная и внутренняя капсула, латеральное коленчатое тело, таламус, базальные ганглии и гиппокамп.[16]
Клиническая картина
Симптомы заболевания появляются обычно в течение 2-3 дней после коррекции гипонатриемии (но могут быть и отклонения от этих сроков до 1-2 недель).
Классические проявления демиелинизации в области моста включают бульбарные нарушения, такие как, дисфагия и дизартрия (анатомически связаны с повреждением кортико-бульбарных волокон) и тетрапарез (вследствие повреждения волокон кортикоспинального тракта)
Клиническая картина может включать такие симптомы как:
- Нарушения сознания (иногда до комы), когнитивные и психические нарушения (делирий, галлюцинации) -анатомически связаны с повреждением покрышки моста и/или таламуса
- Бульбарные нарушения
- Глазодвигательные нарушения (горизонтальный и вертикальный парез взора)
- Слабость в конечностях (вплоть до тетрапареза), также может развиться «синдром запертого человека» («locked-in» syndrome)[10]
- Нарушения координации, тремор[17]
- Чувствительные нарушения
- Паралич лицевой мускулатуры
Диагностика
- Неврологический осмотр.
- Стандартные лабораторные исследования (в первую очередь уровень натрия сыворотки крови и его изменения, уровень калия, тесты для оценки работы печени и почек).
- Нейровизуализация: компьютерная томография как скрининговый метод. В первую очередь для исключения другой патологии головного мозга. Магнитно-резонансная томография. Возможно использование позитронно-эмиссионной томографии (ПЭТ).
- Иногда слуховые вызванные потенциалы (как и ПЭТ, в настоящее время, не является рутинным методом обследования)[17].
На КТ могут быть выявлены очаги сниженной плотности (более тёмной окраски) области в нижней части моста. Но КТ не является методом выбора для визуализации изменений ассоциированных с миелинолизом. Это связано с тем, что чаще всего изменения локализуются в мосту мозга, которых окружён костной тканью, дающей артефакты на изображении.
Чаще изменения локализуются в нижней части моста имеют вид трезубца или бабочки. Но могут быть также в базальных ганглиях, среднем мозге и белом веществе субкортикальных областей. Накопление контрастного вещества возможно.
Ранние изменения (в первые 24 часа от развития тетрапареза): гиперинтенсивный сигнал (что говорит об ограничении диффузии) в режиме DWI. Изменения в режимах Т1- (гипоинтенсивный сигнал) и Т2-ВИ (гиперинтенсивный) могут развиваться не сразу (до 2 недель). Другие последовательности: FLAIR: гиперинтенсивный, ADC: низкий сигнал.
Вначале может быть высокое накопление 18-ФДГ, которое сменяется гипометаболизмом. (ПЭТ не является обязательным и рутинным методом исследования).
Дифференциальная диагностика
- Другие демиелинизирующие заболевания (такие как рассеянный склероз)[2];
- опухоли мостовой локализации (астроцитомы, метастазы, лимфома центральной нервной системы);
- инсульт;
- мультифокальная лейкоэнцефалопатия;
- острые аутоимунные и инфекционные энцефалиты;
- васкулиты центральной нервной системы;
- гипертензивная энцефалопатия, Синдром Гайе — Вернике;
- токсичность вигабатрина[18].
Терапия
Специфической терапии развившегося синдрома осмотической демиелинизации не разработано. Проводится поддерживающая терапия, коррекция осложнений. Пациентам с алкогольным анамнезом дополнительно назначают витамины (в первую очередь тиамин).
Физиотерапия для профилактики контрактур, мышечной атрофии, дыхательных нарушений и так далее[17].
Основным методом предотвращения развития синдрома осмотической демиелинизации является медленная коррекция хронической гипонатриемии (в первые сутки не более 10 ммоль/л и не более 8 ммоль/л в последующие). При быстром повышении уровня натрия, проводят его коррекцию с использованием раствора глюкозы (вводят 5 % раствор глюкозы 10 мл/кг/час), данная терапия требует контроля диуреза[19].
Для предотвращения избыточной коррекции гипонатриемии, на фоне применения гипертонического раствора хлорида натрия, может использоваться десмопрессин, который вводится подкожно или внутривенно 1-2 мкг внутривенно или подкожно каждые 6-8 часов в течение 24 часов[2].
Это методы, которые применялись в отдельных клинических случаях с положительным результатов, но крупных исследований по ним не проводилось. Все эти методы мало изучены и нужны дополнительные исследования для подтверждения их эффективности.
На фоне использования плазмафереза исследователи отмечали положительный клинический эффект, без влияния на картину магнитно-резонансной томографии. Влияние плазмафереза связывают с удалением из сыворотки высокомолекулярных веществ повреждающих миелиновую оболочку нервных волокон.
Есть исследования по применению дексаметазона в экспериментальных моделях осмотического стресса на животных, в которых отмечено меньше очагов поражения головного мозга на фоне терапии, по сравнению с группой не получавшей лечения глюкокортикостероидами. Описаны единичные случаи использования глюкокортикостероидов в лечении синдрома осмотической демиелинизации у людей[2].
Также имеются сообщения о использовании в терапии селективного антагониста V2 рецепторов Толваптана для лечения хронической гипонатриемии[16][20].
Прогноз
Ранее считалось, что синдром осмотической демиелинизации состояние с высокой летальностью. Но по мере улучшения возможностей диагностики и выявления менее тяжёлых форм заболевания, данные по прогнозу также претерпели изменения[21].
По данным исследований проведённых в 2000—2010 годах выживаемость среди пациентов с синдромом осмотической демиелинизации достигает 94 %, при этом 25—40 % без неврологического дефицита, а 25—30 % становятся нетрудоспособными[2].
К факторам неблагоприятного исхода относят:
- уровень натрия менее 120 ммоль/л;
- гипокалиемию;
- низкий балл по шкале ком Глазго;
- состояние после трансплантации печени;
При этом клинические проявления и данные визуализации головного мозга не оказывали значительного влияния на прогноз.
Выявление пациентов из группы риска, которым требуется осторожная коррекция уровня натрия, а также профилактика и терапия вторичных осложнений (таких как аспирационная пневмония, тромбоэмболические осложнения, инфекция мочевыводящих путей и другие) может предотвратить развитие синдрома осмотической демиелинизации и улучшить прогноз для таких больных[22].