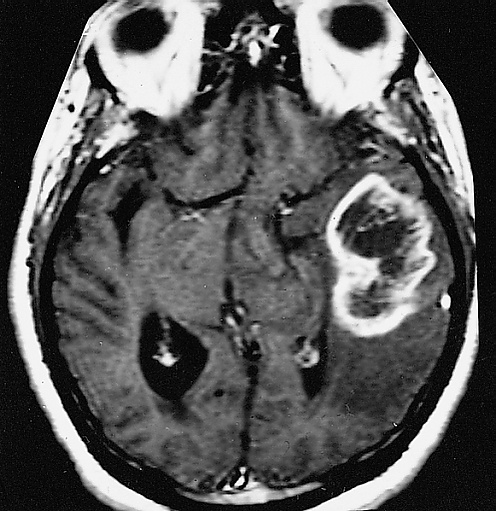
Псевдотуморозный рассеянный склероз
Псевдотуморо́зный рассе́янный склеро́з (ПРС; псевдоо́пухолевые демиелинизи́рующие поражени́я, опухолеподо́бный рассе́янный склеро́з, опухолеви́дная фо́рма рассе́янного склеро́за, опухолеподо́бные демиелинизи́рующие очаги́) — атипичная и редкая форма рассеянного склероза (РС), характеризующаяся образованием опухолевидных очагов в центральной нервной системе. Опухолеподобные очаги на магнитно-резонансной томографии могут имитировать первичные опухоли головного мозга, что создаёт значительные диагностические сложности. Распространённость данной формы составляет 1—3 случая на 1000 пациентов с РС, однако общая распространённость опухолеподобных очагов, включая изолированные случаи и ассоциированные с другими синдромами, остаётся неучтённой. Клинические проявления варьируются в зависимости от локализации и размера очага, при этом наиболее частыми симптомами являются гемипарез, гемичувствительные нарушения, дефекты полей зрения, головные боли, афазия или дисфазия, апраксия, когнитивные нарушения, спутанность сознания и изменения уровня сознания[1][2].
История
Термин «опухолеподобная демиелинизация» (англ. Tumefactive Demyelination) впервые введён в 1979 году ван дер Велденом и соавторами, когда они наблюдали пациента с соответствующим поражением, выявленным на компьютерной томографии головы, при этом данные биопсии соответствовали РС[3].
Классификация
ПРС относится к атипичным формам РС[2].
Этиология
РС и ПРС имеют общую этиологию. Эти состояния часто возникают одновременно, характеризуются демиелинизацией с возможным периваскулярным отёком. Заболевание имеет полигенную наследственную предрасположенность — идентифицировано более 200 генетических факторов, способствующих её формированию. Реализация этой предрасположенности происходит под влиянием внешних факторов, среди которых ключевыми считаются вирусные инфекции (особенно ретровирусы и вирус Эпштейна — Барр), дефицит витамина D, раннее начало курения, изменения микробиома кишечника и другие воздействия окружающей среды[2][4].
Патогенез
Патогенез заболевания связан с продукцией провоспалительных цитокинов Т- и В-лимфоцитами как на системном уровне, так и локально в тканях центральной нервной системы. Эти цитокины активируют аутореактивные Т-лимфоциты, что запускает развитие аутоиммунного воспалительного поражения центральной нервной системы. Нейродегенеративные изменения наблюдаются уже на начальных стадиях патологического процесса. Активация клонов сенсибилизированных иммунных клеток в сочетании с дисбалансом противовоспалительных и регуляторных функций иммунной системы способствует хронизации воспаления. Вторично активированные макрофаги и клетки микроглии дополнительно усиливают патологический процесс через секрецию провоспалительных цитокинов[2][4].
Очаги при ПСР преимущественно локализуются на супратенториальном уровне, в белом веществе, с возможным распространением в серое вещество. Реже встречаются поражения ствола головного мозга и спинного мозга[2].
При гистологическом исследовании наблюдается периваскулярная пролиферация лимфоцитов без атипичных черт. Окрашивание по Клюверу — Баррера демонстрирует фокальное отсутствие миелиновой оболочки, что свидетельствует о демиелинизирующем процессе. Большинство пролиферирующих лимфоцитов относятся к Т-клеточному типу. Характерно присутствие макрофагов (CD68+), свидетельствующих о воспалительных изменениях в области поражения. Совокупность этих признаков подтверждает воспалительно-демиелинизирующую природу заболевания и позволяет дифференцировать его от неопластических процессов[5].
Эпидемиология
Согласно данным литературы, ПСР встречаются с частотой 1—3 случая на 1000 пациентов с РС, однако общая распространённость этих поражений, включая изолированные случаи и ассоциированные с другими синдромами, остаётся неустановленной. Возраст дебюта заболевания обычно варьирует от 10 до 66 лет, при этом средний возраст составляет 27 лет. Также в литературе отмечается преобладание данного состояния среди женщин[2].
Диагностика
Клиническая картина ПСР отличается вариабельностью и зависит от локализации и размера поражения. Наиболее распространёнными симптомами являются гемипарез, гемианопсия, головные боли, афазия или дисфазия, апраксия, когнитивные нарушения, спутанность сознания и изменения уровня сознания. Описан также уникальный случай «бессимптомного» течения, где единственным проявлением в течение двух лет был лёгкий тремор рук, несмотря на наличие крупного очага в левой лобной области и меньших поражений в субкортикальном белом веществе[2].
При магнитно-резонансной томографии выявляются множественные или солитарные опухолевидные очаги. Супратенториальные поражения локализуются в перивентрикулярном белом веществе, фронтальной и теменной долях и височной доле. Наблюдаются очаги с полным или периферическим (кольцевидным) усилением после введения контраста. Присутствуют признаки перифокального отёка с минимальным масс-эффектом, неоднородная структура очагов, а также признаки ограничения диффузии. В спинном мозге редко выявляются неконтрастируемые очаги на уровне 2—3-го шейного, 1—2-го и 9-го грудного позвонков. Отсутствие патологических изменений в шейном и грудном отделах спинного мозга при наличии множественных очагов в головном мозге является более характерной диагностической особенностью данного заболевания[6].
Перфузионная динамическая магнитно-резонансная томография с тензорной диффузионной визуализацией: опухолеподобные демиелинизирующие очаги демонстрируют снижение показателя коэффициента диффузии и анизотропную диффузию при трактографии, что обусловлено деградацией миелина и наличием воспалительных инфильтратов. Метод трактографии позволяет дифференцировать патологии: при опухолях пирамидные тракты визуально искажаются, огибая массу образования, и могут демонстрировать незначительное снижение плотности волокон. В отличие от этого, при демиелинизирующих заболеваниях тракты сохраняют нормальное положение, но выглядят укороченными со значительным уменьшением плотности волокон и низкими значениями фракционной анизотропии[2].
Клинический анализ цереброспинальной жидкости: возможен плеоцитоз, повышение концентрации глюкозы[2].
Для постановки диагноза ПРС должны соблюдаться все следующие критерии[2]:
- Симптомы сохраняются более 24 часов и демонстрируют признаки прогрессирования.
- При магнитно-резонансной томографии (≥1,5 Тесла) выявляется один или несколько церебральных очагов, причём хотя бы один из них проявляет масс-эффект, с отёком или без него, и имеет размер ≥2 см в одном из измерений.
- Преимущественное вовлечение белого вещества.
- Очаг проявляется гиподенсными или изоденсными характеристиками.
- Клинические, лабораторные и нейровизуализационные находки не могут быть объяснены другими синдромами поражения центральной нервной системы.
Дифференциальная диагностика
Дифференциальная диагностика ПРС проводится со следующими состояниями[1][2]:
- абсцесс головного мозга;
- опухоль головного мозга;
- другие атипичные формы РС (острый рассеянный склероз Марбурга, рассеянный энцефаломиелит, оптиконейромиелит, концентрический склероз Бало).
Лечение
Препаратами первой линии терапии ПРС являются кортикостероиды, которые в большинстве случаев демонстрируют эффективность, уменьшая размер очагов. Однако не все пациенты реагируют на кортикостероидную терапию, у части больных сохраняются остаточные изменения, особенно при крупных размерах очагов. В таких случаях, при наличии противопоказаний или неэффективности кортикостероидов, применяются альтернативные методы лечения. Например, плазмаферез показал эффективность при стероид-резистентных демиелинизирующих заболеваниях центральной нервной системы, особенно при наличии кольцевидного контрастного усиления, масс-эффекта и перифокального отёка. Вероятность положительного ответа на плазмаферез выше при небольшой продолжительности заболевания и сохранённых сухожильных рефлексах[2].
Среди других терапевтических опций рассматриваются циклофосфамид и ритуксимаб, хотя доказательная база для их применения при ПРС остаётся ограниченной[2].
Применение натализумаба и финголимода при данной патологии противопоказано, поскольку зафиксированы случаи развития ПРС на фоне терапии этими препаратами[2].
Прогноз
Риск трансформации изолированного опухолеподобного демиелинизирующего очага при ПРС в РС варьирует в различных исследованиях. Согласно данным исследований, общий риск конверсии составляет примерно 30 % в течение 5 лет, в то время как другие работы сообщают о значительно более высоких показателях — до 67 и 81 %. Интересно, что случаи опухолеподобных очагов, которые впоследствии трансформировались в рассеянный склероз, демонстрировали благоприятный прогноз[2].
Примечания
Литература
- Белова Ю. А., Якушина Т. И., Рудакова И. Г. Псевдотуморозная форма рассеянного склероза с симптоматическими судорожными приступами (клиническое наблюдение) // Русский журнал детской неврологии. — 2015. — № 4.
- Якушина Т. И., Якушин Д. М., Штанг И. О. Острая псевдотуморозная воспалительная демиелинизация у пациентки, перенёсшей COVID-19 // Неврология, нейропсихиатрия, психосоматика. — 2021. — Т. 13, № 1S. — С. 57—61. — doi:10.14412/2074-2711-2021-1S-57-61.
- Yaser M. Al Malik. Tumefactive demyelinating lesions: A literature review of recent findings (англ.) // Neurosciences Journal. — 2024. — July (vol. 29, no. 3). — P. 153—160. — doi:10.17712/nsj.2024.3.20230111.
- Tosunoğlu B., Çokal B. G., Güneş H. N., Kaya N., Yoldaş T. K. Tumefactive multiple sclerosis (англ.) // Proceedings (Baylor University. Medical Center). — 2024. — February (vol. 37, no. 2). — P. 344—347. — doi:10.1080/08998280.2023.2289301. — PMID 38343475. — PMC PMC10857543.
- Fereidan-Esfahani M., Decker P. A., Weigand S. D., Lopez Chiriboga A. S., Flanagan E. P., Tillema J. M., Lucchinetti C. F., Eckel-Passow J. E., Tobin W. O. Defining the natural history of tumefactive demyelination: A retrospective cohort of 257 patients (англ.) // Annals of Clinical and Translational Neurology. — 2023. — September (vol. 10, no. 9). — P. 1544—1555. — doi:10.1002/acn3.51844. — PMID 37443413. — PMC PMC10502639.