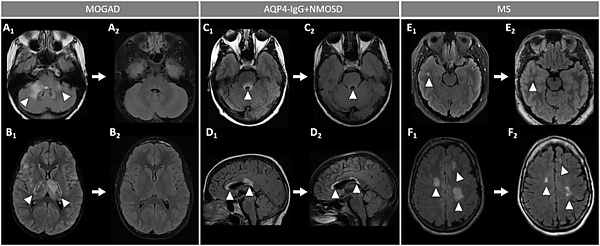
Болезнь антител к миелин-олигодендроцитарному гликопротеину
Боле́знь антите́л к миели́н-олигодендроцита́рному гликопротеи́ну (миели́н-олигодендроцита́рный гликопротеи́н-ассоции́рованное заболева́ние) является воспалительным демиелинизирующим заболеванием центральной нервной системы, в основе которого лежит продукция аутоантител миелин-олигодендроцитарному гликопротеину. Клинические проявления болезни антител к МОГ разнообразны и варьируются от изолированного неврита зрительного нерва или миелита до мультифокальной демиелинизации, часто в форме острого диссеминированного энцефаломиелита, или коркового энцефалита[1].
Общие сведения
История
Исторический интерес к миелин-олигодендроцитарному гликопротеину (МОГ) возник в 1980-х годах в связи с его идентификацией как потенциальной мишени для аутоантител к миелину центральной нервной системы в моделях экспериментального аутоиммунного энцефаломиелита. В 2003 году МОГ-IgM рассматривался в качестве возможного биомаркера для прогнозирования трансформации клинически изолированного синдрома в рассеянный склероз. Однако последующие исследования с использованием методов анализа на основе денатурированного белка МОГ продемонстрировали отсутствие специфичности МОГ-IgG. Антитела обнаруживались с сопоставимой частотой при рассеянном склерозе, иных демиелинизирующих заболеваниях центральной нервной системы и в контрольных группах. В 2007 году было установлено, что применение методов с использованием нативной трёхмерной конформации белка МОГ позволяет выявлять конформационно-чувствительные МОГ -IgG у пациентов с острым диссеминированным энцефаломиелитом и оптическим невритом, но не при рассеянном склерозе. Дальнейшие исследования с применением клеточных тестов с полноразмерным человеческим МОГ подтвердили наличие специфических антител при демиелинизирующих заболеваниях центральной нервной системы, отличных от рассеянного склероза[1].
Классификация
Болезнь относится к спектру демиелинизирующих заболеваний[1].
Этиология
Белок МОГ экспрессируется исключительно в центральной нервной системе, где составляет приблизительно 0,05 % от общего количества миелиновых белков. У человека обнаружено пятнадцать различных альтернативно сплайсированных изоформ данного белка. Биологическая роль MOG и его изоформ остаётся неясной. Согласно ограниченным исследованиям, белок может функционировать как клеточный рецептор, молекула адгезии или регулятор стабильности микротрубочек, являющихся компонентом цитоплазматического цитоскелета. Точная этиология развития болезни антител к МОГ также остаётся неустановленной[2].
Патогенез
Патогенез болезни антител к МОГ основан на нарушении иммунной толерантности к белку МОГ, что запускает аутоиммунный ответ против миелина центральной нервной системы. Ключевым механизмом является нарушение центральной и периферической толерантности из-за слабой экспрессии МОГ в тимусе, что препятствует элиминации МОГ-реактивных T-лимфоцитов. Их активация на периферии происходит под влиянием молекулярной мимикрии, сторонней активации при инфекциях или презентации МОГ-пептидов антигенпрезентирующими клетками. Инфекции усугубляют процесс, повышая уровень провоспалительных цитокинов и экспрессию молекул комплекса гистосовместимости II типа. Активированные МОГ-специфичные CD4+ T-клетки мигрируют через гемато-энцефалический барьер и повторно активируются в центральной нервной системе, что приводит к активации других иммунных клеток и созданию провоспалительной среды. Критическую роль играет гуморальный иммунитет: МОГ-IgG антитела (преимущественно IgG1), продуцируемые на периферии, проникают в центральную нервную систему. Их патогенность реализуется через опсонизацию МОГ, активацию комплемента, антителозависимую клеточную цитотоксичность и прямое воздействие на олигодендроциты. Патогенность антител усиливается в присутствии МОГ-специфичных T-клеток[3].
Нейропатологические особенности болезни антител к МОГ включают демиелинизацию, преимущественную потерю миелина с сохранением белка МОГ, внутрикорковую демиелинизацию, преобладание CD4+ T-лимфоцитов и гранулоцитарного воспаления, отложение комплемента в активных очагах белого вещества, частичное сохранение аксонов и реактивный глиоз[1].
Эпидемиология
Болезнь антител к МОГ относится к редкой патологии. По современным данным, общая заболеваемость составляет 0,16 случая на 100 000 населения в год. При этом среди детей она примерно в три раза выше (0,31 на 100 000 в год), чем среди взрослых. Согласно эпидемиологическим наблюдениям, болезнь антител к МОГ чаще диагностируется у лиц европеоидной расы. Средний возраст дебюта болезни антител к МОГ является наиболее молодым в спектре демиелинизирующих заболеваний центральной нервной системы и составляет около 31 года. В педиатрической практике болезнь антител к МОГ преимущественно развивается у детей в возрасте до 12 лет[2].
Диагностика
Клиническая картина болезни антител к МОГ характеризуется полиморфизмом проявлений у детей и взрослых[1]:
- оптический неврит представляет наиболее частое проявление заболевания. Для него характерно острое начало со значительным снижением остроты зрения, сопровождающееся болью при движениях глазного яблока. Примерно в половине случаев наблюдается одновременное двустороннее поражение или рецидивирующее течение. За несколько дней до развития зрительных нарушений многие пациенты отмечают появление интенсивной головной боли;
- в детском возрасте болезнь антител к МОГ проявляется энцефалопатией с нарушением сознания, когнитивными нарушениями, а также разнообразными очаговыми неврологическими симптомами в зависимости от локализации поражения. В тяжёлых случаях возможно развитие угнетения сознания, требующего респираторной поддержки;
- поражение ствола мозга может проявляться глазодвигательными нарушениями, бульбарным синдромом с дисфагией и дизартрией, а также вегетативными расстройствами. В редких случаях наблюдается тошнота, рвота и икота;
- характерно развитие двигательных нарушений в виде нижнего парапареза или тетрапареза, чувствительными расстройствами по проводниковому типу и выраженными тазовыми нарушениями, требующими катетеризации мочевого пузыря;
- корковый энцефалит проявляется эпилептическими припадками, которые могут переходить в эпилептический статус, выраженной головной болью и нарушением сознания вплоть до комы;
- в редких случаях заболевание сопровождается периферической нейропатией и поражением краниальных нервов.
Магнитно-резонансная томография: картина отличается вариабельностью и не имеет патогномоничных признаков, часто напоминая другие воспалительные заболевания центральной нервной системы. Однако некоторые особенности позволяют заподозрить данный диагноз[4]:
- поражение головного мозга демонстрирует высокую вариабельность. У детей часто наблюдается картина острого диссеминированного энцефаломиелита, в то время как у взрослых очаги в мозге на момент диагностики выявляются менее чем в половине случаев. Характерно наличие немногочисленных, но крупных очагов, обычно двусторонних, с нечёткими контурами. У детей чаще вовлекаются ядра ствола мозга. Легкоменингеальное усиление встречается редко, как изолированно, так и в сочетании с корковыми поражениями. Вариабельное паренхиматозное усиление может затрагивать ствол мозга, серое и белое вещество, перивентрикулярные области;
- поражение зрительных нервов наблюдается у большинства пациентов, обычно в виде двустороннего неврита с вовлечением передних отделов. Характерны выраженный отёк нервов, приводящий к их извитости и отёку диска зрительного нерва. Типичным признаком является оптический периневрит — воспаление оболочки зрительного нерва. Также может отмечаться периорбитальное и интраорбитальное усиление. Вовлечение хиазмы и зрительных трактов встречается нечасто;
- поражение спинного мозга обычно носит центральный характер, затрагивая как серое, так и белое вещество. Наблюдаются как протяжённые, так и короткие очаги, которые могут сочетаться. Поражение серого вещества формирует характерный Н-признак на аксиальных срезах и тонкие линейные сигналы на сагиттальных изображениях. Часто преимущественно поражается нижний отдел спинного мозга. Важным дифференциальным признаком является лептоменингеальное усиление.
Оптическая когерентная томография (ОКТ) играет важную роль в диагностике неврита зрительного нерва и может быть полезна для подтверждения нейропатии, а также для дифференциации дифференциальной диагностики. В острой фазе неврита зрительного нерва часто наблюдается значительное утолщение перипапиллярного слоя нервных волокон сетчатки. В течение последующих 3—6 месяцев развивается прогрессирующее истончение как этого слоя, так и макулярного комплекса ганглиозных клеток и внутреннего плексиформного слоя. Истончение внутреннего плексиформного слоя обычно происходит раньше, в течение нескольких недель после атаки, в то время как истончение перипапиллярного слоя нервных волокон развивается медленнее, что может быть связано с постепенным разрешением отёка диска зрительного нерва[1].
Обнаружение антител МОГ-IgG возможно исключительно с использованием метода клеточного анализа с презентацией антигена на основе живых или фиксированных клеток с последующей визуализацией методом иммунофлюоресцентной микроскопии или проточной цитометрии[2].
Клинический анализ спинномозговой жидкости: характерен плеоцитоз. Наиболее высокие показатели отмечаются при вовлечении спинного мозга, менее выраженные — при поражении головного мозга и ствола, а наименьшие — при изолированном оптическом неврите[2].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями[2][4]:
- нейротуберкулез;
- нейроборрелиоз;
- нейросифилис;
- нейросаркоидоз;
- синдром Бехчета;
- подострая дегенерация спинного мозга;
- васкулиты;
- наследственная оптическая невропатия Лебера;
- лимфома;
- глиоматоз;
- паранеопластические синдромы;
- синдром задней обратимой энцефалопатии;
- прогрессирующая лейкоэнцефалопатия;
- инфекционный заболевания центральной нервной системы;
- рассеянный склероз;
- острый диссеминированный энцефаломиелит.
Осложнения
Наиболее распространённым неврологическим осложнением является нарушение функций тазовых органов, включая сфинктерные и эректильные дисфункции, которые наблюдаются примерно у трети пациентов[2].
Лечение
Лечение болезни антител к МОГ основывается на ограниченных данных и рекомендациях, разработанных преимущественно по аналогии с терапией других нейроиммунных расстройств. Подход к терапии включает два основных направления: купирование острых обострений и поддерживающее лечение для предотвращения рецидивов[2][3].
Для купирования острых обострений в качестве терапии первой линии применяется пульс-терапия высокими дозами кортикостероидов. В случаях недостаточной эффективности кортикостероидной терапии или при тяжёлом течении обострения рекомендуется проведение курса плазмафереза. Для часто рецидивирующих случаев рекомендуется комбинированная терапия, которая может включать пероральные кортикостероиды в сочетании с иммуносупрессивными препаратами или внутривенным иммуноглобулином[2][3].
Эффективность применения моноклональных антител, в частности ритуксимаба, является ограниченной. Значительная часть пациентов демонстрирует недостаточный ответ на эту терапию, включая быстрое восстановление пула В-лимфоцитов после лечения, что, вероятно, связано с особенностями патогенеза заболевания[2].
Прогноз
У половины взрослых пациентов с болезнью антител к МОГ заболевание имеет монофазное течение. Риск развития рецидивов снижается при сероконверсии — исчезновении антител к МОГ. В педиатрической практике течение болезни также преимущественно монофазное. Долгосрочный прогноз при болезни антител к МОГ в целом благоприятный. Необратимые нарушения зрения развиваются примерно у 8 % больных. Около 10 % пациентов требуют помощи при ходьбе в связи со стойкими неврологическими нарушениями[2].
Диспансерное наблюдение
Не разработано.
Профилактика
Профилактическая терапия назначается с учётом индивидуальных прогностических факторов, таких как вероятность повторных рецидивов и риск стойкой инвалидизации. При благоприятном прогнозе заболевания основой профилактической терапии является длительный приём пероральных кортикостероидов с очень медленным снижением дозировки[2].
Примечания
Литература
- Gaillard F., Agazzi G., Sharma R. et al. Myelin oligodendrocyte glycoprotein antibody-associated disease (MOGAD) (англ.) // Radiopaedia.org : Справочная статья. — doi:10.53347/rID-62038.
- Елисеева Д.Д., Васильев А.В., Шабалина А.А., Симанив Т.О., Захарова М.Н. Энцефаломиелиты, ассоциированные с антителами к миелин-олигодендроцитарному гликопротеину // Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски : Журнал. — 2020. — Т. 120, № 7—2. — С. 13—23. — doi:10.17116/jnevro202012007213.
- Sechi E., Cacciaguerra L., Chen J.J., Mariotto S., Fadda G., Dinoto A., Lopez-Chiriboga A.S., Pittock S.J., Flanagan E.P. Myelin Oligodendrocyte Glycoprotein Antibody-Associated Disease (MOGAD): A Review of Clinical and MRI Features, Diagnosis, and Management (англ.) // Frontiers in Neurology : Журнал. — 2022. — 17 June (vol. 13). — P. 885218. — ISSN 1664-2295. — doi:10.3389/fneur.2022.885218.