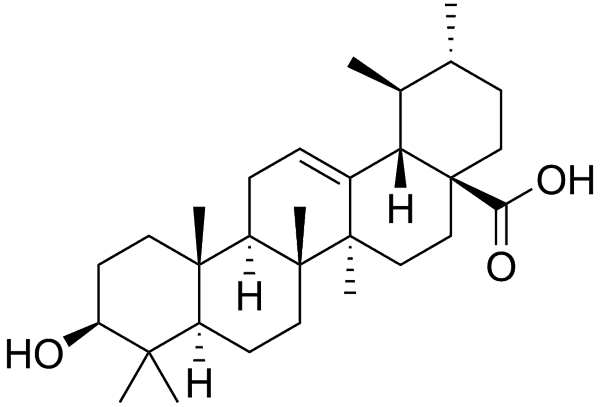
Сапонины
Сапонины — сложные безазотистые[1] органические соединения из гликозидов растительного происхождения с поверхностно-активными свойствами. Растворы сапонинов при взбалтывании образуют густую стойкую пену. Название происходит от латинского sapo (род. падеж saponis) — мыло[2]. Широко распространены в природе, встречаются в различных частях растений — листьях, стеблях, корнях, цветах, плодах[3]. Содержат агликон (сапогенин) и углеводную часть[2].
Для выделения группы сапонинов из других вторичных метаболитов используются свойства поверхностной активности и гемолитической активности. Однако не все сапонины могут ими обладать. Поэтому вещества могут помещать в группу сапонинов на основе структурной формулы (стероидные и терпеноидные гликозиды)[4].
Из-за сапониновых свойств (поверхностная и гемолитическая активность, образование комплексов с холестерином) к сапонинам часто относят также гликозиды азотсодержащих стероидных алкалоидов (гликоалкалоиды)[5].
Многие сердечные гликозиды (карденолиды) дают пену в водных растворах, однако из-за специфических биологических свойств к сапонинам не относятся, а рассматриваются отдельно[6].
Физические свойства
Сапонины — бесцветные или желтоватые аморфные вещества без характерной температуры плавления (обычно с разложением). Оптически активны[2]. Гликозиды растворимы в воде и спиртах, нерастворимы в органических растворителях; свободные сапогенины, наоборот, не растворяются в воде и хорошо растворимы в органических растворителях. В кристаллическом виде получены представители, которые имели в своем составе не более 4 моносахаридных остатков. С увеличением количества моносахаридов повышается растворимость сапонинов в воде и других полярных растворителях. Сапонины с 1—4 моносахаридными остатками в воде растворяются плохо.
Специфическим свойством сапонинов является их способность снижать поверхностное натяжение жидкостей (воды) и давать при встряхивании стойкую обильную пену.
Агликоны сапонинов (Сапогенины), как правило, являются кристаллическими веществами с чёткой температурой плавления, и в отличие от сапонинов, не обладают гемолитической активностью и не токсичны для рыб[7].
Химические свойства
Химические свойства сапонинов обусловлены структурой агликона, наличием отдельных функциональных групп, а также присутствием гликозидной связи.
Сапонины делят на нейтральные (стероидные и тетрациклические тритерпеновые) и кислые (пентациклические тритерпеновые) соединения. Их кислотность обусловлена наличием карбоксильных (-СООН) групп в структуре агликона и присутствием уроновых кислот в углеводной цепи[8]. Гидроксильные группы могут быть ацилированы уксусной, пропионовой, ангеликовой и др. кислотами[9].
Кислые сапонины образуют соли, растворимые с одновалентными и нерастворимые с двухвалентными и многовалентными металлами[8]. При взаимодействии с кислотными реагентами (SbCl3, SbCl5, FеСl3, конц. H2SO4) образуют окрашенные продукты[10][11].
Сапонины гидролизуются под влиянием ферментов и кислот. Производные с О-ацилгликозидными связями гидролизуются под воздействием щелочей[8].
Многие сапонины образуют молекулярные комплексы с белками, липидами, стеринами, танинами[8].
Разновидности агликонов
В зависимости от химического строения агликона все сапонины классифицируют на стероидные и тритерпеновые. Стероидные сапонины синтезируются из холестерина и содержат 27 атомов углерода[12]. Тритерпеновые сапонины синтезируются напрямую из сквалена, при этом во время их циклизации не происходит потерь атомов углерода, они содержат по 30 атомов углерода[7].
Стероидные сапонины
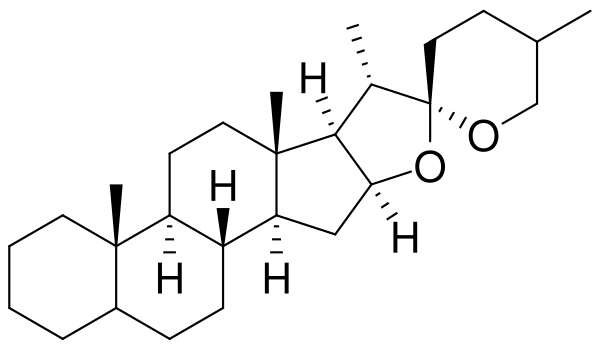
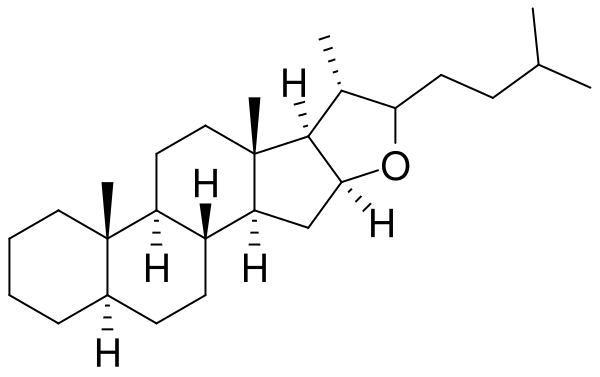
Стероидные сапонины в качестве сапогенинов содержат обычно производные спиростана или фуростана. Поскольку они, как правило, являются производными спиртов, содержащих в 3-м положении гидроксил, то их называют спиро- и фуростаноловыми гликозидами[13].
Спиростаноловые сапогенины, в основном, содержат 27 атомов углерода. Углеводная часть молекулы стероидных сапонинов присоединяется к 3-гидроксилу и может содержать 1-6 моносахаридов (D-глюкоза, D-галактоза, D-ксилоза, L-рамноза, L-арабиноза, галактуроновая и глюкуроновая кислоты). Известны сапонины, содержащие остатки D-хиновозы, D-апиозы и D-фукозы. Моносахариды могут образовывать как линейные, так и разветвленные цепи. Встречаются также гликозиды с углеводным компонентом при атомах С-1, С-2, С-5, С-6, С-11. Углеводных цепей может быть одна (вещества называются монодесмозиды), две (бидесмозиды)[14], редко три (тридесмозиды)[15]. Ацильная группа (остатки уксусной, бензойной, 2-гидрокси-2-метилглутаровой, серной кислот) может находиться как в сапогенной, так и в углеводной частях молекулы[14]. Некоторые спиростанолы образуют труднорастворимые комплексы с холестерином[16]
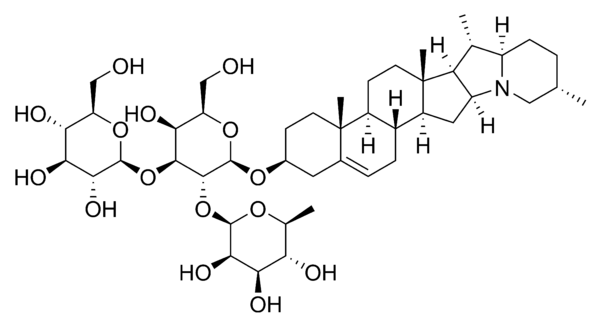
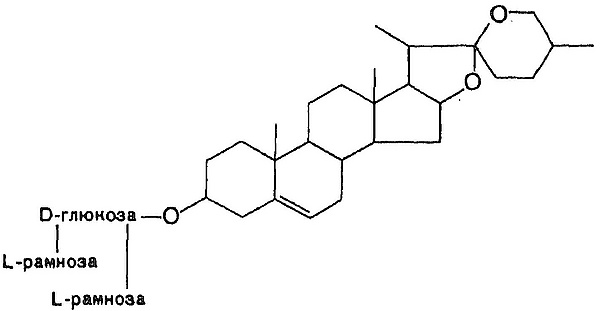
Один из важных представителей спиростаноловых гликозидов — диосцин, состоящий из сапогенина диосгенина и трёх гликозидов в разветвлённой цепи. Диосцин, в частности, содержится в корневищах видов диоскореи Dioscorea [17]. Диосгенин играет важную роль в фармацевтике, как сырьё для производства кортикоидных препаратов[18].
Сапонины ряда фуростанола, как правило, содержат углеводную цепь при С-3 и остаток D-глюкозы при С-26[14]. Отщепление остатка сахара от С-26 под действием кислот или ферментов приводит к спиростаноловым сапонинам[19]. Фуростанолы не осаждают холестерин[16], обладают повышенной по сравнению со спиростанолами гидрофильностью[20] и пониженной поверхностной активностью[16].
Для спиростаноловых сапонинов характерно гемолитическое, гипохолестеринемическое, канцеролитическое, а также фунгицидное, антимикробное[21], моллюскоцидное действие[22]. У фуростаноловых гораздо слабее выражена гемолитическая[23] и фунгицидная активность[24], зато повышены антиоксидантные свойства[22]; они обладают иммуномодулирующими и анаболическими свойствами[25]. Фуростаноловые и спиростаноловые гликозиды влияют на репродуктивную систему животных, оказывая как стимулирующее, так и контрацептивное действие[26].
Стероидные гликозиды — способ защиты растений от патогенов[27]. Фуростаноловые гликозиды повышают всхожесть, скорость прорастания растений и устойчивость их к биотическим и абиотическим стрессам[28], изменяют состав каротиноидных пигментов фотосинтеза[29].
Стероидные гликозиды синтезируются в листьях растений в фуростаноловой форме. Затем они транспортируются по всему растению и накапливаются в идиобластах (специализированных клетках) эпидермиса листьев и стеблей. Основная масса гликозидов транспортируется в корневище (орган вегетативного размножения), где гликозидаза переводит их в спиростаноловую (активную) форму. В надземных органах гликозидаза располагается поблизости от идиобластов (в мезофилле). При повреждении ткани быстро образуются спиростаноловые гликозиды. Таким образом, при защите от патогенов в надземных органах работает стратегия полуиндуцибельных защитных соединений[30].
Стероидные гликозиды могут применяться как основа для синтеза лекарственных стероидных гормонов[31], как гербициды, антигрибные и антидрожжевые препараты (а также консерванты пищевых продуктов, содержащих грибы), эмульгаторы и пенообразователи[32].
Тритерпеновые сапонины
Тритерпеновые сапонины содержат 30 атомов углерода и отличаются большим разнообразием химических структур (среди тритерпеноидов выделяют не менее 30 групп[33]). В зависимости от количества пяти- и шестичленных колец в структуре агликона их можно разделить на 2 группы[34]:
а) тетрациклические — содержат в структуре агликона 4 углеродных кольца;
б) пентациклические — содержат в структуре агликона 5 углеродных колец.
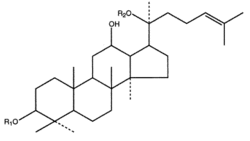
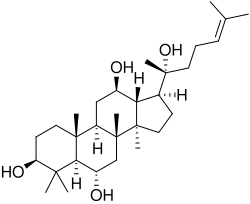
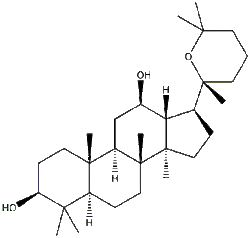
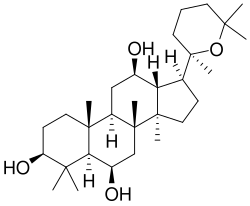
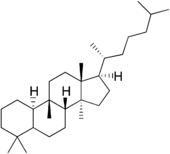
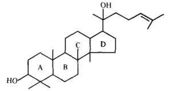
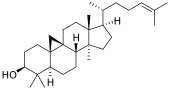
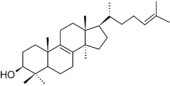
Тетрациклические сапонины относятся к группам даммарана, циклоартана, ланостана, кукурбитана[35] и др.
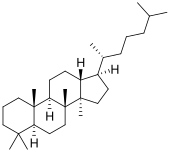
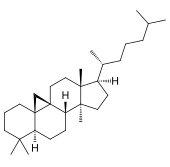
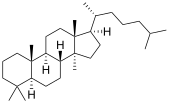
| Структурная основа | Даммаран | Циклоартан | Ланостан | Кукурбитан |
|---|---|---|---|---|
 |
 |
 |
| |
| Химическая основа | Даммарандиол | Циклоартенол | Ланостерол | |
 |
 |
 |
Эти соединения обнаружены в женьшене[36], березе[37][38]. Гликозиды женьшеня являются производными двух агликонов: панаксадиола и панаксатриола[39].
Вначале синтезируются гликозиды на основе протопанаксодиола и протопанаксотриола. При кислом гидролизе происходит отщепление углевода R2, боковая цепь замыкается в гетероцикл, образуются панаксадиол и панаксатриол[40].
Гликозиды женьшеня содержат в углеводных цепях от 3 до 6 моносахаридных остатков (глюкозы, рамнозы, арабинозы, ксилозы). Почти все гликозиды имеют по 2 углеводные цепи, соединенные с агликоном обычными гликозидными связями. Это их отличает от типичных пентациклических тритерпеновых сапонинов, в которых (при наличии двух углеводных цепей) одна присоединяется О-ацил-гликозидной связью[39].
Сапонины женьшеня в России называют панаксозидами, а в Японии — гинзенозидами[36], по латинскому названию женьшеня Panax ginseng.
Как лекарственное растение женьшень известен на Востоке более 1000 лет. Корень женьшеня применяют как стимулирующее и тонизирующее средство. Показано влияние женьшеня на реактивность организма, обмен веществ, гонадотропное и антидиуретическое действие[41]. Ряд панаксозидов стимулируют синтез инсулина в β-клетках поджелудочной железы у мышей с диабетом[42].
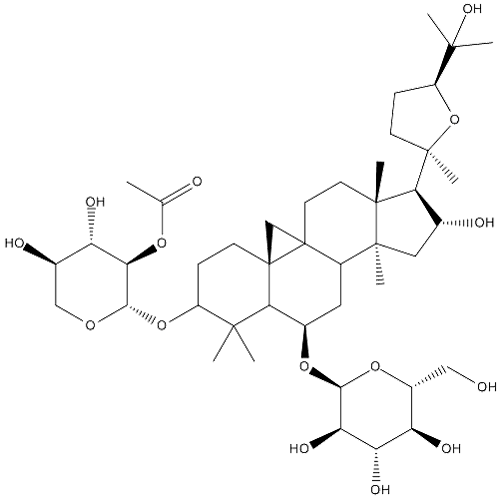
Гликозиды производных циклоартана обнаружены в растениях, принадлежащих большей частью к семействам Лютиковых:
- василистник — таликтозиды, циклофоэтозиды, скваррозиды;
- цимицифуга — шенгманол, цимигенол, дагуринол;
- воронец (растение);
- Beesia — бизиозиды;
и Бобовых:
- астрагал — астрагалозиды, орбикозиды;
- абрус — абрузозиды;
- остролодочник.
Производные циклоартана встречаются в семействах Мареновых (муссенда) и Страстоцветных: страстоцветы — квадрангулозид, пассифлорин[43][44].
Углеводными их компонентами являются D-ксилоза, D-глюкоза, D-галактоза, L-арабиноза, L-рамноза; пентозы встречаются чаще, чем гексозы. Циклоартановые чаще встречаются в форме би- и тридесмозидов.
Растения родов Цимицифуга и Астрагалус издавна используются в народной медицине, для получения успокоительных и гипотензивных средств. Растения рода Астрагалус используются и в научной медицине. Показана гипохолестеринемическая, гипотензивная, диуретическая, кардиотоническая и антивоспалительная активность астрагалозидов.[45]
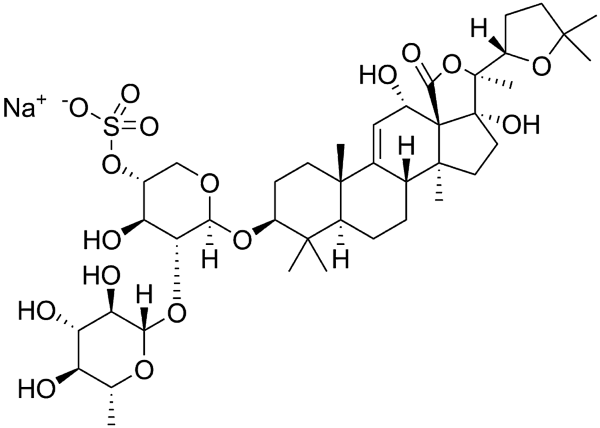
Поскольку ланостерол — одно из промежуточных соединений при синтезе стероидных веществ, то ряд веществ со структурой на основе ланостана иногда выделяют в отдельные группы (например, голостаны).
Голостаны — производные ланостана, имеющие в структуре лактонное кольцо. Они обнаружены в морских организмах отряда Голотурий (морские огурцы). Среди голостанов часто встречаются сульфатированные формы; в углеводной части присутствуют фукоза и хиновоза, метилглюкоза и метилксилоза. Голотоксины, голотурины, эхинозиды и др. служат защитой от морских хищников, показана также их антимикотическая активность.[46][47]
Ланостановые гликозиды эрилозиды обнаружены в губках Erylus[48].
Ланостановые производные содержатся и в растениях. В эвкомисе, пролеске, хионодоксе, Muscari paradoxum обнаружены сцилласапонины; ланостановые гликозиды хионодоксы и Muscari обладают цитотоксичностью[49]; марианозиды расторопши пятнистой способны ингибировать протеазу химотрипсин[50].
Ряд ланостановых гликозидов обнаружен в грибах: лэтипозиды из Laetiporus versisporus[51], аскостерозид из Ascotricha amphitricha имеет антимикотическую активность[52], фомитозиды из трутовика окаймлённого проявляют антивоспалительные свойства[53], для дедалиозидов из дедалеи Дикенса показана цитотоксичность к опухолевым клеткам[54].
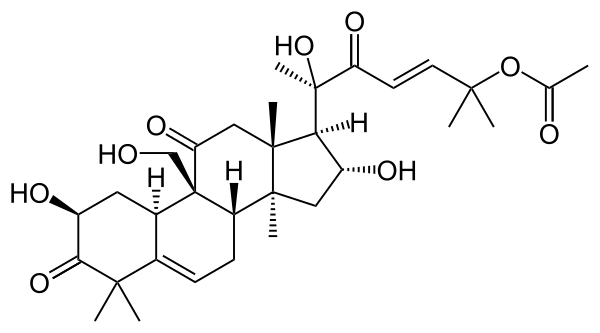
В бахчевых культурах и других растениях семейства Cucurbitaceae содержатся сапонины тритерпенового ряда, обладающие горьким неприятным вкусом. Сапогенины этих сапонинов — кукурбитацины[2].
Кукурбитановые — довольно сильно окисленные агликоны и гликозиды. Циклы и боковые цепи содержат много кислородсодержащих функциональных групп.
Кукурбитацины известны своими вкусовыми свойствами. Глюкозиды обычно безвкусны, но могут иметь и сладкий вкус (например, могрозиды из Sirattia grosvenori[55]). Агликоны очень горькие, выполняют функцию репеллентов (хотя некоторые насекомые, приспосабливаясь, используют их как пищевые аттрактанты и стимуляторы).[56]
Кукурбитацины обнаружены в ряде других семейств растений, у нескольких родов грибов и в морском моллюске. Кукурбитацины обладают широким спектром биологических свойств (противоопухолевые, противозачаточные, антивоспалительные, антимикробные и антигельминтовые и др.) Однако из-за своей неспецифической токсичности в традиционной медицине они имеют ограниченное применение.[55]
Пентациклические тритерпеновые сапонины содержатся не менее чем в 70 семействах, типичны более чем для 150 родов[7].
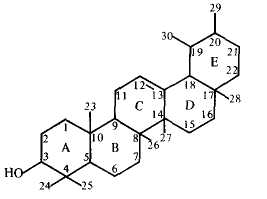
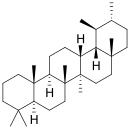
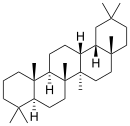
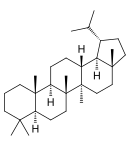
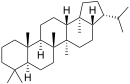
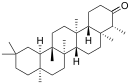
Пентациклические агликоны делят на группы производных различных структур. Наиболее распространены производные олеанана, урсана и лупана[57] (приводятся также структуры гопана и фриделина).
| Структурная основа | Урсан | Олеанан | Лупан | Гопан | Фриделин |
|---|---|---|---|---|---|
 |
 |
 |
 |
| |
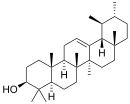
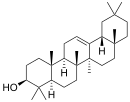
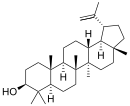
| Химическая основа | α-амирин | β-амирин | Лупеол | ||
 |
 |
 |
Из функциональных групп у них встречаются гидроксильные, карбоксильные, альдегидные, лактонные, эфирные и карбонильные группы. Двойная связь наиболее часто встречается в положении 12—13[34].
У производных β-амирина, α-амирина и лупеола, если имеется один гидроксил, то он находится у С-3, у фриделина в положении 3 — карбонильная группа. Карбоксильная группа, если она одна, чаще всего бывает у С-28, но может быть и при других углеродных атомах. Отдельные сапогенины могут иметь одновременно разные функциональные группы. Сапогенины, содержащие альдегидную, лактонную группы или сложноэфирные связи, неустойчивы и могут изменяться уже в процессе выделения из растений[34].
Углеводная часть тритерпеновых сапонинов обычно присоединяется к агликону в 3 положении за счет гидроксильной (-ОН) группы, в 28 положении за счет карбоксильной (-СООН) группы (ацилгликозидная связь)[58]; распространены бидесмозиды[59], известны тридесмозиды[60]. Углеводная часть тритерпеновых гликозидов может содержать 1-11[58] моносахаридов (D-глюкоза, D-галактоза, D-ксилоза, L-рамноза, L-арабиноза, L-фукоза, D-глюкуроновая и D-галактуроновая кислоты). Она может быть линейной и разветвленной. Разветвление углеводной цепи происходит от первого сахарного остатка, связанного с агликоном[34]. У фриделинов гликозидных форм не обнаружено[35].
Возможно, для биосинтеза фриделиновых тритерпеноидов исходным соединением является β-амирин; при этом происходит серия миграций метильных групп и водородных атомов от кольца А[7].
Большинство пентациклических тритерпеновых сапонинов относится к типу β-амирина, в основе которого лежит углеродный скелет олеанана.
| Сапогенин | Пример гликозида |
|---|---|
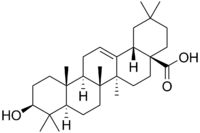
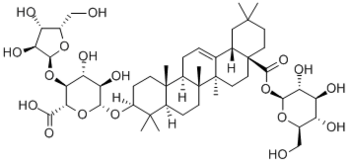
| Олеаноловая кислота | Аралозид A |
 |
|
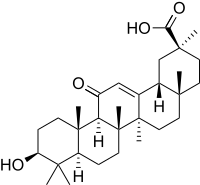
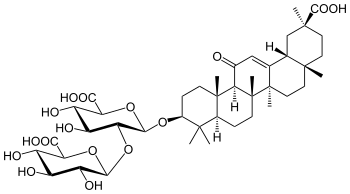
| Глицерритиновая кислота | Глицирризиновая кислота |
 |
|
| Протопримулагенин А | Примуловая кислота I |
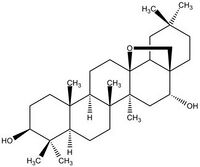 |
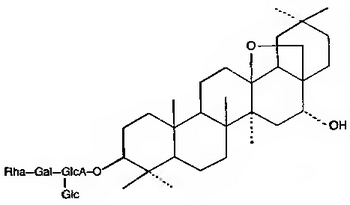
|
| Эсцин | |
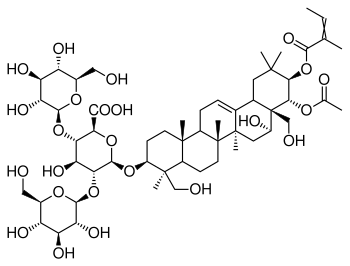
| |
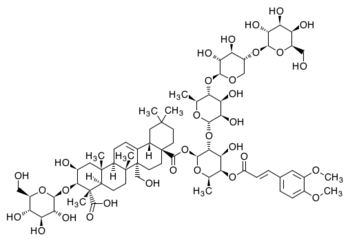
| Полигаловая кислота | Сенегин II |
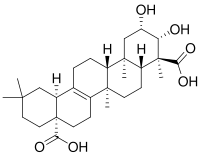 |
|
Одним из наиболее распространённых представителей является олеаноловая кислота[57]. Олеаноловая кислота является агликоном аралозидов аралии манчжурской[61], сапонинов календулы лекарственной[62], патринии средней[63][64].
Другим фармакологически значимым основанием является глицирретиновая кислота. Глицирретиновая кислота является агликоном глицирризиновой кислоты (в 3 положении присоединяется углеводная цепь из двух молекул глюкуроновой кислоты). Глицирризиновая кислота содержится в солодке голой и солодке уральской. Препараты на основе глицирризиновой кислоты используются при гипофункции коры надпочечников [65].
β-амирин также является структурной основой эсцина (конский каштан)[66], примуловой кислоты (первоцвет весенний)[67], полигаловой (от Polygala — истод) кислоты и сенегинов истода[68], сапонинов синюхи голубой[69].
α-амирин лежит в основе различных соединений, которые содержатся в почечном чае (ортосифон тычиночный)[70], лапчатке прямостоячей[71][72][73]. Одним из наиболее важных представителей является урсоловая кислота.
Урсоловая кислота обнаружена не менее, чем в сотне растений[74], в том числе бруснике обыкновенной[75], клюкве болотной[76], причем встречается как в виде гликозидов, так и свободного агликона[75]. Известны её антимикробные, гепатопротекторные, антивоспалительные, антиаллергические, антивирусные, цитотоксические, противоопухолевые свойства.[74]
Кроме лупеола, к лупановым производным относятся бетулин и бетулиновая кислота.
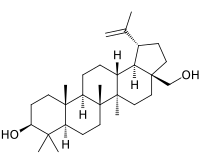
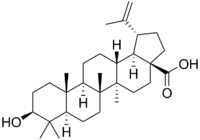
| Бетулин | Бетулиновая кислота |
|---|---|
 |
|
Бетулин содержится в коре берёзы, он обеспечивает её белый цвет. Обнаружен бетулин и в других растениях семейства берёзовых (лещине, грабе, ольхе). Является ценным компонентом косметических продуктов.
Бетулиновая кислота также обнаруживается во многих видах растений, однако, в небольших концентрациях. Показана её избирательная противоопухолевая активность. Бетулиновая кислота и её производные защищают клетки от репликации ВИЧ.
Лупеол, бетулин и бетулиновая кислоты обладают противовоспалительной активностью, возможно, вследствие того, что лупановые производные способны взаимодействовать с глюкокортикоидными рецепторами.[77]
Гликоалкалоиды
Стероидные алкалоиды представляют собой химические вещества, в основе которых лежат стероидные соединения. Однако в структуре их гетероциклов присутствует атом азота, что обеспечивает им щелочные свойства. Гликоалкалоиды (гликозиды стероидных алкалоидов) обнаружены, в основном, в семействе Паслёновые (картофель, томаты) и найдены у представителей семейства Лилейные (чемерица, рябчик).
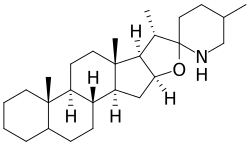
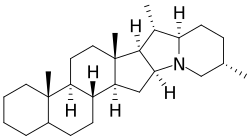
По структуре агликонов у стероидных алкалоидов выделяют группы спиросолановых и соланидановых алкалоидов. Атом азота в них является вторичным (спиросоланы) или третичным (соланиданы). Спиросоланы являются азотными аналогами спиростанов; у соланиданов атом азота входит в индолизидиновую структуру. Углеводные части некоторых гликоалкалоидов получили собственные тривиальные названия.
| Спиросолан | Соланидан |
|---|---|
 |
|
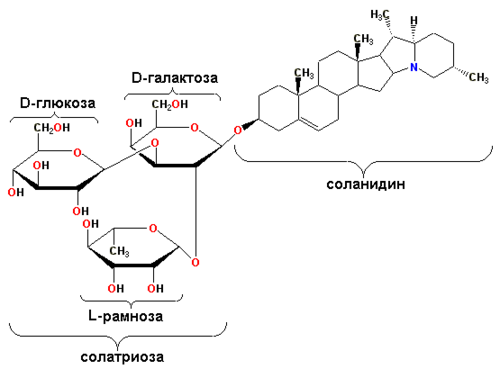
Примером гликоалкалоида картофеля служит соланин (генин — соланидин).
| Соланин |
|---|
|
Другим гликозидом соланидина является хаконин (гликозидная часть — β-хакотриоза — состоит из двух рамноз и одной глюкозы). Хакотриоза и солатриоза являются также углеводными компонентами лептининов и лептинов у соланидановых агликонов лептинидина и ацетил-лептинидина соответственно.
Спиросолановый агликон картофеля — соласодин, его гликозиды — соласонин (глюкоза, рамноза и галактоза), соламаргин (две рамнозы и одна глюкоза), содержатся в видах рода Solanum, солаплюмбин (глюкоза и рамноза) обнаружен у Nicotiana plumbaginifolia.
Томатидин — спиросолановый агликон, обнаруженный в томатах и картофеле. Его производным является томатин (ксилоза, 2 глюкозы и галактоза). Такой же углеводный остаток (β-ликотетраоза) у демиссина, производного соланиданового агликона демиссидина.
Известна токсичность гликоалкалоидов для человека. Гидролиз их в желудочно-кишечном тракте приводит к формированию безвредных агликонов. В случае же их прямого введения их эффект сходен с действием сердечных гликозидов, они могут привести к параличу нервной системы и смерти. Они не уничтожаются при кипячении, жарке или высушивании при высоких температурах. Наибольшие их количества содержатся в зелёных клубнях, листьях и плодах.
Гликоалкалоиды обладают фунгицидными (томатин, соланин), моллюскоцидными (томатин, соласонин, соламаргин), инсектицидными (демиссин, томатин, соланин, хаконин, лептины, соламаргин, соласонин), противоопухолевыми (соламаргин, соласонин, соланин, солаплюмбин), антивоспалительными (соласодин, томатин) свойствами.[78]
Биосинтез сапонинов
Биосинтез сапонинов происходит по изопреноидному пути синтеза тритерпенов и стероидов (см. Биосинтез холестерина). 3 изопреновых 5-углеродных единицы соединяются «голова-к-хвосту» в 15-углеродный фарнезилдифосфат. Два фарнезилдифосфата затем объединяются «хвост-к-хвосту» в 30-углеродный сквален. Сквален затем окисляется до оксидосквалена. Эта точка является исходной для многочисленных реакций циклизации тритерпеноидного биосинтеза. Оксидосквален циклизуется после протонирования и раскрытия эпоксидного кольца. В результате образуется карбокатион, подвергающийся циклизации и последующим перестройкам: гидридным сдвигам и метильным миграциям, в результате которых образуются новые карбокатионы. Нейтрализация карбокатионов происходит при удалении протона — образуется двойная связь или циклопропановое кольцо, а также при реакции с водой — образуется гидроксильная группа. Конкретные типы скелетов и их стереохимия определяются участвующими в реакциях типами циклаз: циклоартенолсинтаза, ланостеролсинтаза, β-амиринсинтаза и др.[35]
Физиологическое действие
Исследования сапонинов класса естественных продуктов показали их комплексообразование с холестерином, с формированием поры в двойных слоях мембраны клетки, например, в мембране эритроцита. Такое комплексообразование приводит к гемолизу при внутривенной инъекции. Оболочка из полупроницаемой становится проницаемой. Гемоглобин свободно поступает в плазму крови и растворяется в ней. На проницаемость мембран и гемолитическую способность влияет структура сапонина, количество и строение активных групп[79]. Усиливают проникновение белков и других макромолекул через клеточные мембраны[80].
Гемолитической активностью обладают только гликозиды[7]. При попадании в кровь сапонины токсичны, поскольку вызывают гемолиз эритроцитов. При приеме внутрь, как правило, менее токсичны[81] вследствие гидролиза гликозидов; однако сапонины мыльного дерева (Sapindus) при проглатывании могут вызвать у некоторых людей крапивницу.
Сапонины высокотоксичны для животных, дышащих жабрами. Они нарушают функцию жабр, которые являются не только органом дыхания, но и регулятором солевого обмена и осмотического давления в организме[8][82]. Сапонины парализуют или вызывают гибель холоднокровных животных даже в больших разведениях (1:1 000 000)[83]. Агликоны сапонинов для холоднокровных животных не токсичны[7]. Рыба, отравленная сапонинами, остается съедобной. Эсцин и прочие сапонины конского каштана не токсичны для рыб.
Сапонины могут оказывать влияние на проницаемость растительных клеток. Определённые концентрации сапонинов ускоряют прорастание семян, рост и развитие растений, а в увеличенных концентрациях могут их тормозить. Особую роль выполняют в растениях фриделиновые тритерпены (фриделин, церин), поскольку они содержатся в лубе растений[7].
Сапонины оказывают раздражающее действие на слизистые оболочки глаз, носа, полости рта[8]. При легком раздражающем действии сапонинов происходит усиление секреции всех желез, что благоприятно сказывается на бронхах — ведет к разжижению мокроты, что облегчает и её эвакуацию[84]. Вместе с тем избыток сапонинов приводит к раздражению слизистой желудка и кишечника, они могут быть токсичными — вызывают тошноту, рвоту, диарею, головокружение[8].
Кардиотоническим, нейротрофным, гипотензивным и тоническим действием обладают аралозиды, календулозиды, патризиды, клематозиды[85].
Сапонины различных растений обладают и другими лекарственными действиями: гипохолестеринемическое и противосклеротическое, диуретическое[84]; кортикотропное[85]; адаптогенное, седативное[86]; противоязвенное[87]; легкое слабительное[67]. Кроме того, в присутствии сапонинов некоторые другие лекарственные вещества легче всасываются[88].
Применение
Благодаря способности сапонинов образовывать обильную пену, они находят некоторое применение в качестве детергентов и пенообразующих агентов в огнетушителях. Эмульгирующие свойства сапонинов широко используются для стабилизации разных дисперсных систем (эмульсий, суспензий). Их используют при приготовлении халвы и других кондитерских изделий, пива и иных шипучих напитков. Благодаря эмульгирующим свойствам сапонины оказывают моющее действие, но их отличает от анионных мыл отсутствие щелочной реакции[89].
Сапонины производятся коммерчески как пищевые и диетические добавки. В терапевтической практике используются как отхаркивающие, мочегонные, тонизирующие, седативные средства, применяются как вспомогательные средства в вакцинах. При этом токсичность, связанная с комплексообразованием стерола (стерина), остаётся главной проблемой.[90] Необходима большая осторожность в оценке терапевтической пользы при употреблении естественных продуктов, содержащих сапонин-разновидности.
Примечания
Литература
- Горовиц М. Б. Сапонины // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1995. — Т. 4: Полимерные — Трипсин. — С. 292—294. — 639 с. — 40 000 экз. — ISBN 5-85270-039-8.
- Физер Л., Физер М. Органическая химия. В 2-х томах. — М.: Химия, 1970. — Т. II. — 800 с.
- Ягодка В. С. Лекарственные растения в дерматологии и косметологии. — К.: Наукова думка, 1991. — 272 с.
- Тринус Ф. П. Фармако-терапевтический справочник. — 6-е изд. — К.: Здоров’я, 1989. — 640 с. — ISBN 5-225-04714-9.
- Муравьева Д. А., Самылина И. А., Яковлев Г. П. Фармакогнозия. — 4 изд. — М.: Медицина, 2002. — 656 с. — ISBN 5-225-04714-9.
- Физер Л., Физер М. Стероиды. — М., 1964.
- Augustin J. M., Kuzina V., Andersen S. B., Bak S. Molecular activities, biosynthesis and evolution of triterpenoid saponins (англ.) // Phytochemistry. — 2011. — Т. 72, № 6. — С. 435–457. — doi:10.1016/j.phytochem.2011.01.015.
- Hostettmann K., Marston A. Saponins. — Cambridge: Cambridge University Press, 1995. — ISBN 0-521-32970-1.
- Васильева И. С., Пасешниченко В. А. Стероидные гликозиды растений и культуры клеток диоскореи, их метаболизм и биологическая активность (рус.) // Успехи биологической химии. — 2000. — Т. 40, № 6. — С. 153—204. Архивировано 15 февраля 2017 года.