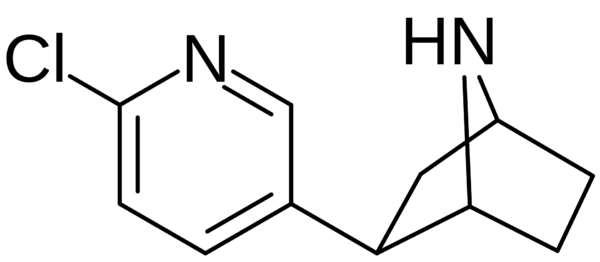
Эпибатидин
Эпибатиди́н (Epibatidine) — это хлорсодержащий высокотоксичный алкалоид пиридинового ряда с формулой C11H13ClN2, содержащийся в коже некоторых тропических лягушек Центральной и Южной Америки из семейства древолазов (лат. Dendrobatidae): вида пятиполосый древолаз (лат. Epipedobates anthonyi) из рода Epipedobates и представителей рода Ameerega.
Самый сильный природный анальгетик, нейротоксин. Анальгезирующий эффект превышает действие морфина примерно в 200 раз. Чрезвычайно токсичен. Из-за уникального сродства к никотиновым ацетилхолиновым рецепторам центральной нервной системы эпибатидин и его синтетические аналоги рассматривались как потенциальные неопиоидные обезболивающие препараты.
Общие сведения
| Эпибатидин | |
|---|---|
| Общие | |
| Систематическое наименование |
1R,2R,4S)-2-(6-хлорпиридин-3-ил)-7-азабицикло[2.2.1]гептан |
| Традиционные названия | Эпибатидин |
| Хим. формула | C11H13ClN2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 208,69 г/моль |
| Классификация | |
| Рег. номер CAS | 140111-52-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 3073763 |
| Рег. номер EINECS | 634-286-9 |
| SMILES | |
| InChI | |
| ChEBI | 4803 |
| ChemSpider | 10399316 |
| ECHA InfoCard | 100.162.281 |
| Безопасность | |
| ЛД50 | 1,4—1,5 мкг/кг (мыши, внутрибрюшинно) |
| Токсичность | чрезвычайно токсичен (яд) |
История
Эпибатидин открыт американским химиком Джоном У. Дейли в 1974 году в ходе исследования кожных экстрактов ядовитых лягушек Эквадора. Учёный и его коллега Чарльз Майерс совершили несколько экспедиций в эту страну с целью сбора образцов кожи лягушек. Вещество удалось выделить из кожи представителей вида пятиполосый древолаз (лат. Epipedobates anthonyi). Так как в то время на протяжении нескольких десятилетий шёл пересмотр таксономии семейства древолазов (лат. Dendrobatidae), в ранних работах по эпибатидину в качестве его источника указывался не вид Epipedobates anthonyi, а вид Epipedobates tricolor.
Исследованиям мешало то, что пятиполосому древолазу в 1984 году Международным союзом охраны природы был присвоен статус охраняемого вида («вид, близкий к уязвимому положению»); Конвенция о международной торговле видами дикой фауны и флоры, находящимися под угрозой исчезновения (CITES), запрещает вывоз таких животных.
С развитием аналитической химии, методов спектрометрии и ЯМР, в 1990-х годах, началось активное изучение соединения. В лаборатории Дейли, используя методы хроматографии, из остатков многолетнего экстракта (хранившегося с 1970-х годов) удалось выделить менее 1 миллиграмма чистого вещества. Тем не менее это позволило провести анализ структуры и полностью установить в 1992 году уникальное природное строение эпибатидина. Оказалось, что он содержит в себе хлор. Наличие хлора в природном алкалоиде — редкость.
Год спустя, в 1993 году, группой Криса Брока был осуществлён и опубликован первый полный синтез эпибатидина. Это позволило получать вещество в количествах, достаточных для проведения исследований.
Источники эпибатидина
- Лягушки из семейства древолазов (лат. Dendrobatidae): главным образом — вид пятиполосый древолаз (лат. Epipedobates anthonyi) из рода Epipedobates, населяющий влажные тропические леса Эквадора в Южной Америке (а также представители рода Ameerega из этого же семейства). Эпибатидин содержится в кожных железах лягушек и служит химической защитой от хищников. Выращенные в неволе, эти лягушки теряют токсичность. Следовательно, они не производят эпибатидин самостоятельно, а получают его из пищи, содержащей токсичные алкалоиды (видимо, из мелких жуков, клещей, муравьёв и др.).
- Химический синтез. Из-за высокой токсичности и сложности добычи эпибатидина из лягушек (менее 1 мкг на особь, защита природных популяций лягушек со стороны CITES) эпибатидин для научных и медицинских исследований получают путём химического синтеза в лабораториях.
Химическая структура и синтез
Эпибатидин является бициклическим алкалоидом, с присоединённым хлорсодержащим пиридиновым кольцом. В чистом виде представляет собой белое кристаллическое вещество. Хорошо растворим в органических растворителях (спирты, хлороформ). Отличается жёсткой стехиометрической структурой.
Классический синтез по Кори:
- Реакция Дильса — Альдера для формирования бициклического каркаса.
- Защита аминогруппы трифторуксусным ангидридом.
- Циклизация под действием трет-бутилата калия для создания азабициклогептановой системы.
- Введение хлорпиридинового фрагмента через палладий-катализируемое кросс-сочетание.
Помимо метода Кори, к числу известных методов относятся методы Брока[1], Хуана и Шена[2], а также Клейтона и Регана[3]. В 1999 году было опубликовано исследование о методе синтеза с использованием микробного гидроксилирования неактивированного углерода в 7-азанорборнане[4]. Известен метод синтеза эпибатидина, опубликованный в 2013 году Российским государственным научно-исследовательским институтом органической химии и технологии (препаративный способ)[5].
Фармакология
Механизм действия эпибатидина основан на его способности выступать в роли высокоаффинного агониста нейрональных никотиновых ацетилхолиновых рецепторов, в частности подтипа α4β2. Эти рецепторы играют ключевую роль в передаче болевых сигналов в центральной нервной системе. Другим механизмом действия эпибатидина является возможность связываться с мускариновыми ацетилхолиновыми рецепторами. Связываясь с рецепторами в головном и спинном мозге, он оказывает анальгетический эффект и подавляет большинство болевых импульсов.
В тесте «горячая пластина» на мышах эпибатидин показал анальгетическую активность, в 200 раз превышающую активность морфина[6] и в 30—120 раз — никотина. Эффективная доза (ED50) для грызунов составляет 0,005 мг/кг[7]. В отличие от морфина, эпибатидин не вызывает привыкания в краткосрочной перспективе и не угнетает дыхание в терапевтических дозах.
Токсикология
Терапевтическое применение чистого эпибатидина запрещено из-за высокой токсичности. Может вызывать судороги, гипертензию, двигательные нарушения, полное онемение тела, паралич. Средняя летальная доза, или ЛД50 (мыши, внутрибрюшинно): 1,4—1,5 мкг/кг (примерно в 200 раз токсичнее никотина).
Для эпибатидина характерен узкий терапевтический индекс. Доза, вызывающая обезболивающий эффект, немного меньше дозы (примерно в 5 раз), вызывающей летальный исход. Это делает эпибатидин непригодным для клинического применения.
Терапевтический индекс синтетических аналогов эпибатидина искусственно улучшен в ходе изменения молекулы.
Аналоги
- Тебаниклин ABT-594[8].
Первый и самый известный аналог эпибатидина, разработанный компанией Abbott Laboratories. ABT-594 сохранил высокую активность в отношении α4β2-рецепторов, но потерял сродство к мышечным подтипам, что сделало его значительно менее токсичным. На этапе второй фазы клинических испытаний тебаниклин вызвал отрицательное действие на желудочно-кишечный тракт и центральную нервную систему. В результате разработка препарата была приостановлена[9].
- Эпибоксидин.
Учёные из Института органической химии имени Н. Д. Зелинского РАН совместно с коллегами из США создали эпибоксидин, в котором один из атомов углерода в молекуле эпибатидина был заменён на атом кислорода, что привело к образованию оксабициклической структуры. Эпибоксидин показал ещё более высокую селективность к α4β2- и α7-подтипам рецепторов, чем ABT-594[10].
- Флюбатин.
Фторированный аналог.
Применение и исследование
- Радиоактивно меченный эпибатидин ([3H]-Epibatidine) используется в авторадиографии для визуализации плотности никотиновых рецепторов в мозге[11]. Способствует пониманию распределения никотиновых рецепторов в мозге, что необходимо для исследования механизмов работы нервной системы.
- Эпибатидин — перспективный диагностический маркер при болезнях Альцгеймера и Паркинсона. Снижение связывания эпибатидина в мозге коррелирует с потерей холинергических нейронов[12].
- Фармакофорное моделирование. Особенность структуры молекулы эпибатидина служит шаблоном для химического компьютерного моделирования активного центра рецептора[12].
Примечания
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |