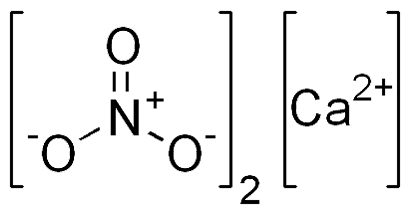
Нитрат кальция
Ка́льция нитра́т, ка́льциевая сели́тра, азотноки́слый ка́льций, норве́жская сели́тра — неорганическое вещество, соль азотной кислоты, широко применяемая в сельском хозяйстве в качестве щелочного азотного удобрения, а также в строительстве, пиротехнике, производстве реактивов и стеклопластиков. Химическая формула соединения — Са(NО3)2. Это первое синтетическое азотное удобрение, произведённое в промышленных масштабах в Норвегии (одно из названий — «норвежская селитра»), которая является одним из главных производителей вещества в мире[1]. В агрономии ценится за способность улучшать структуру почвы, стимулировать рост растений и повышать устойчивость культур к заболеваниям, особенно к вершинной гнили томатов. Из-за высокой гигроскопичности, кальциевую селитру хранят без доступа влаги[2][3][4].
Общие сведения
| Нитрат кальция | |
|---|---|
| Общие | |
| Традиционные названия | кальциевая селитра, норвежская селитра, азотнокислый кальций |
| Хим. формула | CaN2O6 |
| Физические свойства | |
| Состояние | гранулы сферической формы белого, светло-серого, светло-бежевого цвета |
| Молярная масса | 164,088 г/моль |
| Плотность |
(безводная) 2,504 г/см³; (тетрагидрат) 1,896 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления |
(безводная) 561 °C; (тетрагидрат) 42,7 °C |
| • кипения |
(безводная) разлагается; (тетрагидрат) 132 °C |
| • вспышки | негорючая °C |
| Мол. теплоёмк. | 149,33 Дж/(моль·К) |
| Энтальпия | |
| • образования | -937,2 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде |
Безводной: 121,2 г/100 мл (20 °C); 271,0 г/100 мл (40 °C); 359 г/100 мл (51,6 °C). Тетрагидрата: 102 г/100 мл (0 °C); 129 г/100 мл (20 °C); (100 °C) 363 г/100 мл |
| • в | спирте и ацетоне |
| Структура | |
| Кристаллическая структура |
кубическая (безводная) моноклинная (тетрагидрат) |
| Классификация | |
| Рег. номер CAS |
10124-37-5 (безводная) 13477-34-4 (тетрагидрат) |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 24963 |
| UNII | NF52F38N1N |
| CompTox Dashboard EPA | DTXSID1039719 |
| Рег. номер EINECS | 233-332-1 |
| SMILES | |
| InChI | |
| RTECS | EW2985000 |
| ChEBI | 64205 |
| Номер ООН | 1454 |
| ChemSpider | 23336 и 21500286 |
| ECHA InfoCard | 100.030.289 |
| Безопасность | |
| NFPA 704 | |
История происхождения
Изначально синтез кальциевой селитры не был связан с агрономией. Первооткрыватели стремились получить компонент для производства пороха. Существует гипотеза, что принцип создания вещества был подсмотрен человеком в природе: естественные соединения извести и органического азота обнаруживались на стенах пещер в виде минерала нитрокальцита[5][3]. Позже было замечено, что добавление извести в так называемые «селитряные ямы» приводит к образованию нитрата кальция, который неожиданно проявил себя как эффективный стимулятор роста культурных растений[6]. Кальциевая селитра была первым синтетическим азотным удобрение, производство которого наладили в Норвегии в 1905 году (отсюда название «норвежская селитра»[1].
Свойства
Кальциевая селитра представляет собой водорастворимое кристаллическое вещество белого цвета без запаха и вкуса, хорошо растворимого в воде[3][7].
Молярная масса тетрагидрата нитрата кальция — 236,15 г/моль, безводного — 164,088 г/моль.
Вещество представляет собой соль азотной кислоты и гидроксида кальция. Соответственно, оно имеет все свойства, характерные для солей кислот.
Например,
Ионы кальция образуют устойчивые соединения с краун эфирами.
При 500 °C начинает разлагаться с выделением О2 и образованием сначала Ca(NO2)2, а затем СаО и NO2.
Кальциевая селитра при нормальных условиях негорючая, пожаро- и взрывобезопасная, устойчивая в интервале температур от −60 °C до +155 °C.
Производство
Выпускается в форме порошка или гранул[3][7]. В промышленных масштабах кальциевую селитру получают методом низкотемпературной нейтрализации 40—48%-ной азотной кислоты мелом или известью[7].
Гидрофобные добавки (парафинистый мазут) уменьшают гигроскопичность. Также в процессе производства для улучшения физических свойств кальциевой селитры добавляют 4–7% нитрата аммониям[1][8].
Нитрат кальция производится путём обработки известняка с азотной кислотой, после нейтрализации аммиака:
Он также является побочным продуктом процесса Оддо при добыче фосфата кальция:
Так же как нитраты других щелочноземельных металлов и LiNO3, кальциевая селитра при нагревании разлагается на выпуске диоксида азота:
Хранение
Характерной особенностью вещества является высокая гигроскопичность: порошок активно впитывает влагу из воздуха, поэтому хранение требует использования герметичной тары в сухих помещениях. Вскрытую упаковку с порошкообразной селитрой необходимо сразу пересыпать в герметичную тару (стеклянную или пластиковую) и хранить в сухом, прохладном месте, защищённом от попадания влаги. Гранулированные формы менее подвержены слёживанию и сохраняют эффективность до 5 лет[3][7].
Готовый водный раствор не подлежит хранению и должен быть использован в течение 1—2 часов после приготовления[7].
В лабораторных условиях при хранении нитрата кальция необходимо соблюдать изоляцию от других реактивов[9].
Токсичность
Применение
Кристаллический нитрат кальция (его транспортировка на большие расстояния более экономически выгодна, чем раствор жидкой кальциевой селитры, на основе которой он произведён) находит применение в различных сферах: при приготовлении тампонажных цементов для цементирования нефтяных скважин и технологических растворов, предназначенных для ремонта нефтяных и газовых скважин; как добавка в бетон, замедляющая коррозию стальной арматуры, ускоряющая отвердение и повышающая прочность; для приготовления рассола в холодильной технике; в производстве реактивов и стеклопластиков[9][10].
Кальциевая селитра — один из компонентов для производства эмульсионных составов на основе нитратов аммония, используемой при проведении буровзрывных работ на открытых горных выработках. Ведение кальциевой селитры позволяет увеличить энергию взрыва в скважине, что особенно важно для крепких и особо крепких взрываемых пород[11][9].
Кальциевая селитра эффективна на всех типах почв, но особенно востребована на кислых и слабокислых грунтах. Являясь щелочным удобрением, в отличие от других азотсодержащих туков (например, сульфата аммония), кальциевая селитра не закисляет, а, наоборот, снижает кислотность почвенного субстрата, улучшая его структуру[12][4], поэтому её не рекомендуется использовать для растений, предпочитающих кислые почвы: голубики, брусники, клюквы, рододендронов, вересков, гортензий и большинство хвойным пород[7][4].
Кальций в удобрении содержится в водорастворимой форме, доступной для растений; укрепляет ткани растений и повышает их механическую прочность; препятствует развитию патогенной микрофлоры (корневых гнилей, вершинной гнили томатов, побурения краёв листьев); повышает сахаристость плодов, улучшает их лёжкость (сохранность) и товарный вид. В то же время избыток кальция блокирует усвоение калия, магния и железа[13][4].
Азот, присутствующий в нитратной форме, усваивается корневой системой без предварительной переработки почвенными бактериями[3][7] и способствует эффективному усвоению кальция.
Кальциевая селитра не содержит хлора, что делает её безопасной для культур, чувствительных к этому элементу (картофель, виноград, табак)[7][4].
Внесение рекомендуется преимущественно весной и первую половину лета, осенью — только под озимые культуры (например, чеснок)[3][12].
Способы внесения:
- под перекопку — вносится в сухом виде в почву перед посевом весной и в лунки при высадке рассады в грунт[3][13];
- корневая подкормка (полив) — наиболее эффективный метод[7][4];
- внекорневая подкормка (опрыскивание) — используется для быстрого устранения дефицита кальция (например, при вершинной гнили). Опрыскивание проводят утром и вечером, избегая попадания прямых солнечных лучей[7][13].
Запрещено смешивать нитрат кальция с удобрениями, содержащими фосфор и серу (суперфосфат, сульфат калия), а также с органикой в одном растворе, так как это приводит к химическим реакциям с образованием нерастворимых осадков и потере эффективности. Допустимо совместное применение с мочевиной и древесной золой[3][7].
Примечания
Литература
- Межерицкий С. Э., Соснин В. А., Ефимкин А. Г. Особенности применения и преимущества эмульсионных взрывчатых веществ на основе кальциевой селитры // Горная промышленность. — 2018. — № 6 (142).
- Минеев В.Г. Агрохимия. — М.: Издательство ВНИИА им. В. Д. Пряшникова, 2017. — С. 289. — 854 с.
- Ягодин Б.А., Жуков Ю.П., Кобзаренко В.Н. Агрохимия. — М.: Колос, 2002. — 584 с.