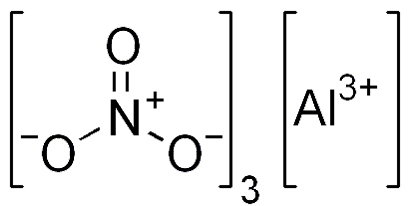
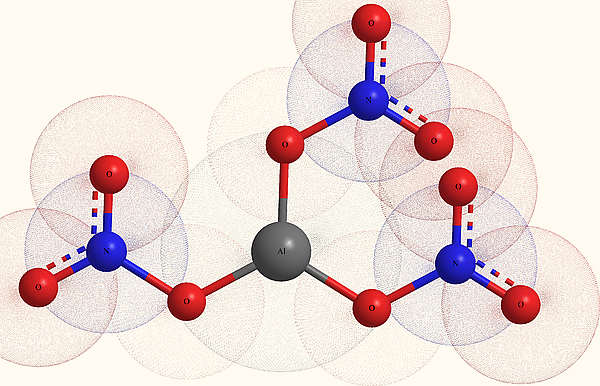
Нитрат алюминия
Нитра́т алюми́ния, азотнокислый алюминий — Al(NO3)3, неорганическое соединение, алюминиевая соль азотной кислоты.
Помимо собственно безводного нитрата, у алюминия существуют и основные нитраты: AlOH(NO3)2 и Al(OH)2NO3, а также ряд гидратированных солей Al(NO3)3•xH2O (х = 4, 6, 8, 9), среди которых наиболее стабилен нонагидрат: Al(NO3)3•9H2O.
Общие сведения
| Нитрат алюминия | |
|---|---|
| Общие | |
| Систематическое наименование |
Нитрат алюминия |
| Традиционные названия | Азотнокислый алюминий; нитрат алюминия(+3), тринитрат алюминия, алюминия (III) нитрат |
| Хим. формула | Al(NO3)3 |
| Рац. формула | Al(NO3)3 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 212,996 г/моль |
| Плотность | 1,89[1] |
| Термические свойства | |
| Температура | |
| • плавления | +66 °C (с разл.)[1]; нонагидрат: 73,5[1] |
| • разложения | +150-200 °C |
| Энтальпия | |
| • образования |
− 927 кДж/моль; нонагидрат: − 3757[2]; гексагидрат: − 2871[3] кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | при 25 °C: 63,7 г/100 мл |
| • в воде | нонагидрат при 20 °C: 73,9[4] |
| • в в метаноле | при 35 °C: 14,45[5] |
| • в в этаноле | при 35 °C: 8,63[5] |
| • в в этиленгликоле | при 35 °C: 18,32[5] |
| Структура | |
| Кристаллическая структура | моноклинная |
| Классификация | |
| Рег. номер CAS |
13473-90-0 7784-27-2 (нонагидрат) |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 16713320 |
| UNII | HUO854648Y |
| CompTox Dashboard EPA | DTXSID7040318 |
| Рег. номер EINECS | 236-751-8 |
| SMILES | |
| InChI | |
| RTECS |
BD1040000 BD1050000 (нонагидрат) |
| ChemSpider | 24267 |
| ECHA InfoCard | 100.033.396 |
| Безопасность | |
| ЛД50 | (крысы, перорально) 4280 мг/кг |
| Токсичность | Низкая |
| NFPA 704 | |
Физические свойства
Безводный нитрат алюминия представляет собой белое или бесцветное кристаллическое, чрезвычайно гигроскопичное вещество, дымящее на воздухе[2][6]. Хорошо растворим в холодной воде (63,7 % при 25 °C) и полярных органических растворителях[6]. Температура плавления 66 °C (с разложением), в вакууме возгоняется при 50 °C. Разлагается в горячей воде[2].
Нонагидрат Al(NO3)3•9H2O — белые кристаллы, расплывающееся на воздухе, с моноклинной структурой (a=1,086 нм, b=0,959 нм, c=1,383 нм, β=95,15°, z=4, пространственная группа P21/a). При нагревании чуть выше температуры плавления (73,6 °C) теряет сперва одну, а затем ещё две молекулы воды[2].
Плотность водного раствора нитрата алюминия при 18 °C[7]:
| 1 % | 2 % | 4 % | 6 % | 8 % | 10 % | 12 % | 14 % | |
|---|---|---|---|---|---|---|---|---|
| Плотность, г/л | 1006,5 | 1014,4 | 1030,5 | 1046,9 | 1063,8 | 1081,1 | 1098,9 | 1117,1 |
| 16 % | 18 % | 20 % | 24 % | 28 % | 30 % | 32 % | — | |
| 1135,7 | 1154,9 | 1174,5 | 1215,3 | 1258,2 | 1280,5 | 1303,6 | — |
Химические свойства
- Водные растворы нитрата алюминия имеют pH от 2,5 до 3,7[9].
- При нагревании гидролиз можно провести полностью[8]:
- Вступает в реакцию со щелочами:
- Реакция с концентрированным водным раствором аммиака может идти по двум направлениям[8].
- На холоде:
- При нагревании:
- При нагревании разлагается [8]:
- Нонагидрат при сильном нагревании (135 °C) сперва образует основную соль Al(OH)2NO3•1,5H2O, а при более высокой температуре (200 °C) разлагается до аморфного оксида алюминия[10].
- Нитрат алюминия является сильным окислителем — его безводная форма со взрывом реагирует со многими органическими растворителями (например: с диэтиловым эфиром и бензолом).
Получение
В лаборатории водный раствор нитрата алюминия получают растворением алюминия в разбавленной азотной кислоте:
Альтернативный метод заключается во взаимодействии гидроксида алюминия с азотной кислотой:
Наконец, искомую соль можно получить обменной реакцией сульфата алюминия с нитратом бария или свинца:
Из водного раствора посредством кристаллизации выделяют нонагидрат нитрата алюминия. Кристаллогидраты с меньшим количеством воды получают из водных растворов азотной кислоты[10].
Безводный нитрат алюминия можно получить реакцией кристаллогидрата с избытком оксидом азота (V) (реакция (1)) или безводного хлорида алюминия с нитратом хлора (реакция (2))[10][11]:
В промышленности безводный нитрат алюминия получают взаимодействием оксида или гидроксида алюминия с оксидом азота (V)[8]:
В случае использования бромида алюминия в качестве исходного сырья для синтеза, реакция идёт в две стадии:
Применение
Соединение используется в текстильной промышленности как протрава при крашении тканей, для дубления кожи, в производстве нитей накаливания, в качестве катализатора при очистке нефти, антикоррозионного агента; в производстве изоляционных бумаг, нагревательных элементах, антиперспирантов; в ядерной физике[12].
Примечания
Литература
- Downs A.J. Chemistry of aluminium, gallium, indium, and thallium. — First edition. — London: Chapman & Hall, 1993. — 526 p. — ISBN 0-7514-0103-X.
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001. — ISBN 5-06-003363-5.
- Лидин Р. А. Справочник по общей и неорганической химии. — М.: КолосС, 2008. — ISBN 978-5-9532-0465-1.
- Некрасов Б. В. Основы общей химии. — М.: Лань, 2004. — ISBN 5-8114-0501-4.
- Спицын В. И., Мартыненко Л. И. Неорганическая химия. — М.: МГУ, 1991, 1994.
- Турова Н. Я. Неорганическая химия в таблицах. Учебное пособие. — М.: ЧеРо, 2002. — ISBN 5-88711-168-2.

![{\displaystyle {\mathsf {Al(NO_{3})_{3}+4H_{2}O\leftrightarrows [Al(H_{2}O)_{4}]^{3+}+3NO_{3}^{-}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/20e7f089b6f887fdf2b9bc0243c59168ba412052)
![{\displaystyle {\mathsf {[Al(H_{2}O)_{4}]^{3+}+H_{2}O\leftrightarrows [Al(H_{2}O)_{3}(OH)]^{2+}+H_{3}O^{+}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/4b99b79a01eb414967bc983c36ed9faf716e34a2)


![{\displaystyle {\mathsf {Al(NO_{3})_{3}+4NaOH=Na[Al(OH)_{4}]+3NaNO_{3}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/4fdad34d0f1bcad0329d43d50a4fadcffcee3155)










![{\displaystyle {\mathsf {2AlBr_{3}+8N_{2}O_{5}=2[NO_{2}]^{-}[Al(NO_{3})_{4}]^{+}+3Br_{2}+6NO_{2}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/bef4333c8d98bf4e9855d208a2770329f0dde6fb)
![{\displaystyle {\mathsf {2[NO_{2}]^{-}[Al(NO_{3})_{4}]=2Al(NO_{3})_{3}+4NO_{2}+O_{2}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/ce2690b48a974e284fda6581b1515299bb3b260b)