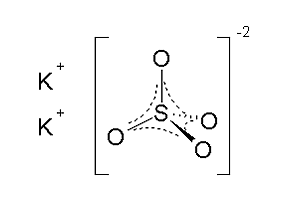
Сульфат калия
Сульфа́т ка́лия — неорганическое соединение. Химическая формула K2SO4. Используется в сельском хозяйстве в качестве удобрения, а также в производстве стекла и как пищевая добавка.
Общие сведения
| Сульфат калия | |
|---|---|
| Общие | |
| Систематическое наименование |
сульфат калия |
| Традиционные названия | сернокислый калий |
| Хим. формула | K2SO4 |
| Физические свойства | |
| Состояние | белое кристаллическое вещество |
| Молярная масса | 174.252 г/моль |
| Плотность | 2.66 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1069 °C |
| • кипения | 1689 °C |
| • вспышки | негорюч °C |
| Мол. теплоёмк. | 131,4 Дж/(моль·К) |
| Энтальпия | |
| • образования | −1437,7 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде |
(20 °C) 11.1 г/100мл (25 °C) 12 г/100мл (100 °C) 24 г/100 мл |
| • в остальных веществах | слабо растворим в глицерине, нерастворим в ацетоне, спирте, CS2 |
| Структура | |
| Кристаллическая структура | ромбическая |
| Классификация | |
| Рег. номер CAS | 7778-80-5 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 24507 |
| UNII | 1K573LC5TV |
| CompTox Dashboard EPA | DTXSID6029701 |
| Рег. номер EINECS | 231-915-5 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E515(i) и E515 |
| RTECS | TT5900000 |
| ChEBI | 32036 |
| ChemSpider | 22915 |
| ECHA InfoCard | 100.029.013 |
| Безопасность | |
| ЛД50 | 6600 мг/кг |
| NFPA 704 | |
История
Нахождение в природе
В природе находится на месторождениях калийных солей. Присутствует в водах солёных озёр.
Физические свойства
Бесцветные кристаллы, ромбическая сингония (a = 0,742 нм, b = 1,001 нм, c = 0,573 нм, Z = 4, пространственная группа Pnam). При температуре выше 584 °C переходит в гексагональную модификацию (a = 0,5947 нм, c = 0,8375 нм, Z = 2, пространственная группа P63/mmc).
Хорошо растворим в воде, не подвергается гидролизу. Нерастворим в концентрированных растворах щелочей или в чистом этаноле.
Вкус горько-солёный[1].
Получение
Минеральные формы чистого сульфата калия относительно редки. Минерал арканит (англ. Arcanite) состоит из чистого K2SO4, представляет собой белые или прозрачные кристаллы, встречается в Калифорнии (США).
Есть много минералов, содержащих соли калия:
- Каинит — MgSO4·KCl·H2O
- Глазерит — 2K2SO4·Na2SO4
- Шёнит — K2SO4·MgSO4·6H2O
- Леонит — K2SO4·MgSO4·4H2O
- Лангбейнит — K2SO4·2MgSO4
- Полигалит — K2SO4·MgSO4·2CaSO4·2H2O
- Сингенит — K2SO4·CaSO4·H2O
Промышленные методы получения основаны на обменных реакциях KCl с различными сульфатами и в результате сульфат калия, как правило, сильно загрязнён побочными продуктами:
Наиболее чистый продукт получают, обрабатывая твёрдый хлорид калия концентрированной серной кислотой:
Прокаливанием с углём минерала лангбейнита:
В лабораторной практике применяют следующие методы:
- из оксида калия:
- вытеснением из слабых или неустойчивых кислот:
- из щёлочи и разбавленной кислоты:
- окислением сульфида калия:
Сульфат калия получается при нагреве сульфита калия до температуры в 600 °C:
Окисление серы бихроматом калия:
Взаимодействием сульфата аммония и гидроксид калия:
Химические свойства
Как соль двухосновной кислоты образует кислые соли:
Как все сульфаты взаимодействует с растворимыми соединениями бария:
Восстанавливается до сульфида:
С оксидом серы образует пиросульфат:
Применение
Основной потребитель сульфата калия — сельское хозяйство. Сульфат калия является ценным бесхлорным удобрением. Эффективность сульфата калия лучше проявляется на бедных калием дерново-подзолистых почвах гранулометрического состава и торфяных почвах. На чернозёмных почвах он применяется обычно под культуры, которые усваивают много калия и натрия (сахарная свёкла, подсолнечники, плодовые, для корнеплодов, овощей). На каштановых и серозёмных почвах используют в зависимости от вида культуры, технологии выращивания и содержания калия в почве. Сульфат калия намного эффективнее влияет на величину урожая и его качество, если его применять в комплексе с азотными и фосфорными удобрениями. На кислых почвах действие сульфата калия повышается на фоне использования извести.
Калий повышает содержание сахаров и витаминов в выращиваемой продукции, а подкормки в конце августа-сентябре способствуют лучшему зимованию плодово-ягодным и декоративным деревьям и кустарникам. Используется на различных почвах, под все культуры, а также для комнатного и балконного цветоводства. Сульфат калия пригоден для всех способов внесения: основного (при перекопке почвы весной или осенью) и для подкормки в течение вегетационного периода.[2]
Применяется в первую очередь под культуры, чувствительные к хлору, положительно влияя на урожай растений семейства крестоцветных (капуста, брюква, турнепс и др.), бобовых, картофеля, ягодных кустарников, земляники и винограда. Для эффективного воздействия на урожай рекомендуется внесение сульфата калия осенью под перекопку. Весной необходимо внести удобрение за месяц до посадки растений. Глубина заделки на лёгких почвах — 5—10 см, на тяжёлых — не менее 15 см. Летом лучше использовать корневые и внекорневые подкормки растворами сульфата калия при появлении у растений признаков калийного голодания[3].
Также сульфат калия используется в производстве стекла, различных квасцов и других соединений калия, как флюс в металлургии.
В Европейском союзе допущен к использованию как пищевая добавка E515. Она относится к эмульгаторам, которые используют для получения однородной массы из несмешиваемых компонентов (например, воды с маслом). Также Е515 применяется при промышленном производстве продуктов питания для регулирования кислотности[4].
Признаки недостатка и избытка калия
Недостаток калия в растениях приводит к снижению интенсивности фотосинтеза и синтеза белка, что влияет на качество урожая и увеличивает его восприимчивость к различным грибам в период роста растений и хранения. При долгом калийном голодании листья приобретают бронзовый отлив. Также дефицит калия можно заподозрить по следующим признакам[5]:
- листья растений имеют неправильную форму;
- на листьях появляются бурые пятна;
- короткие междоузлия;
- на нижних листьях картофеля проявляется «краевой ожог».
При избытке калия в растениях появляются признаки, характерные для недостатка железа, цинка, марганца и магния[5]:
- побурение верхних листьев;
- тонкие и мелкие новые листья;
- быстрое увядание при достатке влаги в почве из-за плохого всасывания;
- толстая кожура плодов.
Сведения о безопасности
Следующие действия сульфатом калия на части тела могут вызвать:
- Глаза: попадание пыли может вызвать механическое раздражение,
- Кожа: попадание на кожу может вызвать раздражение,
- Проглатывание: употребление в пищу больших количеств может вызвать раздражение желудочно-кишечного тракта,
- Вдыхание: при вдыхании может вызвать раздражение дыхательных путей,
- При хроническом употреблении сульфата калия: отравления могут возникать в редких случаях длительного воздействия.