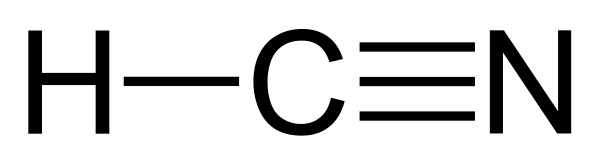Синильная кислота
Сини́льная (циа́нистоводорóдная) кислота́ (гидроцианид, циа́нистый водорóд, циа̀новодоро́д[3]) — химическое соединение с формулой HCN. Бесцветная, очень летучая, легкоподвижная ядовитая жидкость, имеющая неприятный запах[4] (некоторые люди не способны ощущать её запах, порог чувствительности широко варьируется среди населения[5][6]).
Синильная кислота содержится в некоторых растениях, коксовом газе, табачном дыме, выделяется при термическом разложении нейлона, полиуретанов.
Общие сведения
| Синильная кислота | |
|---|---|
| Общие | |
| Систематическое наименование |
Цианид водорода, цианистый водород |
| Традиционные названия | Гидроцианид; циановодород, синильная кислота |
| Хим. формула | HCN |
| Рац. формула | HCN |
| Физические свойства | |
| Состояние | бесцветный ядовитый газ или бесцветная легколетучая жидкость с резким неприятным запахом |
| Молярная масса | 27,0253 г/моль |
| Плотность | 0,687 г/см³ |
| Динамическая вязкость | 0,201 Па·с |
| Энергия ионизации | 13,6[2] |
| Термические свойства | |
| Температура | |
| • плавления | −13,4 °C |
| • кипения | 26,7 °C |
| • вспышки | −17,8 °C |
| Пределы взрываемости | 5,6[2] |
| Мол. теплоёмк. | (средняя для газа и жидкости) 1,97 Дж/(моль·К) |
| Давление пара | 630[2] |
| Химические свойства | |
| Константа диссоциации кислоты | 9,21 |
| Растворимость | |
| • в воде | в любых пропорциях |
| Оптические свойства | |
| Показатель преломления | 1,2675 |
| Структура | |
| Дипольный момент | 2,98 Д |
| Классификация | |
| Рег. номер CAS | 74-90-8 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 768 |
| UNII | 2WTB3V159F |
| CompTox Dashboard EPA | DTXSID9024148 |
| Рег. номер EINECS | 200-821-6 |
| SMILES | |
| InChI | |
| RTECS | MW6825000 |
| ChEBI | 18407 |
| Номер ООН | 1051 |
| ChemSpider | 748 и 19951400 |
| ECHA InfoCard | 100.000.747 |
| Безопасность | |
| Предельная концентрация | 0,3 мг/м3 (максимально-разовая) [1] |
| ЛД50 | 3,7 мг/кг (мыши, перорально) |
| Токсичность | Чрезвычайно токсична, СДЯВ |
| Пиктограммы ECB |
|
| NFPA 704 | |
Физические свойства
Смешивается во всех соотношениях с водой, этанолом, диэтиловым эфиром. Смешивается также со многими другими спиртами и эфирами, ароматическими углеводородами и тетрахлоруглеродом[4].
Молекула HCN имеет линейное строение[7][8] с межатомными расстояниями H—C 0,1064 нм и C≡N 0,1156 нм и сильно полярна (электрический дипольный момент μ = 0,992⋅10−29 Кл·м)[4].
Безводный цианистый водород является сильно ионизирующим растворителем, растворённые в нём электролиты хорошо диссоциируют на ионы. Его относительная диэлектрическая проницаемость при 25 °C равна[4] 106,8 (выше, чем у воды). Это обусловлено линейной ассоциацией полярных молекул HCN за счёт образования водородных связей.
Температура плавления −13,29 °C, кипения +25,65 °C. Плотность 0,71618 г/см3 при 0 °C, 0,68708 г/см3 при 0 °C[4].
Критическое давление 4,95 МПа, критическая температура +183,5 °C, критическая плотность 0,195 г/см3[4].
Коэффициент преломления nD = 1,26136 (20 °C)[4].
Энтальпия образования 132 кДж/моль, энтальпия плавления 8,41 кДж/моль, энтальпия испарения 25,2 кДж/моль. Энтальпия сгорания −663 кДж/моль. Энтропия 201,71 Дж/(моль·К) (при 298 К)[4].
Динамическая вязкость 0,183 мПа·с, кинематическая вязкость 17,78 мН/м[4].
Удельное электрическое сопротивление жидкой синильной кислоты 105 Ом·м[4].
Твёрдая синильная кислота при нормальном давлении существует в двух кристаллических модификациях. При температуре ниже −102,78 °C образует кристаллы ромбической сингонии, пространственная группа I2mm, параметры ячейки a = 0,413 нм, b = 0,485 нм, c = 0,434 нм, Z = 2. Выше этой температуры переходит в кристаллы тетрагональной сингонии, пространственная группа I4mm, параметры ячейки a = 0,463 нм, c = 0,434 нм, Z = 2[4].
Химические свойства
Очень слабая одноосновная кислота: её константа диссоциации Ka = 1,32⋅10−9, pKa = 8,88 (при 18 °C)[4]. Образует с металлами соли — цианиды. Взаимодействует с оксидами и гидроксидами щелочных и щёлочноземельных металлов.
Пары синильной кислоты горят на воздухе фиолетовым пламенем с образованием Н2О, СО и N2. Температура самовоспламенения в воздухе 538 °C. Температура вспышки −18 °C. Взрывоопасная концентрация паров HCN в воздухе 4,9—39,7 %[4].
В смеси кислорода с фтором горит с выделением большого количества тепла:
- кДж.
Синильная кислота широко применяется в органическом синтезе. Она реагирует с карбонильными соединениями, образуя циангидрины:
С хлором, бромом и иодом прямо образует циангалогениды:
С галогеналканами — нитрилы (реакция Кольбе):
С алкенами и алкинами реагирует, присоединяясь к кратным связям:
Легко полимеризуется в присутствии основания (часто со взрывом). Образует аддукты, например, HCN-CuCl.
При разложении водой даёт формиат аммония, либо формамид
Название
Цианогруппа в сочетании с железом даёт насыщенный ярко-синий цвет. Известное соединение берлинская лазурь, смесь гексацианоферратов с формулой Fe7(CN)18. Берлинскую лазурь получил в 1704 году немецкий мастер Иоганн Якоб Дисбах, готовивший краски для художников. И уже в 1782 шведский химик Карл Шееле получил из берлинской лазури синильную (синюю) кислоту.
Физиологические свойства
Синильная кислота очень токсична и смертельно ядовита. Является веществом, вызывающим кислородное голодание тканевого типа[9]. При этом наблюдается высокое содержание кислорода как в артериальной, так и в венозной крови и уменьшение таким образом артерио-венозной разницы, резкое понижение потребления кислорода тканями с уменьшением образования в них углекислоты. Синильная кислота и её соли, растворённые в крови, достигают тканей, где вступают во взаимодействие с трёхвалентной формой железа цитохромоксидазы. Соединившись с цианидом, цитохромоксидаза теряет способность переносить электроны на молекулярный кислород. Вследствие выхода из строя конечного звена окисления блокируется вся дыхательная цепь и развивается тканевая гипоксия. С артериальной кровью кислород доставляется к тканям в достаточном количестве, но не усваивается ими и переходит в неизменённом виде в венозное русло. Одновременно нарушаются процессы образования макроэргов, необходимых для нормальной деятельности различных органов и систем. Активизируется гликолиз, то есть обмен с аэробного перестраивается на анаэробный. Также подавляется активность и других ферментов — каталазы, пероксидазы, лактатдегидрогеназы.
В результате тканевой гипоксии, развивающейся под влиянием синильной кислоты, в первую очередь нарушаются функции центральной нервной системы.
В результате острого отравления наблюдается резкое увеличение частоты и глубины дыхания. Развивающуюся одышку следует рассматривать как компенсаторную реакцию организма на гипоксию. Стимулирующее действие синильной кислоты на дыхание обусловлено возбуждением хеморецепторов каротидного синуса и непосредственным действием яда на клетки дыхательного центра. Первоначальное возбуждение дыхания по мере развития интоксикации сменяется его угнетением вплоть до полной остановки. Причинами этих нарушений являются тканевая гипоксия и истощение энергетических ресурсов в клетках каротидного синуса и в центрах продолговатого мозга.
Проникая в кровь, синильная кислота снижает способность клеток воспринимать кислород из притекающей крови. А так как нервные клетки больше остальных нуждаются в кислороде, они первыми страдают от её действия. В начальном периоде интоксикации наблюдается замедление сердечного ритма. Повышение артериального давления и увеличение минутного объёма сердца происходят за счёт возбуждения синильной кислотой хеморецепторов каротидного синуса и клеток сосудодвигательного центра с одной стороны, и выброса катехоламинов из надпочечников и вследствие этого спазма сосудов — с другой. В дальнейшем артериальное давление падает, пульс учащается, развивается острая сердечно-сосудистая недостаточность и наступает остановка сердца.
Содержание в крови эритроцитов увеличивается, что объясняется рефлекторным сокращением селезёнки в ответ на развивающуюся гипоксию. Цвет венозной крови становится ярко-алым за счёт избыточного содержания кислорода, не поглощённого тканями. Артерио-венозная разница по кислороду резко уменьшается. При угнетении тканевого дыхания изменяется как газовый, так и биохимический состав крови. Содержание CO2 в крови снижается вследствие меньшего образования и усиленного его выделения при гипервентиляции. Это приводит в начале развития интоксикации к газовому алкалозу, который меняется метаболическим ацидозом, что является следствием активации процессов гликолиза. В крови накапливаются недоокисленные продукты обмена. Увеличивается содержание молочной кислоты, нарастает содержание ацетоновых тел, отмечается гипергликемия. Нарушение окислительно-восстановительных процессов в тканях приводит к гипотермии. Таким образом, синильная кислота и её соли вызывают явления тканевой гипоксии и связанные с ней нарушения дыхания, кровообращения, обмена веществ, функции центральной нервной системы, выраженность которых зависит от тяжести интоксикации.
Как и многие другие кислоты, синильная кислота коррозийно-активна по отношению к металлам[10].
Биологическая роль
Показано, что нейроны способны вырабатывать эндогенную синильную кислоту (цианистый водород, HCN) после их активации эндогенными или экзогенными опиоидами и что образование нейронами эндогенной синильной кислоты повышает активность NMDA-рецепторов и, таким образом, может играть важную роль в передаче сигнала между нейронами (нейротрансмиссии). Более того, образование эндогенного цианида оказалось необходимым для проявления в полном объёме анальгетического действия эндогенных и экзогенных опиоидов, а вещества, снижающие образование свободной HCN, оказались способны уменьшать (но не полностью устранять) анальгетическое действие эндогенных и экзогенных опиоидов. Выдвинуто предположение, что эндогенная синильная кислота может являться нейромодулятором[11].
Известно также, что стимуляция мускариновых холинорецепторов клеток феохромоцитомы в культуре повышает образование ими эндогенной синильной кислоты, однако стимуляция мускариновых холинорецепторов ЦНС в живом организме крысы приводит, наоборот, к снижению образования эндогенной синильной кислоты[12].
Также показано, что синильная кислота выделяется лейкоцитами в процессе фагоцитоза и способна убивать патогенные микроорганизмы[11].
Возможно, что вазодилатация, вызываемая нитропруссидом натрия, связана не только с образованием окиси азота (механизм, общий для действия всех сосудорасширяющих препаратов группы нитратов, таких как нитроглицерин, нитросорбид), но и с образованием цианида. Возможно, что эндогенный цианид и образующийся при его обезвреживании в организме тиоцианат играют роль в регуляции функций сердечно-сосудистой системы, в обеспечении вазодилатации и являются одними из эндогенных антигипертензивных веществ[13].
Получение
В настоящий момент существуют три наиболее распространённых метода получения синильной кислоты в промышленных масштабах:
- Метод Андрусова — прямой синтез из аммиака и метана в присутствии воздуха и платинового катализатора при высокой температуре:
- Метод BMA (Blausäure aus Methan und Ammoniak), запатентованный фирмой Degussa: прямой синтез из аммиака и метана без воздуха в присутствии платинового катализатора при высокой температуре:
- Побочный продукт при производстве акрилонитрила путём окислительного аммонолиза пропилена.
- Реакцией цианида калия с водой и диоксидом углерода:
- Термическим разложением железосинеродистой и железистосинеродистой кислот:
(в присутствии влаги)
- В Шавиниганском процессе углеводороды (например, пропан) реагируют с аммиаком. В лаборатории небольшие количества синильной кислоты образуются путём добавления кислот к цианидным солям щелочных металлов:
Эта реакция иногда является основой случайных отравлений, потому что кислота превращает нелетучую цианидную соль в газообразный циановодород.
- Реакцией монооксида углерода с аммиаком:
- Фотолиз метана в бескислородной атмосфере:
Может быть получена в лабораторных условиях взаимодействием красной кровяной соли и разведённой кислоты:[14]
Применение
Является сырьём для получения акрилонитрила, метилметакрилата, адипонитрила и других соединений. Большое число её производных используются при извлечении благородных металлов из руд, при гальванопластическом золочении и серебрении, в производстве ароматических веществ, химических волокон, пластмасс, каучука, органического стекла, стимуляторов роста растений, гербицидов.
Впервые в роли боевого отравляющего вещества синильная кислота была использована французской армией 1 июля 1916 года на реке Сомме[15]. Однако из-за отсутствия кумулятивных свойств и малой стойкости на местности её последующее использование в этом качестве прекратилось.
Синильная кислота являлась основной составляющей препарата «Циклон Б», который был наиболее популярным в Европе во время Второй мировой войны инсектицидом, а также использовался нацистами для убийства людей в концентрационных лагерях. В некоторых штатах США синильная кислота использовалась в газовых камерах в качестве отравляющего вещества при исполнении приговоров смертной казни; в последний раз это было сделано в Аризоне в 1999 году[16]. Смерть, как правило, наступает в течение 5—15 минут.
Соли
Соли синильной кислоты называются цианидами. Все цианиды, как и сама кислота, очень ядовиты. Цианиды подвержены сильному гидролизу. При хранении водных растворов цианидов при доступе диоксида углерода они разлагаются:
Ион CN− (изоэлектронный молекуле СО) входит как лиганд в большое число комплексных соединений d-элементов. Комплексные цианиды в растворах очень стабильны.
Цианиды тяжёлых металлов термически неустойчивы; в воде, кроме цианида ртути (Hg(CN)2), нерастворимы. При окислении цианиды образуют соли — цианаты:
Многие металлы при действии избытка цианида калия или цианида натрия дают комплексные соединения, что используется, например, для извлечения золота и серебра из руд:
Токсичность и биологические свойства
Синильная кислота — сильнейший яд общетоксического действия, блокирует клеточную цитохромоксидазу, в результате чего возникает выраженная тканевая гипоксия. Половинные летальные дозы (LD50) и концентрации для синильной кислоты[17]:
- Мыши:
- перорально (ORL-MUS LD50) — 3,7 мг/кг;
- при вдыхании (IHL-MUS LC50) — 323 м.д.;
- внутривенно (IVN-MUS LD50) — 1 мг/кг.
- Кролики, внутривенно (IVN-RBT LD50) < 1 мг/кг;
- Человек, минимальная опубликованная смертельная доза перорально (ORL-MAN LDLo) < 1 мг/кг.
При вдыхании синильной кислоты в небольших концентрациях наблюдается царапанье в горле, горький вкус во рту, головная боль, тошнота, рвота, боли за грудиной. При нарастании интоксикации уменьшается частота пульса, усиливается одышка, развиваются судороги, наступает потеря сознания. При этом цианоз отсутствует (содержание кислорода в крови достаточное, нарушена его утилизация в тканях).
При вдыхании синильной кислоты в высоких концентрациях или при попадании её внутрь появляются клонико-тонические судороги и почти мгновенная потеря сознания вследствие паралича дыхательного центра. Смерть может наступить в течение нескольких минут.
В организме человека метаболитом синильной кислоты является роданид (тиоцианат) SCN−, образующийся при её взаимодействии с серой под действием фермента роданазы.
Антидоты синильной кислоты
Для лечения отравлений синильной кислотой известно несколько антидотов, которые могут быть разделены на две группы. Лечебное действие одной группы антидотов основано на их взаимодействии с синильной кислотой с образованием нетоксичных продуктов. К таким препаратам относятся, например, коллоидная сера и различные политионаты, переводящие синильную кислоту в малотоксичную роданистоводородную кислоту, а также альдегиды и кетоны (глюкоза, диоксиацетон и др.), которые химически связывают синильную кислоту с образованием циангидринов. К другой группе антидотов относятся препараты, вызывающие образование в крови метгемоглобина: синильная кислота связывается метгемоглобином и не доходит до цитохромоксидазы. В качестве метгемоглобинообразователей применяют метиленовую синь, а также соли и эфиры азотистой кислоты.
Сравнительная оценка антидотных средств: метиленовая синь предохраняет от двух смертельных доз, тиосульфат натрия и тетратиосульфат натрия — от трёх доз, нитрит натрия и этилнитрит — от четырёх доз, метиленовая синь совместно с тетратиосульфатом — от шести доз, амилнитрит совместно с тиосульфатом— от десяти доз, азотистокислый натрий совместно с тиосульфатом — от двадцати смертельных доз синильной кислоты.
Охрана труда
См. также
Примечания
Литература
- Бобков С. С., Смирнов С. К. Синильная кислота. — М.: Химия, 1970. — 176 с.
- Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия. — М.: Химия, 1994.
- Некрасов Б. В. Основы общей химии. — 3-е изд., испр. и доп.. — М.: Химия, 1973. — Т. 1. — 656 с.
- Basset H., Corbet A. S. CLXXI.—The hydrolysis of potassium ferricyanide and potassium cobalticyanide by sulphuric acid (англ.) // Journal of the Chemical Society : journal. — Chemical Society, 1924. — Vol. 125. — P. 1358—1366. — doi:10.1039/CT9242501358.














![{\displaystyle {\mathsf {2H_{3}[Fe(CN)_{6}]\ {\xrightarrow {T}}\ Fe[Fe(CN)_{6}]+6HCN\uparrow }}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/15427a7a507047f249f08524300d8afa4d21aac4)
![{\displaystyle {\mathsf {3H_{4}[Fe(CN)_{6}]\ {\xrightarrow {100^{o}C}}\ Fe_{2}[Fe(CN)_{6}]+12HCN\uparrow }}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/faf701461732d6fd40cfda5556270327bd0f24a0)




![{\displaystyle {\mathsf {K_{3}[Fe(CN)_{6}]+6HCl{\xrightarrow {}}\ 3KCl+FeCl_{3}+6HCN{\uparrow }}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/1f4a0e0476d4fbffaffa94c262693676d88e826d)



![{\displaystyle {\mathsf {8NaCN+4Au+O_{2}+2H_{2}O\rightarrow 4Na[Au(CN)_{2}]+4NaOH}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/e77a143642e28270421f66fdb285f009576c9f93)