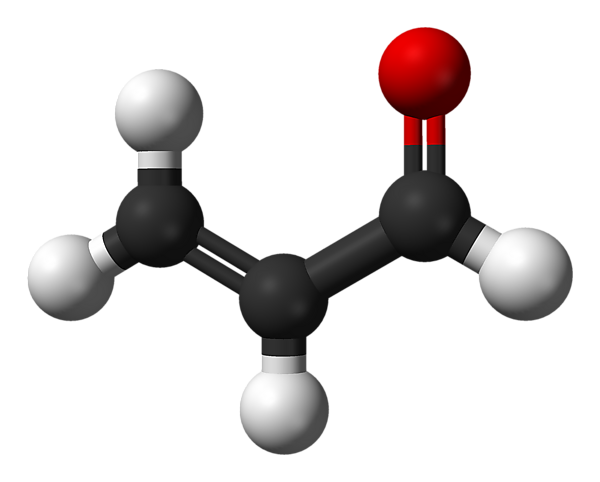
Акролеин
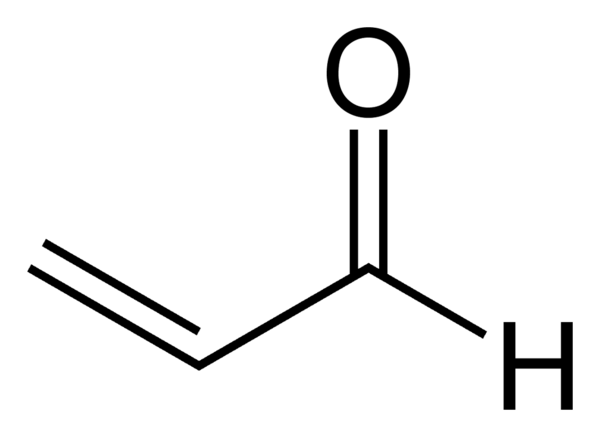
Акролеи́н (лат. acris — острый, едкий + oleum — масло) (пропеналь) — H2C=CH-CHO, альдегид акриловой кислоты, простейший ненасыщенный альдегид.
При обычных условиях легколетучая жидкость с резким запахом, пары вызывают слезоточение, сильный лакриматор.
Общие сведения
| Акролеин | |
|---|---|
| Общие | |
| Систематическое наименование |
Проп-2-ен-1-аль |
| Традиционные названия | Акролеин, пропеналь, акрилальдегид |
| Хим. формула | C3H4O |
| Физические свойства | |
| Молярная масса | 56,0633 ± 0,003 г/моль |
| Плотность | 0,843 г/см³ |
| Энергия ионизации | 974,7911 кДж/моль |
| Термические свойства | |
| Температура | |
| • плавления | −87 °C |
| • кипения | 52,7 °C |
| • вспышки | -26 °C |
| • самовоспламенения | 234 °C |
| Пределы взрываемости | 2,8–31 % % |
| Критическая точка | 232,85 °С |
| Давление пара | 29 кПа (20 °С) |
| Химические свойства | |
| Растворимость | |
| • в воде | 209 г/100 мл |
| Структура | |
| Дипольный момент |
2,552 ± 0,003 (цис-положение), 3,117 ± 0,004 (транс-положение) |
| Классификация | |
| Рег. номер CAS | 107-02-8 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 7847 |
| UNII | 7864XYD3JJ |
| CompTox Dashboard EPA | DTXSID5020023 |
| Рег. номер EINECS | 203-453-4 |
| SMILES | |
| InChI | |
| RTECS | AS1050000 |
| ChEBI | 15368 |
| Номер ООН | 1092 |
| ChemSpider | 7559 |
| ECHA InfoCard | 100.003.141 |
| Безопасность | |
| Предельная концентрация | 0,03 мг/м3 |
| ЛД50 |
46 мг/кг (белые крысы, перорально); 7 мг/кг (кролики, перорально); 28 мг/кг (мыши, перорально) |
| Токсичность | высокотоксичен, особенно опасны его пары, сильный ирритант, лакриматор |
| Пиктограммы ECB |
|
| NFPA 704 | |
Реакционная способность
Акролеин как непредельный альдегид, проявляет реакционную способность, свойственную как олефинам, так и альдегидам. Так, акролеин образует ацетали.
Альдегидная группа легко, даже при стоянии на воздухе окисляется до карбоксильной:
и восстанавливается до гидроксильной:
- .
Карбонильная группа акролеина находится в сопряжении с двойной связью, что обуславливает его высокую реакционную способность по отношению к нуклеофилам, при этом присоединение идёт по β-атому углерода:
- ,
- .
Присоединение азотистой кислоты () к акролеину используется как препаративный метод синтеза 3-нитропропаналя[1].
Галогены присоединяются к акролеину по двойной связи с образованием дигалогенпроизводного, которое далее отщепляет галогеноводород с образованием α-галогенакролеина:
- ;
- .
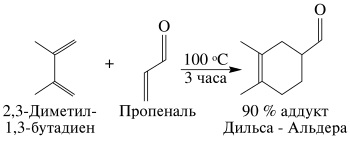
Благодаря наличию электроноакцепторной альдегидной группы, сопряжённой с двойной связью, акролеин является диенофилом и реагирует с диенами с образованием продуктов циклоприсоединения (реакция Дильса-Альдера):
Синтез
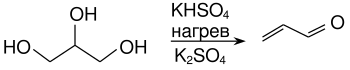
В лаборатории акролеин получается дегидратацией глицерина в присутствии гидросульфата калия[2]:
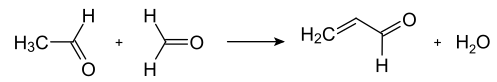
В промышленности акролеин получают каталитическим окислением пропилена над оксидными висмут-молибденовыми катализаторами или оксидом меди. Ранее в промышленности был распространён процесс парофазной кротоновой конденсации ацетальдегида с формальдегидом (устаревший метод):
Токсичность, особенности обращения
Вследствие своей чрезвычайно высокой реакционной способности акролеин является токсичным, сильно раздражающим слизистые оболочки глаз и дыхательных путей соединением, сильный лакриматор. Максимально разовая предельно-допустимая концентрация в воздухе 0,03 мг/м³. Среднесуточная предельно-допустимая концентрация в воздухе 0,01 мг/м³ (Список ПДК ГН 2.1.6 1338-03). Вызывает мутагенез у микроорганизмов и дрожжей, проявляет мутагенные свойства на культуры клеток млекопитающих[3].
Класс опасности — 2 (вещества высокоопасные) согласно ГОСТ 12.1.007-76.
Акролеин является одним из продуктов термического разложения глицерина и жиров-триглицеридов, чем объясняются раздражающие слизистые оболочки свойства дыма горелого жира.
Аспекты охраны труда
Применение
Применяют для синтеза акрилонитрила, глицерина, пиридина, β-пиколина, аминокислот (метионина), этилвиниловых эфиров, глутарового альдегида, полиакролеина. Также используется в производстве лекарственных препаратов.
Во время Первой мировой войны использовался в качестве химического оружия.
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.

![{\displaystyle {\ce {H2C=CH-CHO ->[{\ce {O}}] H2C=CH-COOH}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/1393d106e3f121b51e140a16f73e9ecd54fe9cc8)
![{\displaystyle {\ce {H2C=C-CHO ->[][{\ce {H}}] H2C=CH-CH2OH}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/c213d3c4847b6131dc3f6b19a0e13ac909d8d100)