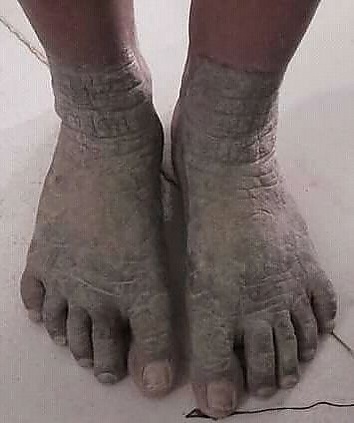
Бородавчатая эпидермодисплазия
Борода́вчатая эпидермодисплази́я (лат. epidermodysplasia verruciformis, верруцифо́рмная эпидермодисплази́я Левандо́вского — Лю́тца) — редкое аутосомно-рецессивное заболевание, относящееся к группе предраковых дерматозов. Патология характеризуется множественными симметрично расположенными папулёзными и папуло-бляшечными высыпаниями, преимущественно локализующимися на коже лица и конечностей, с возможным вовлечением туловища. Заболевание связано с повышенной восприимчивостью кожи к определённым типам вируса папилломы человека, что определяет формирование характерных клинических проявлений. В большинстве случаев верруциформная эпидермодисплазия манифестирует в детском или юношеском возрасте. Наряду с наследственными описаны приобретённые формы заболевания, развивающиеся на фоне первичных или вторичных иммунодефицитных состояний. Особенностью бородавчатой эпидермодисплазии является высокая склонность поражённых участков кожи к злокачественной трансформации, особенно при длительном воздействии ультрафиолетового излучения.
Общие сведения
История
Бородавчатая эпидермодисплазия была впервые описана в 1922 году немецким дерматовенерологом Феликсом Левандовским и швейцарским дерматологом Вильгельмом Лутцем как редкое наследственное заболевание кожи. Впоследствии было установлено, что данная патология относится к группе генодерматозов и характеризуется стойким, длительно сохраняющимся течением. Позднее заболевание было ассоциировано с генерализованной кожной инфекцией, вызванной вирусами папилломы человека. Высокая частота развития злокачественных опухолей кожи при бородавчатой эпидермодисплазии послужила основанием для её рассмотрения в качестве модели вирус-индуцированного канцерогенеза у человека[2][3].
Известными клиническими случаями бородавчатой эпидермодисплазии являются пациенты Деде Косвара и Абул Бажандар, получившие широкую известность в медицинской литературе и средствах массовой информации в связи с крайне выраженными проявлениями заболевания[4].
Этиология
Бородавчатая эпидермодисплазия относится к редким генодерматозам и в большинстве случаев имеет наследственную природу[5]. Заболевание чаще наследуется по аутосомно-рецессивному типу и связано с мутациями в генах TMC6 и TMC8, локализованных на хромосоме 17q25[6]. У части пациентов выявляются мутации в гене CIB1, формирующем функциональный комплекс с белками EVER, а также дефекты в ряде других генов, участвующих в регуляции Т-клеточного иммунитета и функции натуральных киллеров, включая RHOH, CORO1A, CARMIL2, RASGRP1, MST1, DCLRE1C, DOCK8, TPP2 и LCK[7][8].
У части пациентов мутации EVER1 и EVER2 не обнаруживаются, что отражает генетическую гетерогенность заболевания. Описаны приобретённые формы бородавчатой эпидермодисплазии, возникающие на фоне иммунодефицитных состояний, включая ВИЧ-инфекцию, лимфопролиферативные заболевания, состояние после трансплантации органов и длительную иммуносупрессивную терапию[8][9].
Заболевание связано с инфицированием определёнными типами вируса папилломы человека, преимущественно бета-папилломавирусами. Описано более 30 ассоциированных серотипов ВПЧ, среди которых наибольшее значение имеют типы 5 и 8, а также 14, 17, 20, 25 и 47. Эти типы ВПЧ могут выявляться у иммунокомпетентных лиц без клинических проявлений, тогда как при бородавчатой эпидермодисплазии они реализуют патогенный потенциал на фоне генетически обусловленного нарушения противовирусной защиты кожи[7][8].
Патогенез
Патогенез бородавчатой эпидермодисплазии обусловлен сочетанием генетически детерминированного дефекта кожного клеточного иммунитета и персистирующей инфекции бета-папилломавирусами. Ключевой особенностью заболевания является нарушение клеточно-опосредованного иммунного ответа кожи к определённым типам вируса папилломы человека, что приводит к персистенции вируса в эпидермисе и невозможности его эффективной элиминации[3][9].
Мутации в генах EVER1, EVER2 и CIB1 нарушают функцию белкового комплекса, выполняющего роль рестрикционного фактора для бета-папилломавирусов в кератиноцитах. Дефект данного комплекса сопровождается изменением внутриклеточного гомеостаза цинка, что способствует активации вирусной репликации и экспрессии вирусных генов. В результате формируется стойкая продуктивная инфекция в эпидермисе. Генерализованный иммунодефицит для бородавчатой эпидермодисплазии не характерен. Нарушение носит избирательный характер и затрагивает преимущественно клеточный иммунный ответ кожи. Отмечается ослабление реакций контактной гиперчувствительности и снижение контроля над кератиноцитами, инфицированными вирусом папилломы человека. При выраженной иммуносупрессии заболевание может приобретать более распространённое течение[3][9].
Механизмы злокачественной трансформации при бородавчатой эпидермодисплазии носят многофакторный характер. В опухолевых очагах выявляются ДНК и транскрипты бета-папилломавирусов, при этом интеграция вирусного генома в ДНК хозяина, как правило, отсутствует. Экспрессия вирусных онкобелков E6 и E7 сохраняется, однако их трансформирующая активность ограничена. Существенное значение в канцерогенезе играет хроническое воздействие ультрафиолетового излучения, приводящее к мутациям гена TP53 и нарушению механизмов репарации ДНК. Дополнительную роль в опухолевом росте играют ультрафиолет-индуцированная локальная иммуносупрессия и повышенная экспрессия иммунорегуляторных цитокинов, включая фактор некроза опухоли-альфа, трансформирующий фактор роста-бета и интерлейкин-10, что способствует выживанию повреждённых кератиноцитов и постепенному развитию немеланомных опухолей кожи[3][9].
Эпидемиология
Бородавчатая эпидермодисплазия относится к крайне редким дерматологическим заболеваниям. Точная распространённость в популяции не установлена. Описано около 500 пациентов с данным заболеванием. Географической или расовой предрасположенности не выявлено. Заболевание встречается у лиц обоего пола с одинаковой частотой. Гендерных различий в распространённости не отмечается, несмотря на редкие описания Х-сцепленных и аутосомно-доминантных вариантов наследования. В большинстве случаев бородавчатая эпидермодисплазия наследуется по аутосомно-рецессивному типу. Примерно у 10 % пациентов родители состоят в кровном родстве. Наряду с наследственными формами описаны спорадические случаи заболевания. Клинические проявления, как правило, возникают в детском возрасте. Дебют в младенчестве отмечается примерно у 7,5 % пациентов, в возрасте 5-11 лет — у большинства больных, в пубертатный период — примерно у четверти пациентов. Заболевание характеризуется длительным существованием кожных очагов с тенденцией к появлению новых элементов с течением времени. Злокачественные опухоли кожи формируются обычно спустя десятилетия от начала заболевания, преимущественно в четвёртом и пятом десятилетиях жизни. Частота злокачественной трансформации кожных очагов составляет около 30-60 %[9][10].
Диагностика
Бородавчатая эпидермодисплазия характеризуется полиморфными кожными высыпаниями с хроническим течением, манифестирующими в детском возрасте. Первичные элементы представлены множественными, густо расположенными мелкими округлыми или полигональными папулами, формирующими характерный сетевидный рисунок. На отдельных участках кожи папулы склонны к слиянию с образованием бляшек. Поверхность бляшек может быть плоской или шероховатой за счёт чешуек, которые варьируют от тонких белесоватых до более плотных, желтоватых, слоистых. Окраска элементов колеблется от бледно-розовой до синюшно-красной, а также от телесной до коричневатой. На коже лица, помимо папул, могут определяться пигментные пятна, напоминающие веснушки. На туловище преобладают плоские, чётко очерченные бляшки и очаги, иногда сходные с проявлениями отрубевидного лишая. Кожа туловища может быть неравномерно пигментированной и шелушащейся, напоминая изменения при вульгарном ихтиозе[2]. В отдельных случаях возможна алопеция[9][11].
На конечностях, особенно в дистальных отделах, элементы часто имеют вид обыкновенных бородавок со склонностью к группировке, линейному или полосовидному расположению и слиянию с формированием крупных бородавчатых очагов. Папулы и бляшки преимущественно локализуются на открытых участках кожи, подвергающихся воздействию ультрафиолетового излучения, включая тыльные поверхности кистей, лицо, шею и разгибательные поверхности конечностей. Пигментированные бляшки чаще располагаются на туловище, шее и проксимальных отделах конечностей[2][9].
Высыпания обычно множественные и распространённые, однако в редких случаях возможно ограничение поражения одной анатомической областью или конечностью. Поражение слизистых оболочек встречается редко. Течение заболевания длительное. Со временем одни элементы могут подвергаться регрессу, тогда как на других участках кожи формируются новые очаги[2][9].
По мере прогрессирования заболевания отдельные очаги способны трансформироваться в бородавчатые бляшки и узлы, а в дальнейшем — в злокачественные новообразования кожи, преимущественно плоскоклеточный рак[9].
Основным методом лабораторной диагностики бородавчатой эпидермодисплазии является гистологическое исследование биопсийного материала изменённого участка кожи. Гистологическая картина во многом сходна с изменениями, характерными для плоской бородавки. В эпидермисе выявляются гиперкератоз по типу «плетёной корзинки», акантоз с утолщением эпидермальных выростов, а также вакуольная дистрофия клеток шиповатого слоя. Вакуоли отличаются крупными размерами[2]. Отмечаются пикноз и фрагментация ядер поражённых клеток, зернистый слой часто атрофичен. Характерным морфологическим признаком является наличие кератиноцитов с перинуклеарными вакуолями и бледно-эозинофильной либо синевато-серой цитоплазмой, так называемых «синих клеток», отражающих цитопатический эффект папилломавирусной инфекции. В ряде случаев выявляются признаки койлоцитоза[8]. В дерме может определяться незначительный периваскулярный инфильтрат, представленный лимфоцитами и гистиоцитами[9][11].
При предраковых изменениях сохраняется нормальная дифференцировка кератиноцитов, тогда как при злокачественной трансформации отмечается нарушение поверхностной дифференцировки эпидермиса. Возможны гистологические изменения, сходные с актиническим кератозом и болезнью Боуэна, включая атипию кератиноцитов[8][9].
Выявление ДНК вируса папилломы человека возможно с использованием методов гибридизации in situ на формалин-фиксированных биоптатах кожи. Типирование ВПЧ может также выполняться методом полимеразной цепной реакции на свежем или замороженном материале. Молекулярно-генетическое обследование может включать анализ мутаций в генах EVER1 и EVER2, проводимый на ДНК лейкоцитов с использованием методов скрининга экзонных участков[9].
Дифференциальная диагностика
Дифференциальную диагностику бородавчатой эпидермодисплазии следует проводить со следующими заболеваниями[2][8]:
- плоские бородавки;
- контагиозный моллюск;
- верруциформный акрокератоз Гопфа;
- болезнь Дарье[11];
- отрубевидный лишай;
- себорейный кератоз;
- актинический кератоз;
- плоскоклеточный рак кожи;
- актинический кератоз;
- базальноклеточный рак кожи;
- WHIM-синдром[12];
- WILD-синдром[13];
- синдром Нетертона.
Осложнения
Основным и наиболее клинически значимым осложнением бородавчатой эпидермодисплазии является развитие немеланомных злокачественных опухолей кожи, прежде всего плоскоклеточного рака и болезни Боуэна. Опухолевые изменения обычно возникают на участках кожи, длительно подвергающихся инсоляции, и формируются через 20-30 лет от начала заболевания. В ряде случаев отмечается постепенный переход от доброкачественных верруциформных очагов к внутриэпидермальным карциномам с последующим развитием инвазивных форм. Описаны также отдельные случаи сочетания заболевания с другими злокачественными новообразованиями, включая лимфопролиферативные процессы. Хроническое течение и множественность кожных поражений могут сопровождаться снижением качества жизни, социальной дезадаптацией и психоэмоциональными нарушениями. При отсутствии лечения опухолевые очаги способны к местно-деструктивному росту[8][9].
Лечение
Лечение бородавчатой эпидермодисплазии представляет значительные трудности, поскольку этиотропная и радикальная терапия заболевания отсутствует. Лечебные мероприятия носят преимущественно профилактический и паллиативный характер и направлены на контроль кожных проявлений, снижение активности папилломавирусной инфекции и предупреждение злокачественной трансформации[7][9].
Ключевое значение в ведении пациентов имеет строгая фотозащита, которая должна быть начата сразу после установления диагноза и соблюдаться пожизненно. В терапии используются различные местные и системные методы. Используются топические ретиноиды, имиквимод, аналоги витамина D, цидофовир и кератолитические средства[14]. В ряде случаев назначаются системные ретиноиды, в частности ацитретин, который рассматривается как препарат поддерживающей терапии и применяется длительно[8]. Интерфероны могут использоваться как системно, так и в виде внутриочагового введения, особенно при множественных активных поражениях[7][9].
В комплексном лечении применяются также деструктивные методы, включая криотерапию, электрохирургические вмешательства, фотодинамическую терапию и лазерные методики. Фотодинамическая терапия с аминолевулиновой кислотой применяется при отдельных внутриэпидермальных неопластических изменениях, развивающихся на фоне бородавчатой эпидермодисплазии. Хирургическое лечение показано при развитии злокачественных опухолей кожи и включает иссечение очагов с последующим гистологическим исследованием. В отдельных случаях применяется микрографическая хирургия по Мосу, в том числе при множественных или рецидивирующих очагах[7][9].
Лучевая терапия при бородавчатой эпидермодисплазии противопоказана, поскольку может способствовать формированию более агрессивных опухолевых форм. При наличии иммунодефицитных состояний терапия подбирается индивидуально с учётом общего статуса пациента. В отдельных случаях обсуждается возможность вакцинации против вируса папилломы человека как потенциального дополнительного подхода[8][9].
Прогноз
Прогноз при бородавчатой эпидермодисплазии характеризуется хроническим, пожизненным течением заболевания и высоким риском злокачественной трансформации кожных очагов. Высыпания сохраняются на протяжении всей жизни и склонны к постепенному прогрессированию, начинающемуся в детском возрасте и сохраняющемуся в последующие возрастные периоды[2]. Существенным неблагоприятным прогностическим фактором является длительное воздействие ультрафиолетового излучения. Злокачественные новообразования кожи формируются преимущественно после 30 лет, чаще в четвёртом и пятом десятилетиях жизни. Инвазивные опухоли кожи развиваются у значительной части пациентов. В большинстве случаев опухоли остаются локальными, метастазирование наблюдается крайне редко. Летальные исходы возможны в исключительных ситуациях и обычно связаны с инвазивным плоскоклеточным раком, в том числе с поражением конъюнктивы. При регулярном медицинском наблюдении и своевременном выявлении злокачественных изменений прогноз в отношении продолжительности жизни в целом остаётся благоприятным[8][9].
Диспансерное наблюдение
Наблюдение у врача-дерматовенеролога. Регулярные осмотры дерматолога направлены на раннее выявление диспластических и злокачественных изменений кожи. Частота наблюдения определяется индивидуально, с учётом возраста пациента, распространённости поражений и степени инсоляции. При выявлении подозрительных очагов показано их углублённое обследование и своевременное хирургическое лечение. Ведение пациентов целесообразно осуществлять с участием специалистов смежных профилей, включая онколога и генетика. Длительное динамическое наблюдение является ключевым условием снижения риска тяжёлых осложнений и улучшения отдалённых исходов заболевания[8].
Профилактика
Специфических мер профилактики бородавчатой эпидермодисплазии не разработано. Основное значение имеет вторичная профилактика, направленная на снижение риска злокачественной трансформации кожных очагов. Ключевым профилактическим мероприятием является строгая фотозащита, предусматривающая ограничение инсоляции, регулярное применение солнцезащитных средств широкого спектра и использование защитной одежды. Пациентам рекомендуется избегать длительного пребывания на солнце, особенно в периоды максимальной ультрафиолетовой активности. Существенную роль играет информирование пациентов о признаках возможной малигнизации кожных элементов и необходимости своевременного обращения за медицинской помощью при появлении изменений со стороны очагов поражения[8].
Примечание
Литература
- Ламоткин И. А. Онкодерматология: атлас : учебное пособие. — М. : Лаборатория знаний, 2017. — С. 110—111. — 878 с. — ISBN 978-5-00101-432-4.
- Антоньев А. А., Бабаянц Р. С., Беренбейн Б. А. Дифференциальная диагностика кожных болезней. Руководство для врачей. — Медицина (Москва), 1989. — С. 145. — 666 с. — ISBN 5-225-00051-7.