Рецепторные тирозинкиназы
Рецепторные тирозинкиназы, рецепторы с тирозинкиназной активностью (англ. Receptor Tyrosin Kinases, сокр. RTK) — метаботропные клеточные рецепторы, представляют собой трансмембранные белки, которые состоят из каталитического внутриклеточного домена, участвующего в фосфорилировании субстратов (тирозинкиназа), трансмембранного и внешнего домена (связывающего) с высоким сродством к лигандам: гормонам (инсулин), цитокинам и полипептидным факторам роста[1][2]. Из 90 уникальных генов тирозинкиназы, идентифицированных в геноме человека, 58 кодируют рецепторные тирозинкиназы[3].
Было показано, что рецепторные тирозинкиназы не только являются ключевыми регуляторами нормальных клеточных процессов, но также играют критическую роль в развитии и прогрессировании многих типов злокачественных опухолей[4]. Мутации в рецепторных тирозинкиназах приводят к активации ряда сигнальных каскадов, которые оказывают многочисленные воздействия на экспрессию белка. Рецепторные тирозинкиназы являются частью более широкого семейства протеинтирозинкиназ, охватывающих рецепторные тирозинкиназные белки, которые содержат трансмембранный домен, а также нерецепторные тирозинкиназы, которые не обладают трансмембранными доменами[5].
Общие сведения
| receptor protein-tyrosine kinase | |
|---|---|
| Идентификаторы | |
| Шифр КФ | 2.7.10.1 |
| Базы ферментов | |
| IntEnz | IntEnz view |
| BRENDA | BRENDA entry |
| ExPASy | NiceZyme view |
| MetaCyc | metabolic pathway |
| KEGG | KEGG entry |
| PRIAM | profile |
| PDB structures | RCSB PDB PDBe PDBj PDBsum |
| Gene Ontology | AmiGO • EGO |
| Поиск | |
| PMC | статьи |
| PubMed | статьи |
| NCBI | NCBI proteins |
История
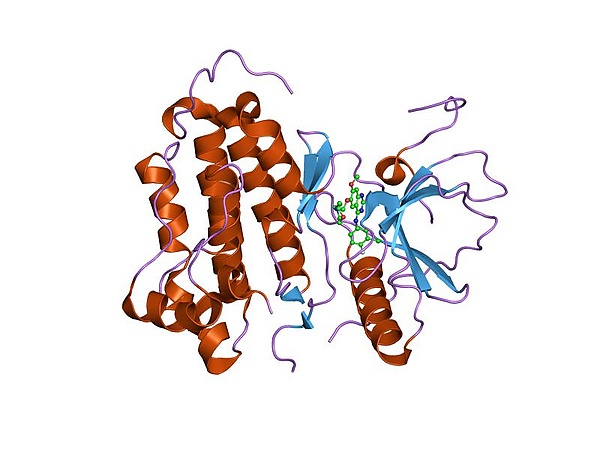
Структура
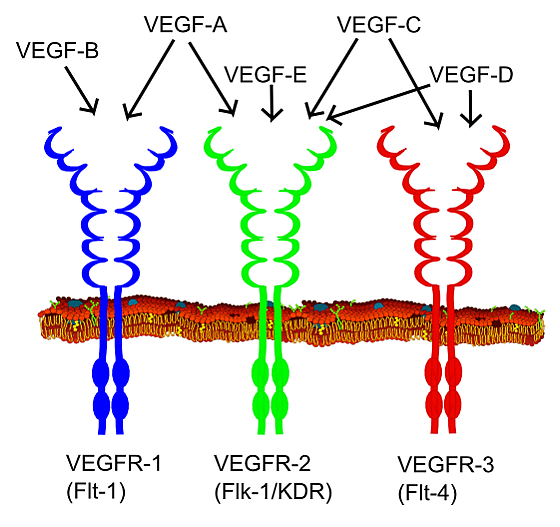
Большинство RTK являются рецепторами, состоящих из одной субъединицы, но некоторые существуют в виде мультимерных комплексов, например, инсулиновый рецептор, который образует дисульфид-связанные димеры в присутствии молекул гормона (инсулина); кроме того, связывание лиганда с внеклеточным доменом вызывает образование димеров рецептора[7]. Каждый мономер имеет один гидрофобный трансмембранно-охватывающий домен, состоящий из 25-38 аминокислотных остатков, внеклеточную N-концевую область и внутриклеточную С-концевую область[8]. Внеклеточная N-концевая область обладает множеством консервативных элементов, включая иммуноглобулин (Ig)-подобный или эпидермальный фактор роста (EGF)-подобные домены, повторы фибронектина типа III или богатые цистеином области, которые характерны для каждого подсемейства RTK; эти домены содержат в основном лиганд-связывающий сайт, который ответственен за связывание внеклеточных лигандов, например, факторов роста или гормонов. Внутриклеточная С-концевая область обладает наивысшим уровнем консервативности и содержит каталитические домены, ответственные за киназную активность этих рецепторов, которая катализирует аутофосфорилирование рецепторов и фосфорилирование остатков тирозина, являющихся субстратами RTK.
Передача сигнала
С помощью различных средств внеклеточное связывание лиганда обычно вызывает или стабилизирует димеризацию рецептора. Это позволяет трансфосфорилировать тирозин в цитоплазматической части каждого мономера рецептора его партнёрским рецептором, распространяя сигнал через плазматическую мембрану. Фосфорилирование специфических остатков тирозина в активированном рецепторе создает сайты связывания для белков, src-гомологичные домены 2 (SH2) и связывающий домен фосфотирозина (PTB). Специфические белки, содержащие данные домены, включают Src и фосфолипазу Cγ. Фосфорилирование и активация этих двух белков при связывании рецептора приводят к инициации путей передачи сигнала. Другие белки, которые взаимодействуют с активированным рецептором, как адаптерные белки не имеют собственной ферментативной активности. Эти адаптерные белки связывают процесс активации молекул RTK с нисходящими сигнальными путями трансдукции, такими как сигнальный каскад MAP-киназы. Примером жизненно важного пути трансдукции сигнала является рецепторная тирозинкиназа, c-met, которая необходима для выживания и пролиферации мигрирующих миобластов во время миогенеза (роста и развития мышечной ткани). Недостаток c-met нарушает вторичный миогенез и как в LBX1-препятствует формированию мускулатуры конечностей. Такое локальное действие FGF (факторов роста фибробластов) с их рецепторами RTK классифицируется как паракринная передача сигналов. Поскольку молекулы RTK фосфорилируют множество остатков тирозина, они могут активировать множество путей передачи сигнала.
Регуляция
Путь рецептора тирозинкиназы (RTK) тщательно регулируется различными положительными и отрицательными петлями обратной связи[9]. поскольку RTKs координируют широкий спектр клеточных функций, таких как пролиферация и дифференцировка клеток, они должны регулироваться для предотвращения серьёзных нарушений в функционировании клеток, таких как рак и фиброз[10].