Сублимация (физика)
Сублима́ция (от лат. sublimo «возносить»), возго́нка — переход вещества из твёрдого состояния сразу в парообразное, минуя стадию плавления (перехода в жидкое состояние) и кипения. Поскольку при возгонке изменяется удельный объём вещества и поглощается энергия (теплота сублимации), возгонка является фазовым переходом первого рода[1][2].
Общие сведения
Общие положения
Обратным процессом является десублимация — конденсация вещества из парообразного состояния непосредственно в твёрдое, минуя жидкое[2]. Как и сублимация, десублимация представляет собой фазовый переход первого рода. Десублимация может осуществляться на холодной поверхности или при смешении паров вещества с более холодным газом, при расширении некоторых сжатых газов (образование твёрдого диоксида углерода при работе углекислотных огнетушителей). Примерами десублимации служат такие атмосферные явления, как десублимация атмосферной влаги с образованием инея на поверхности земли и изморози на ветвях деревьев и проводах, морозных узоров на оконных стёклах[1]. Образование и изменение ядер комет также имеет сублимационно-десублимационную природу[2].
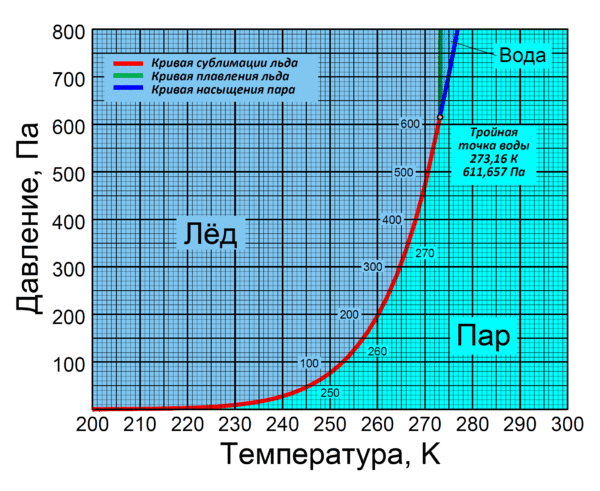
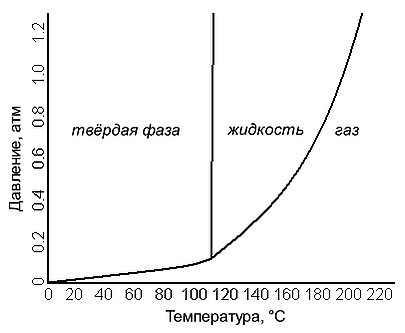
Оба процесса — и сублимация, и десублимация — протекают при температуpaх и давлениях ниже соответствующихтройной точке рассматриваемого вещества[1].
Примеры возгонки
Возгонка характерна, например, для элементарного иода I2, который при нормальных условиях не имеет жидкой фазы: чёрные с голубым отливом кристаллы сразу превращаются (сублимируются) в газообразный молекулярный иод (медицинский «иод» представляет собой спиртовой раствор).
Сухой лёд (твёрдый углекислый газ) является наиболее типичным примером вещества, подвергающегося при нормальном атмосферном давлении возгонке. Температура сублимации углекислого газа составляет 194,65 K (или — 78,5 °C), в жидком состоянии диоксид углерода может существовать только при повышенном давлении. Так, при 20 °C диоксид углерода переходит в жидкость при давлении более 6 МПа (61.183 кгс/см²).
Хорошо поддаётся возгонке лёд, что определило широкое применение данного процесса как одного из способов сушки.
Применение процесса
В промышленности сублимацию и десублимацию используют для выделения веществ из газовых потоков (в частности, фталевого ангидрида, гексафторида урана), очистки веществ, сублимационной сушки (например, пищевых продуктов), тепловой защиты летательных аппаратов при сверхзвуковых скоростях полёта, нанесения защитных и функциональных покрытий при изготовлении приборов и др[1].
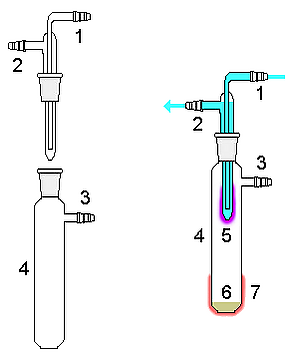
На эффекте возгонки основан один из способов очистки твёрдых веществ. При определённой температуре одно из веществ в смеси возгоняется с более высокой скоростью, чем другое. Пары очищаемого вещества конденсируют на охлаждаемой поверхности. Прибор, в котором используется этот способ очистки, называется сублиматор.
Сублимационная сушка (лиофилизация; лиофильная сушка) (от англ. freeze drying, или lyophilization) — процесс удаления растворителя из замороженных растворов, гелей, суспензий и биологических объектов, основанный на сублимации затвердевшего растворителя (льда) без образования макроколичеств жидкой фазы.
При промышленной возгонке сначала производят заморозку исходного тела, а затем помещают его в вакуумную или заполненную инертными газами камеру. Физически процесс возгонки продолжается до тех пор, пока концентрация водяных паров в камере не достигнет нормального для данной температуры уровня, в связи с чем избыточные водяные пары постоянно откачивают. Возгонка применяется в химической промышленности, в частности, на производствах взрывоопасных или взрывчатых веществ, получаемых осаждением из водных растворов.
Возгонка также используется в пищевой промышленности: так, сублимированный кофе получают из замороженного кофейного экстракта через обезвоживание вакуумом. Фрукты после сублимирования весят в несколько раз меньше, а в воде восстанавливаются. Сублимированные продукты значительно превосходят сушёные по пищевой ценности, так как возгонке поддаётся только вода, а при термическом испарении теряются многие полезные вещества.
Примечания
Литература
- Горелик Г. С. Сублимация // Химическая энциклопедия. — Большая Российская энциклопедия, 1995. — Т. 4. — С. 449—451.
- Раков Э. Г. Сублимация и десублимация // Большая российская энциклопедия. — Большая Российская энциклопедия, 2016. — Т. 31. — С. 361.
- Румер Ю. Б. Термодинамика, статистическая физика и кинетика : учебное пособие для студентов. — Новосибирск : Издательство Новосибирского университета, 2000.
- Ландау Л. Д. Курс общей физики : механика и молекулярная физика. — Москва : Добросвет : Издательство КДУ, 2011.