Абдоминальный компартмент-синдром
Абдомина́льный компа́ртмент-синдро́м (АКС; англ. abdominal compartment syndrome) представляет собой жизнеугрожающее состояние, определяемое как стойкое повышение внутрибрюшного давления свыше 20 мм рт. ст., которое сопровождается впервые возникшей дисфункцией органов. Данное состояние развивается в различных клинических ситуациях, включая тупую или проникающую травму, массивную инфузионную терапию, внутрибрюшное кровотечение, кишечную непроходимость или тяжёлый сепсис. Повышенное внутрибрюшное давление нарушает венозный возврат, снижает сердечный выброс, ограничивает экскурсию диафрагмы и вентиляцию лёгких, ухудшает почечную перфузию и может быстро прогрессировать до полиорганной недостаточности при несвоевременной диагностике. Без лечения АКС может привести к летальному исходу, а отсрочка медицинской помощи связана с высокими показателями смертности[1].
История
Первое научное описание мышечного компартмент-синдрома было сделано в 1850 году, а уже год спустя та же концепция была применена к абдоминальному синдрому. Немецкий хирург Рихард фон Фолькманн связал ишемию мышц с повышенным давлением в замкнутом пространстве, ограничивающим кровоснабжение[2].
С развитием методов измерения давления в XIX веке начались исследования внутрибрюшного давления. Учёные, такие как Поль Бер, измеряли давление в прямой кишке и коррелировали его с дыханием. Затем последовали измерения давления в других органах: мочевом пузыре, матке, а также путём прямой пункции брюшной полости. В 1911 году Хейвен Эмерсон опубликовал знаковое исследование, связав резкое повышение внутрибрюшного давления с сердечно-сосудистым коллапсом и показав, что эвакуация асцитической жидкости ведёт к восстановлению работы сердца. Было установлено, что повышенное внутрибрюшное давление нарушает как венозный, так и артериальный кровоток, снижает сердечный выброс и почечную фильтрацию, что приводит к уменьшению диуреза. Этот синдром стали выявлять после сложных операций, при травмах, внутрибрюшном кровотечении и напряжённом асците[2].
Лечение повышенного внутрибрюшного давления имеет давнюю историю. Ещё в Средневековье Ги де Шолиак проводил лапароцентез при асците. Позже для этого использовали троакары. Концепция хирургической декомпрессии для снятия давления была введена Бернхардом Барденхойером в 1906 году для синдрома сдавления в конечностях. В 1940-х годах Хенидж Огилви применил этот принцип к брюшной полости, используя лапаростомию (оставление живота открытым) при обширных ранениях. Эмпирический опыт этапного закрытия больших омфалоцеле у детей также подтвердил важность снижения внутрибрюшного давления[2].
В 1951 году анестезиолог М. Г. Баггот связал послеоперационную дыхательную недостаточность с форсированным закрытием живота и предложил оставлять брюшную полость открытой. Широкое внедрение лапароскопии в 1970-х годах вновь привлекло внимание к мониторингу внутрибрюшного давления, так как создаваемый пневмоперитонеум мог вызывать опасные сердечно-сосудистые и дыхательные осложнения. Это привело к возрождению интереса к измерению внутрибрюшного давления в хирургии. В 1984 году Крон и его коллеги начали использовать измерение давления для определения показаний к релапаротомии и декомпрессии у послеоперационных пациентов. Внутрипузырное измерение давления стало стандартом в отделениях интенсивной терапии для руководства хирургическим лечением. К концу XX века было доказано, что оперативная декомпрессия живота может обратить вспять жизнеугрожающие последствия АКС[2].
Классификация
АКС классифицируется следующим образом[3]:
- первичный АКС: связан с травмой или патологией в брюшной полости (например, травма, панкреатит, кровотечение);
- вторичный АКС: связан с патологическими состояниями не брюшной локализации (например, сепсис, массивная инфузионная терапия, ожоги);
- хронический рецидивирующий АКС: состояние, при котором АКС развивается повторно после предыдущего хирургического или медикаментозного лечения первичного или вторичного АКС.
Этиология
Причины первичного АКС включают следующие состояния: проникающая травма, внутрибрюшное кровотечение, панкреатит, внешние сдавливающие силы, такие как завал после автомобильной аварии или взрыва крупных сооружений, перелом костей таза, разрыв аневризмы брюшной аорты, перфорация полого органа[4].
Вторичный АКС может возникать у пациентов без внутрибрюшной травмы, когда объём накопленной жидкости достаточен для развития внутрибрюшной гипертензии. Причины включают: интенсивная инфузионная терапия (риск значительно возрастает при инфузии более 3 литров), обширные ожоги третьей степени, проникающую или тупую травму, особенности послеоперационного ведения (тампонада и первичное закрытие фасции), сепсис. Факторами напрямую связанными с развития вторичного АКС также являются массивная гемотрансфузия, наличие диабета в анамнезе[4].
Причины хронического абдоминального компартмент-синдрома включают: перитонеальный диализ, морбидное ожирение, цирроз печени, синдром Мейгса, внутрибрюшное объёмное образование[4].
Патогенез
Патогенез АКС связан с повышением внутрибрюшного давления, что приводит к прогрессирующей полиорганной недостаточности через ряд взаимосвязанных механизмов[1][5]:
- сердечно-сосудистая система: высокое внутрибрюшное давление вызывает сдавление нижней полой вены, что резко снижает венозный возврат крови к сердцу. Это приводит к снижению сердечного выброса и, как следствие, доставки кислорода к тканям. Одновременно диафрагма смещается вверх, повышая внутригрудное давление, которое напрямую сдавливает сердце, уменьшая его растяжимость и усугубляя нарушения гемодинамики;
- дыхательная система: повышенное внутригрудное давление ограничивает подвижность лёгких, снижая дыхательный объём и функциональную остаточную ёмкость. Возрастает сопротивление в лёгочных сосудах и давление в дыхательных путях, что затрудняет вентиляцию. Развивается компрессионный ателектаз, нарушается газообмен: снижается поступление кислорода (гипоксемия) и накапливается углекислый газ (гиперкапния), приводя к распираторному ацидозу.
- мочевыделительная система: почечный кровоток значительно ухудшается из-за внешнего сдавления сосудов и паренхимы. Это снижает клубочковую фильтрацию и приводит к острому повреждению почек со снижением диуреза;
- пищеварительная система: кровоток в брыжеечных сосудах резко падает, что вызывает гипоксию слизистой оболочки кишечника. Нарушается функция кишечного барьера, что позволяет бактериям и их токсинам проникать через стенку кишки (феномен бактериальной транслокации) в системный кровоток, провоцируя или усугубляя сепсис. Снижение печёночного кровотока нарушает метаболизм и детоксикацию, способствуя развитию метаболического ацидоза.
- нервная система: повышенное внутрибрюшного давления нарушает венозный отток от головного мозга, что приводит к повышению внутричерепного давления и снижению церебрального кровотока. Накопление углекислого газа дополнительно усиливает приток крови к мозгу, ещё больше увеличивая внутричерепное давление.
Эпидемиология
АКС представляет значительную и распространённую проблему для пациентов отделений реанимации и интенсивной терапии. Эпидемиологические данные показывают, что внутрибрюшная гипертензия — патологическое состояние, предшествующее АКС, — является частым явлением в этой популяции. Согласно результатам проспективных исследований, при поступлении в отделение реанимации внутрибрюшная гипертензия диагностируется у каждого третьего пациента в критическом состоянии. В течение последующих двух недель лечения этот показатель возрастает, достигая почти половины всех пациентов. Непосредственно АКС, как конечная стадия этого патологического процесса, наблюдается примерно у 3 % пациентов в отделении реанимации, причём некоторые исследования отмечают его более частное развитие у пациентов терапевтических отделений[6].
Диагностика
Клиническая картина АКС отличается вариабельностью и во многом определяется первичным заболеванием. Наиболее характерным симптомом служит боль в животе, которая часто предшествует развёрнутой картине синдрома и бывает непосредственно связана с причинным фактором — например, тупой травмой живота или приступом панкреатита. Общая слабость или эпизоды потери сознания могут указывать на развивающуюся гиповолемию[4].
Следует подчеркнуть, что классические симптомы — боль и вздутие живота — наблюдаются не у всех пациентов. Во многих случаях первыми тревожными сигналами становятся внезапно возникшая одышка и прогрессирующее уменьшение объёма выделяемой мочи. Особую сложность для диагностики представляет то, что значительная часть пациентов с развивающимся АКС находится в крайне тяжёлом, часто бессознательном состоянии, подключена к аппарату искусственной вентиляции лёгких и не может субъективно описывать свои ощущения[4].
Ключевым признаком при физикальном обследовании, позволяющим заподозрить развитие АКС, является увеличение обхвата живота. При остром состоянии живот становится напряжённым и болезненным. Хотя у пациентов с морбидным ожирением это бывает сложно оценить, у большинства больных наблюдается характерная, непропорциональная телу вздутость живота, которая становится особенно заметной, если пациент сидит или стоит. Помимо напряжённого живота, синдром проявляется вторичными эффектами, связанными с нарушением функции органов. К ним относятся признаки дыхательной недостаточности, такие как влажные хрипы при аускультации и учащённое дыхание, а также цианоз[4].
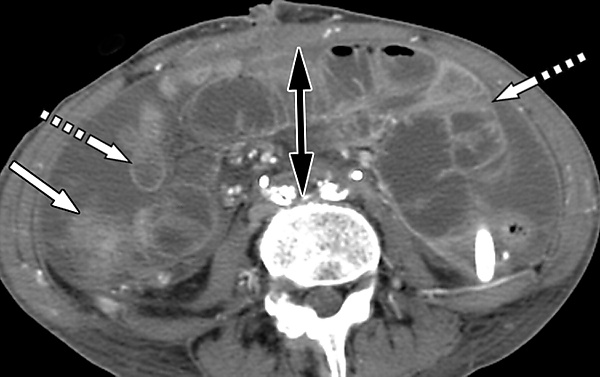
Компьютерная томография играет важную роль в выявлении косвенных признаков, позволяющих заподозрить АКС. Хотя некоторые находки, такие как уплощённая нижняя полая вена и повышенное контрастное усиление стенки кишечника («шоковая кишка»), традиционно связывают с гиповолемическим шоком, они также регулярно наблюдаются и у пациентов с АКС, даже при отсутствии выраженной гипотонии. Ключевые КТ-признаки, ассоциированные с АКС, включают[4][5]:
- сосудистые компрессионные изменения: уплощение нижней полой вены и почечных вен из-за внешнего сдавления повышенным внутрибрюшным давлением;
- патология паренхиматозных органов: наличие мозаичной перфузии печени, которая особенно характерна для пациентов с сопутствующей травмой печени. Также может наблюдаться повышение резистивного индекса печёночной артерии с резким снижением или даже реверсным диастолическим кровотоком;
- изменения со стороны желудочно-кишечного тракта: повышение контрастного усиления не только стенки тонкой кишки, но и стенки желудка. Кроме того, может наблюдаться вздутие петель тонкой кишки и выраженное растяжение желудка (гастростаз);
- изменение анатомии: высокое стояние куполов диафрагмы, являющееся прямым следствием повышенного давления в брюшной полости и смещения органов вверх.
Для достоверной диагностики АКС необходимо измерение внутрибрюшного давления. Прямое измерение, осуществляемое путём установки катетера в брюшную полость, хотя и считается высокоточным, является инвазивным и сопряжено с риском осложнений. На практике широкое применение нашли косвенные методы, которые позволяют оценить внутрибрюшное давление путём измерения давления в полых органах: мочевом пузыре (внутрипузырное давление), желудке (внутрижелудочное), прямой кишке (ректальное) или матке (внутриматочное). Золотым стандартом непрямого измерения признана методика определения давления в мочевом пузыре. При повышении внутрибрюшного давления более 20 мм рт. ст. диагностируется АКС[6].
В рамках диагностики АКС могут быть проведены следующие лабораторные исследования: клинический анализ крови, клинический анализ мочи, коагулограмма, биохимический анализ крови, определение кардиомпецифических маркеров и анализ газового состава крови. Данные исследования необходимы для комплексной оценки состояния пациента[4].
Дифференциальная диагностика
Дифференциальная диагностика АКС включает широкий спектр заболеваний, которые могут имитировать его клиническую картину. К ним относятся мезентериальная ишемия, разрыв аневризмы брюшной аорты, токсический мегаколон, острый аппендицит и острый дивертикулит. Также в список входят тупая травма живота, острый холецистит, застойная сердечная недостаточность с отёком лёгких, расслоение аорты, дивертикулярная болезнь, инородные тела желудочно-кишечного тракта, бактериемия и сепсис у детей, а также обструкция мочевыводящих путей[1][4].
Осложнения
Абдоминальный компартмент-синдром характеризуется развитием тяжёлых, часто полиорганных осложнений, обусловленных критическим повышением давления в брюшной полости[1][4]:
- со стороны мочевыделительной системы возникает острая почечная недостаточность. Её развитие связано с прямым сдавлением почечной паренхимы и резким снижением почечного кровотока;
- дыхательная система реагирует развитием острой дыхательной недостаточности;
- со стороны желудочно-кишечного тракта развивается ишемия кишечника, вызванная компрессией сосудов брыжейки и нарушением спланхнического кровотока;
- повышенное внутрибрюшное давление напрямую влияет на центральную нервную систему, приводя к значительному росту внутричерепного давления;
- сердечно-сосудистая система отвечает снижением сердечного выброса и развитием рефрактерного шока.
Лечение
Тактика лечения АКС зависит от причины повышения внутрибрюшного давления, длительности его воздействия и степени органной дисфункции. Терапия включает консервативные и хирургические методы[1]:
- консервативное лечение направлено на снижение объёма содержимого брюшной полости и повышение податливости брюшной стенки. Оно включает декомпрессию желудочно-кишечного тракта с помощью назогастрального зонда и газотводной трубки, лапароцентез или дренирование при наличии гематомы. Также применяются адекватное обезболивание и седация, нейромышечная блокада, устранение сдавливающих повязок. Подход также включает оптимизацию инфузионной терапии, ультрафильтрацию или гемодиализ[1].
- хирургическое лечение показано при неэффективности консервативных мер и прогрессировании органной дисфункции. Золотым стандартом является экстренная лапаротомия (декомпрессионная лапаростомия), которая позволяет быстро нормализовать внутрибрюшное давление. После вскрытия брюшной полости фасцию часто оставляют открытой, используя системы негативного давления для временного закрытия раны. Окончательное закрытие брюшной стенки выполняют через несколько дней при стабилизации состояния пациента. Хирургическая декомпрессия, хотя и является основным методом лечения, сопряжена с риском осложнений. Важным аспектом является определение оптимальных сроков вмешательства, поскольку как преждевременная, так и поздняя операция могут ухудшить исход[1].
Прогноз
АКС характеризуется чрезвычайно высокой летальностью. При отсутствии лечения заболевание почти всегда приводит к летальному исходу. Даже при проведении терапии показатель смертности остаётся очень высоким и, по данным различных исследований, составляет от 25 до 75 %. Например, у пациентов с АКС, развившимся после операции по поводу разрыва аневризмы брюшной аорты, смертность достигает 47 %. Столь неблагоприятный прогноз объясняется тем, что данное состояние приводит к полиорганной недостаточности и, как правило, является следствием изначально критических повреждений или заболеваний, самих по себе несущих высокий риск. Факторами, напрямую ассоциированными с повышенной смертностью, являются[4]:
- массивная гемотрансфузия;
- сопутствующий сахарный диабет в анамнезе;
- внутрибрюшное давление >20 мм рт. ст. при поступлении в стационар;
- концентрация лактата в крови >5 ммоль/л при поступлении, что также связано с повышенным риском острой почечной недостаточности и большей потребностью в переливании крови;
- тупая травма как механизм повреждения;
- развитие синдрома в течение первых 48 часов после госпитализации, что ведёт к значительному увеличению продолжительности искусственной вентиляции лёгких и пребывания в отделении реанимации;
- продолжительность первоначальной операции более 2 часов, что повышает риск развития полиорганной недостаточности.
Диспансерное наблюдение
Пациенты с АКС находятся под наблюдением у хирурга по месту жительства. Объём и частота контрольных обследований определяются индивидуально[1].
Профилактика
Не разработана.
Примечания
Литература
- Тимербулатов Ш.В., Абдуллин У.М., Викторов В.В., Плечев В.В., Гафарова А.Р. Интраабдоминальная гипертензия и абдоминальный компартмент-синдром. Обзор литературы // Креативная хирургия и онкология. — 2024. — Т. 14, № 2. — С. 174—179. — doi:10.24060/2076-3093-2024-14-2-174-179.
- Patel A., Lall C.G., Jennings S.G., Sandrasegaran K. Abdominal Compartment Syndrome (англ.) // American Journal of Roentgenology. — 2007. — Vol. 189, no. 5. — P. 1037—1043. — doi:10.2214/AJR.07.2092.