Каспазы
Каспазы (англ. caspase; сокр. от англ. cysteine-dependent aspartate specific protease) — протеолитические ферменты, относящихся к семейству цистеиновых протеаз, расщепляющих белки исключительно после аспартата. Каспазы играют важную роль в процессах апоптоза, некроза и воспалительных процессах.
Каспазы подразделяют на инициаторные, воспалительные и эффекторные (экзекуторные). Все каспазы первоначально синтезируются в неактивной форме, и активируются по мере необходимости инициаторными каспазами отсечением небольшого участка. Инициаторные каспазы активируются более сложным образом — специальными белковыми комплексами: апоптосомами, PIDD-осомами, DISC. По состоянию на 2009 г. у человека имеется 11 или 12 подтверждённых каспаз и 10 у мышей[note 1], выполняющих разнообразные клеточные функции.
Роль этих ферментов в запрограммированной гибели клеток была впервые определена в 1993 году, а их функции в апоптозе хорошо охарактеризованы. Такая форма запрограммированной гибели клеток, широко распространённая в процессе развития и в течение всей жизни служит для поддержания клеточного гомеостаза. Активация каспаз обеспечивает контролируемое деструкции клеточных компонентов, что приводит к гибели клеток с минимальным воздействием на окружающие ткани (без их вовлечения в процесс)[3].
Каспазы играют другие определённые роли в запрограммированной гибели клеток, таких как пироптоз и некроптоз. Данные формы гибели клеток важны для защиты организма от сигналов клеточного стресса и атаки патогенами. Каспазы также играют роль в воспалении, посредством чего они непосредственно усиливают процессинг провоспалительных цитокинов, таких как про-IL1β. Это сигнальные молекулы, которые позволяют рекрутировать иммунные клетки, атакующих инфицированные клетки или ткани. Существуют и другие идентифицированные роли каспаз, такие как пролиферация клеток, подавление опухолей, дифференцировка клеток, развитие нервной системы, направление аксонов и старение[4].
Дефицит каспазы был идентифицирован как одна из причин развития новообразований. Рост опухоли может происходить за счёт комбинации факторов, в том числе мутации в генах клеточного цикла, которые снимают ограничения роста клеток, в сочетании с мутациями в апоптопных белках, таких как каспазы, которые активируются и вызывают гибель аномально растущих клеток[5]. И наоборот, чрезмерная активация некоторых каспаз, например, каспазы 3, может привести к чрезмерной запрограммированной гибели клеток. Такое являение наблюдается при некоторых нейродегенеративных заболеваниях, когда происходит необратимая потеря нервных клеток, примером служит болезнь Альцгеймера[5]. Каспазы, связанные с процессингом воспалительных сигналов, также вовлечены в протекание многих заболеваний. Недостаточная активация данных каспаз может повысить восприимчивость организма к инфекции, так как соответствующий иммунный ответ может не произойти[5]. Неотъемлемая роль каспаз в гибели клеток и протекании заболеваний привела к исследованию использования ферментов в качестве мишеней для лекарств (таргетная терапия). Например, воспалительная каспаза 1 участвует в патогенезе аутоиммунных заболеваний; препараты, блокирующие активацию каспазы 1, использовались для улучшения здоровья пациентов. Кроме того, учёные использовали каспазы в качестве терапии злокачественных опухолей для уничтожения нежелательных клеток в бластомогенных тканях[6].
Общие сведения
Функциональная классификация каспаз
Большинство каспаз играют роль в запрограммированной гибели клеток. Они обобщены в таблице ниже. Ферменты подразделяются на три типа: инициаторные, эффекторные или экзекуторные и воспалительные[7].
| Запрограммированная смерть клеток | Тип каспазы | Фермент | Организм, в котором обнаружены каспазы |
|---|---|---|---|
| Апоптоз | Инициаторные | Каспаза 2 | человек и мышь |
| Каспаза 8 | человек и мышь | ||
| Каспаза 9 | человек и мышь | ||
| Каспаза 10 | только человек [8] | ||
| Экзекуторные | Каспаза 3 | человек и мышь | |
| Каспаза 6 | человек и мышь | ||
| Каспаза 7 | человек и мышь | ||
| Пироптоз | Воспалительные | Каспаза 1 | человек и мышь |
| Каспаза 4 | человек[note 2] | ||
| Каспаза 5 | человек[note 2] | ||
| Каспаза 11 | мышь[note 2] | ||
| Каспаза 12 | мышь и некоторые люди[note 1] | ||
| Каспаза 13 | только коровы[10] | ||
| Другая роль | Другие | Каспаза 14 | человек и мышь |
Обратите внимание, что в дополнение к апоптозу каспаза 8 также необходима для ингибирования другой формы запрограммированной гибели клеток, называемой некроптозом[11]. Каспаза 14 играет роль в дифференцировке кератиноцитов эпителиальных клеток и может образовывать эпидермальный барьер, который защищает от дегидратации (обезвоживания) и ультрафиолетового излучения[12].
Активация каспаз
Каспазы синтезируются как неактивные зимогены (прокаспазы), которые активируются только после соответствующего стимула. Данный посттрансляционный уровень контроля позволяет быстро и жестко регулировать фермент.
Активация включает димеризацию и часто олигомеризацию прокаспаз с последующим расщеплением на две субъединицы различного размера — большую и малую. Большая и маленькая субъединицы связываются друг с другом, образуя активную гетеродимерную каспазу. Активный фермент в природе часто существует в качестве гетеротетрамера, где димер прокаспазы расщепляется вместе с образованием гетеротетрамера[13].
Активация инициаторных каспаз и воспалительных каспаз инициируется димеризацией, посредством связывания с адапторными белками, имеющих мотивы межбелкового взаимодействия, так называемые фолды смерти. Фолды смерти расположены в структурном домене каспаз, известном как про-домен, его больше в тех каспазах, которые содержат фолды смерти, чем в не содержащих каспазах. Про-домен внутренних исходных инициаторных каспаз и воспалительных каспаз содержит один смертельный фолд, известный как домен активации и рекрутирования каспазы (сокр. CARD), тогда как про-домен внешних инициаторных каспаз содержит два фолда смерти, известных как домены эффектора смерти (сокр. DED)[14][15].
Часто, во время активации каспаз образуются мультипротеиновые комплексы[13]. Некоторые, активирующиеся мультипротеиновые комплексы включают в себя:
- Индуцирующий смерть сигнальный комплекс (сокр. DISC), образуется во время внешней стадии апоптоза
- Апоптосому во время собственного апоптоза
- Инфламмасому во время пироптоза.
После соответствующего процесса димеризации каспазы расщепляются в междоменных линкерных областях, образуя большую и маленькую субъединицу. Такое расщепление позволяет петлям активного сайта принимать конформацию, благоприятную для ферментативной активности[16]. Расщепление инициаторных и эффекторных (экзекуторных) каспаз происходит различными способами, описанными в таблице ниже.
- Инициаторные каспазы подвержены автоматическому протеолизу, тогда как экзекуторные каспазы расщепляются инициаторными каспазами. Такая иерархия позволяет усиливать цепную реакцию или каскад для деградации клеточных компонентов во время контролируемой гибели клеток.
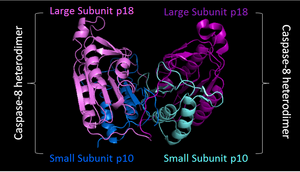
| Инициаторная каспаза
Каспаза 8 |
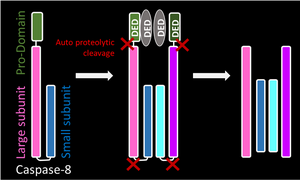 Инициаторная прокаспаза имеет продомен, который позволяет рекрутировать другие прокаспазы, которые впоследствии димеризуются. Обе молекулы прокаспазы подвергаются расщеплению автокаталитическим путём. Это приводит к удалению продомена и расщеплению линкерной области между большой и малой субъединицами. Происходит образование гетеротетрамера. |
|
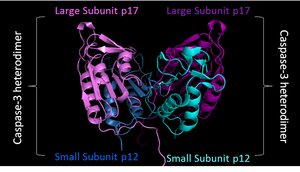
| Экзекуторная каспаза
Каспаза Каспазы 3 |
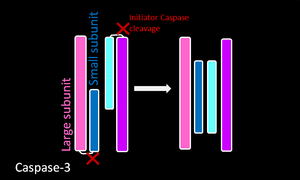 Экзекуторная каспаза конститутивно существует в виде гомодимеров. Красные разрезы представляют области, где инициаторная каспаза расщепляет эффекторную каспазу. Образующиеся малая (p12) и большая субъединица (p17) каждой каспазы 3 в дальнейшем ассоциируется, что приводит к образованию гетеротетрамера. |
Некоторые роли, исполняемые каспазами
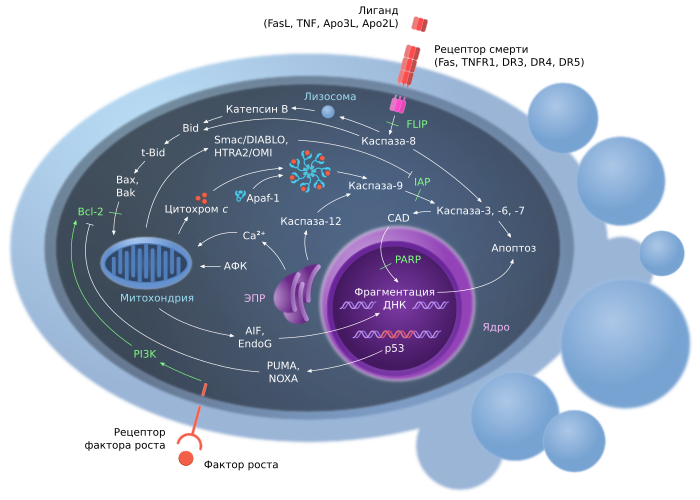
Апоптоз является формой запрограммированной гибели клеток, когда клетка претерпевает морфологические изменения, которые минимизируют своё влияние на окружающие клетки, чтобы избежать индукции иммунного ответа. Клетка сжимается и конденсируется — цитоскелет разрушается, ядерная оболочка разбирается и происходит фрагментация ДНК. Это приводит к тому, что клетки образуют замкнутые тела, называемые «пузырьками», чтобы избежать высвобождения клеточных компонентов во внеклеточную среду. Кроме того, изменяется содержание фосфолипидов в клеточной мембране, что делает умирающую клетку более восприимчивой к фагоцитарной атаке и утилизации[18].
Апоптопические каспазы подразделяются на:
- Инициаторные каспазы (каспаза 2, каспаза 8, каспаза 9, каспаза 10)
- Эффекторные (экзекуторные) каспазы (каспаза 3, каспаза 6 и каспаза 7)
Как только происходит активация инициаторных каспаз, запускается цепная реакция, приводящая к активации нескольких других эффекторных каспаз. Экзекуторные каспазы разрушают более 600 клеточных компонентов[19], чтобы вызвать морфологические изменения при апоптозе.
Примеры каспазных каскадов, происходящих во время апоптоза:
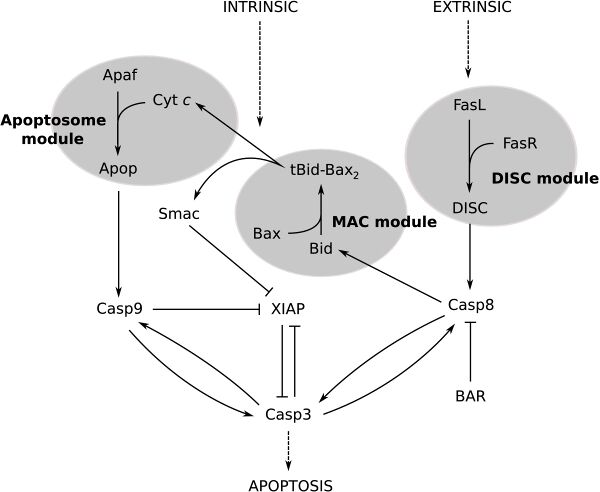
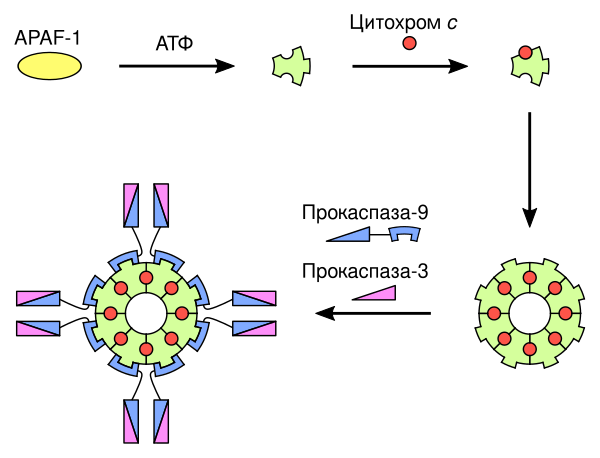
- Внутренний (митохондриальный) сигнальный путь апоптоза: во время клеточного стресса митохондриальный цитохром с высвобождается в цитозоль. Эта молекула связывает адапторный белок (APAF-1), который рекрутирует инициаторную каспазу 9 (посредством взаимодействия CARD-CARD). Это приводит к образованию каспазы, активирующей мультипротеиновый комплекс, называемый апоптосомой. После активации инициаторных каспаз, таких как каспаза 9, происходит расщепление и активация других каспаз-эффекторов. Это приводит к деградации клеточных компонентов при апоптозе.
- Внешний сигнальный путь апоптоза: Каспазный каскад также активируется внеклеточными лигандами посредством рецепторов смерти, расположенных на клеточной поверхности. Это достигается путём формирования полипротеинового сигнального комплекса смерти (DISC), который рекрутирует и активирует прокаспазу. Например, лиганд FasL связывает рецептор FasR на внеклеточной поверхности рецептора; связывание активирует домены смерти в цитоплазматическом хвосте рецептора. Адаптерный белок FADD будет рекрутировать (посредством взаимодействия домена смерти и домена смерти) прокаспазу 8 через домен DED. Данные белки FasR, FADD и прокаспаза 8 образуют сигнальный комплекс, вызывающий смерть (DISC), в котором активируется каспаза 8. Это может привести либо к нисходящей активации внутреннего пути путём индукции митохондриального стресса, либо к прямой активации каспаз-экзекуторов (каспаза 3, каспаза 6 и каспаза 7), предназначенных для разрушения клеточных компонентов, как показано внизу на обобщённой схеме[20].
Пироптоз является одной из форм запрограммированной гибели клеток, которая по своей природе вызывает иммунный ответ. Он морфологически отличается от других типов гибели клеток — клетки набухают, разрываются и выделяют провоспалительное клеточное содержимое. Это происходит в ответ на ряд раздражителей, включая микробные инфекции, а также сердечные приступы (например, происходящие при инфаркте миокарда)[21]. Каспаза 1, каспаза 4 и каспаза 5 у людей и каспаза 1 и каспаза 11 у мышей играют важную роль в индукции гибели клеток при пироптозе. Данный процесс ограничивает жизнь и время пролиферации внутриклеточных и внеклеточных патогенов.
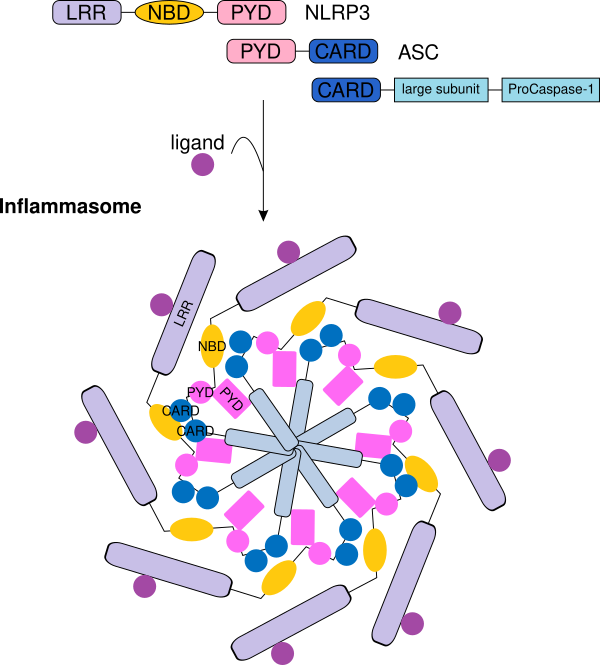
Активация каспазы 1 опосредована репертуаром белков, что позволяет выявлять целый ряд патогенных лигандов. Некоторыми медиаторами активации каспазы 1 являются: NOD-подобные рецепторы (NLRs), AIM2-подобные рецепторы (ALRs), Пирин и IFI16[22]. Данные белки позволяют активировать каспазу 1 путём образования активирующего мультипротеинового комплекса, называемого инфламмасомой.
Например, NOD-подобный обогащённый лейцином повтор, NLRP3 чувствителен к оттоку ионов калия из клетки. Этот клеточный ионный дисбаланс приводит к олигомеризации молекул NLRP3 с образованием мультипротеинового комплекса, называемого NLRP3-инфламмасомой. Прокаспаза 1 приводится в непосредственную близость с другой молекулой прокаспазы, происходит дальнейший процесс димеризации и аутопротеолитическое расщеплению[22].
Некоторые патогенные сигналы, которые приводят к пироптозу, вызванный активацией каспазой 1, перечислены ниже:
- ДНК в цитозоле клетки связывается с AIM2-подобными рецепторами, вызывающими пироптоз
- Аппарат бактериальной системы секреции III типа (встречается у бактерий Yersinia, Salmonella и Shigella[23]) связывается с NOD-подобным богатым лейцином повтором, называемым NAIP (NAIP1 у человека и NAIP4 у мышей).
Эти каспазы обладают способностью вызывать прямой пироптоз, когда молекулы липополисахарида (LPS) (обнаруженные в клеточной стенке грамотрицательных бактерий) проникают и идентифицируются в цитоплазме клетки-хозяина. Например, каспаза 4 действует как рецептор и протеолитически активируется без необходимости в инфламмасоме или без активации каспазы 1[22].
Важнейшим нижестоящим субстратом для пироптопических каспаз является гасдермин D (GSDMD)[24].
Воспаление представляет собой как защитную реакцию организма в результате негативного воздействия вредного раздражителя, таких как повреждение ткани или бактериальная инфекция и направленную на восстановление равновесного (нормального) гомеостатического состояния[19].
Каспаза 1, каспаза 4, каспаза 5 и каспаза 11 считаются воспалительными каспазами[7].
- Каспаза 1 является ключевой в активации провоспалительных цитокинов; они действуют как сигналы для иммунных клеток и создают благоприятную среду для рекрутирования иммунных клеток в месте повреждения. Поэтому каспаза 1 играет фундаментальную роль во врождённой иммунной системе. Фермент отвечает за процессинг цитокинов, таких как pro-ILβ и pro-IL18, а также за их секрецию (выделение)[22].
- Каспаза 4 и 5 у человека и каспаза 11 у мышей играют уникальную роль в качестве рецептора, благодаря чему они связываются с LPS, молекулой, которой богаты поверхности клеток грамотрицательных бактерий. Связывание может привести к процессингу и секреции цитокинов IL-1β и IL-18 путём активации каспазы 1; этот последующий эффект такой же, как описано выше. Это также приводит к секреции другого воспалительного цитокина, который не подвержен процессингу. Молекула цитокина называется про-IL1α. Также имеются данные о воспалительной каспазе, способствующей секреции цитокинов, осуществляемой каспазой 11; процесс происходит путём инактивации мембранного канала, который блокирует секрецию IL-1β[22].
- Каспазы могут также вызывать воспалительный ответ на транскрипционном уровне. Существуют доказательства того, что данный воспалительный ответ способствует транскрипции ядерного фактора-κB (NF-κB), транскрипционного фактора, который помогает транскрибировать воспалительные цитокины, такие как IFN, TNF, IL-6 и IL-8. Например, каспаза 1 активирует каспазу 7, которая в свою очередь расщепляет поли(АДФ-рибоза)-полимеразу — это активирует транскрипцию генов, контролируемых NF-κB[19].
Открытие каспаз
Роберт Хорвиц первоначально установил важность каспаз при апоптозе и обнаружил, что ген ced-3 необходим для гибели клеток, которая произошла во время развития нематоды C. elegans. Хорвиц и его коллега Джуниинг Юань обнаружили в 1993 году, что белок, кодируемый геном ced-3, представляет собой цистеиновую протеазу со свойствами, аналогичными ферменту, интерлейкин-1-бета превращающему у млекопитающих (ICE) (в настоящее время известный как каспаза 1). В то время ICE была единственной известной каспазой[25]. Впоследствии были идентифицированы каспазы других млекопитающих, в дополнение к каспазам, втречаемых в организмах, как, например у плодовой мухи Drosophila melanogaster.
Исследователи определились с номенклатурой каспаз в 1996 году. Во многих случаях конкретная каспаза была идентифицирована одновременно более чем одной лабораторией; каждая из которых тогда дали белкам различные наименования. Например, каспаза 3 была по-разному известна как CPP32, апопаин и Yama. Поэтому каспазы были пронумерованы в том порядке, в котором они были идентифицированы[26]. Поэтому ICE был переименован в каспазу 1. ICE был первой каспазой млекопитающих, которая была охарактеризована из-за её сходства с геном гибели нематод ced-3, но, по-видимому, основная роль этого фермента заключается в опосредовании воспаления, нежели в гибели клеток.
Эволюция
У животных апоптоз индуцируется каспазами, а у грибов и растений апоптоз индуцируется аргинин- и лизин-специфической каспазоподобной протеазой, называемой метакаспазой. Поиск гомологии выявил тесную гомологию между каспазами и каспазоподобными белками Reticulomyxa (одноклеточного организма). Филогенетическое исследование показывает, что расхождение последовательностей каспазы и метакаспазы происходило до расхождения эукариот[27].
Литература
- Обзор: Human caspases: activation, specificity, and regulation. Pop C, Salvesen GS. J Biol Chem. 2009 Aug 14;284(33):21777-81. Epub 2009 May 26. PMID 19473994