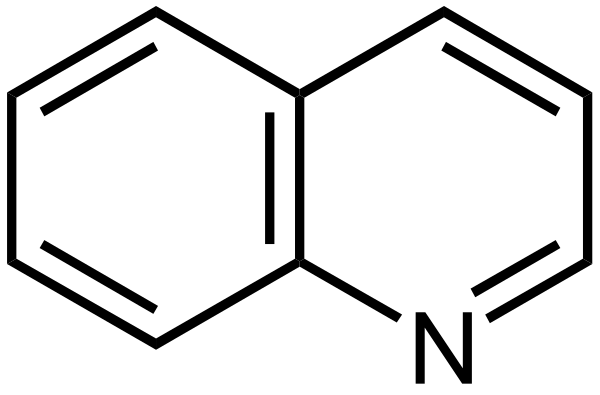
Хинолин
Хиноли́н (бензопиридин) — органическое соединение гетероциклического ряда. Применяют как растворитель для серы, фосфора и др., для синтеза органических красителей. Производные хинолина используют в медицине (плазмоцид, хинин).
Общие сведения
| Хинолин | |
|---|---|
| Общие | |
| Хим. формула | C9H7N |
| Физические свойства | |
| Молярная масса | 129,16 г/моль |
| Плотность | 1,093 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -15 °C |
| • кипения | 237,1 °C |
| Энтальпия | |
| • образования | 174,9 |
| Классификация | |
| Рег. номер CAS | 91-22-5 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 7047 |
| UNII | E66400VT9R |
| CompTox Dashboard EPA | DTXSID1021798 |
| Рег. номер EINECS | 202-051-6 |
| SMILES | |
| InChI | |
| RTECS | VA9275000 |
| ChEBI | 17362 |
| Номер ООН | 2656 |
| ChemSpider | 6780 |
| ECHA InfoCard | 100.001.865 |
| Безопасность | |
| NFPA 704 | |
Физические и химические свойства
Промышленное получение
Хинолин встречается в составе каменноугольной смолы, из которой и добывается.
Методы синтеза
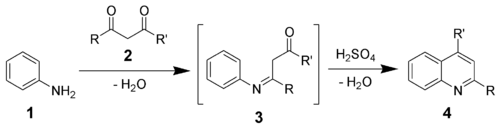
- Производные хинолина с заместителями в положениях 2 и 4 можно получить путём конденсации анилина (1) и β-дикетонов (2) в кислой среде. Этот метод получил название «синтез хинолинов по Комба»
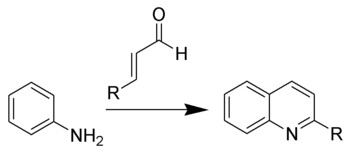
- Из анилина и α,β-ненасыщеных альдегидов (метод Дёбнера-Миллера). Механизм данной реакции очень близок к механизму реакции Скраупа
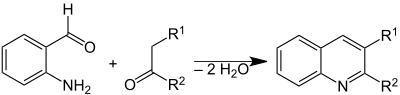
- Из 2-аминобензальдегида и карбонильных соединений, содержащих α-метиленовую группу (синтез Фридлендера). Метод практически не употребляется из-за низкой доступности о-карбонильных производных анилина
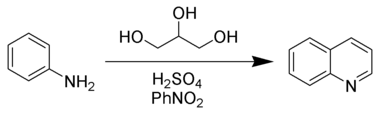
- Конденсацией анилина и глицерина в присутствии серной кислоты (метод Скраупа)
Механизм этой реакции точно не установлен, но предполагают, что процесс идет как 1,4-присоединение анилина к акролеину. Акролеин образуется в результате дегидратации глицерина в присутствии серной кислоты (образование акролеина подтверждено: из готового акролеина и анилина также образуется хинолин).
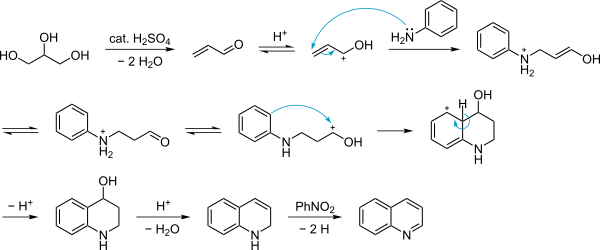
Реакция сильно экзотермична, поэтому процесс обычно проводят в присутствии сульфата железа (II). В качестве окислителя используют также оксид мышьяка (V), в этом случае процесс протекает не так бурно, как с нитробензолом, и выход хинолина выше.
- По реакции Поварова из бензальдегида, анилина и алкена.
- Из орто-ацилацетофенона и гидроксида (en:Camps quinoline synthesis).
- Из β-кетоанилида (en:Knorr quinoline synthesis).
- Из анилина и β-кетоэфиров[3] (en:Conrad-Limpach synthesis).
- en:Gould-Jacobs reaction
Токсикология и безопасность
Опасен при попадании в глаза и приёме внутрь, ирритант, канцероген. ЛД50 для крыс — 331—460 мг/кг (орально), для кроликов — 540 мг/кг (трансдермально)[4].
Примечания
Литература
- Гончаров А. И., Корнилов М. Ю. Справочник по химии. — 2-е. — К.: Вища школа, 1978.
- Гетероциклические соединения / Под ред. Эльдерфилда Р.. — М.: Издательство иностранной литературы, 1955. — Т. 4.