Анилин
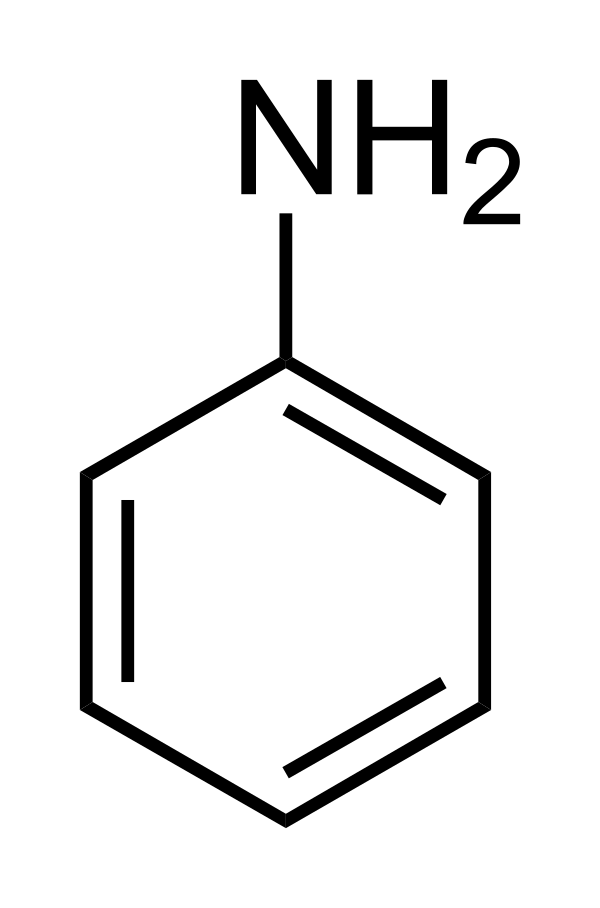
Анили́н (аминобензол, фениламин) — органическое соединение с формулой C6H5NH2, родоначальник класса ароматических аминов. Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного плотнее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Весьма токсичен. Название «анилин» происходит от названия одного из растений, содержащих индиго — Indigofera anil (современное международное название растения — Indigofera suffruticosa).
Общие сведения
| Анилин | |
|---|---|
| Общие | |
| Традиционные названия |
Аминобензол Анилин Бензоламин Фениламин |
| Хим. формула | C6H5NH2 |
| Рац. формула | C6H7N |
| Физические свойства | |
| Состояние | бесцветная или желтоватая жидкость |
| Молярная масса | 93,1265 ± 0,0055 г/моль |
| Плотность | 1,0217 г/см³ |
| Поверхностное натяжение | 43,3 Н/м |
| Динамическая вязкость | 3,71 Па·с |
| Энергия ионизации | 7,7 ± 0,1 |
| Скорость звука в веществе | 1659 м/с |
| Термические свойства | |
| Температура | |
| • плавления | −6,3 °C |
| • кипения | 184,13 °C |
| • вспышки | 158 ± 1 и 76 |
| • самовоспламенения | 562 °C |
| Пределы взрываемости | 1,3 ± 0,1 |
| Критическая точка | |
| • температура | 425,65 °C |
| • давление | 5,134 МПа |
| Критическая плотность | 0,314 см³/моль |
| Давление пара | 0,6 ± 0,1 |
| Химические свойства | |
| Растворимость | |
| • в воде | 3,6 г/100 мл |
| • в циклогексане | 66,7 (30,8°C) |
| Диэлектрическая проницаемость | 6,89 |
| Оптические свойства | |
| Показатель преломления | 1,5863 |
| Структура | |
| Дипольный момент | 1,53 Д |
| Классификация | |
| Рег. номер CAS | 62-53-3 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 6115 |
| UNII | SIR7XX2F1K |
| CompTox Dashboard EPA | DTXSID8020090 |
| Рег. номер EINECS | 200-539-3 |
| SMILES | |
| InChI | |
| RTECS | BW6650000 |
| ChEBI | 17296 |
| Номер ООН | 1547 |
| ChemSpider | 5889 |
| ECHA InfoCard | 100.000.491 |
| Безопасность | |
| Предельная концентрация | 0,3 мг/м3 |
| ЛД50 |
9-12 мг/кг (кошки, внутрижелудочно), 132 мг/кг (мыши, внутрижелудочно) |
| Токсичность | Чрезвычайно токсичен для мелких млекопитающих, высокотоксичен для человека, является гематотоксином (вызывает гемолиз). |
| Пиктограммы ECB |
|
| NFPA 704 | |
История
Впервые анилин был получен в 1826 году при перегонке индиго с известью немецким химиком Отто Унфердорбеном, который дал ему название «кристаллин».
В 1834 году Фридлиб Фердинанд Рунгe обнаружил анилин в каменноугольной смоле и назвал «кианолом».
В 1840 году Юлий Фрицше получил анилин нагреванием индиго с раствором гидроксида калия и назвал его «анилином».
В 1842 году Николай Зинин получил анилин восстановлением нитробензола действием (NH4)2S и назвал его «бензидамом».
В 1843 году Август Вильгельм Гофман установил идентичность всех перечисленных соединений.
Промышленное производство фиолетового красителя мовеина на основе анилина началось в 1856 году.
Получение
В промышленности анилин получают в две стадии.
На первой стадии бензол нитруется смесью концентрированной азотной и серной кислот при температуре 50—60 °C, в результате образуется нитробензол:
На втором этапе нитробензол гидрируют при температуре 200—300 °C в присутствии катализаторов:
Впервые восстановление нитробензола было произведено с помощью железа:
Другим способом получение анилина является восстановление нитросоединений — реакция Зинина:
Также, в анилин — идёт восстановление нитробензола цинком в присутствии избытка соляной кислоты.
;
;
И этот избыток связывает образующийся анилин в соль под названием хлорид фениламмония (анилин солянокислый):
;
Эта соль легко растворима в образующейся при этом воде и может быть выкристаллизована из неё,
к тому же после обработки щёлочью хлорид фениламмония — даёт анилин:
Химические свойства
Для анилина характерны реакции как по аминогруппе, так и по ароматическому кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов. С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению с алифатическими аминами и даже с аммиаком. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. Хорошо галогенируется, нитруется и сульфируется. Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок). С HNO2 даёт диазосоединения.
В отличие от аминов алифатического ряда, ароматические амины легко окисляются. Примером может служить реакция хромовой смеси с анилином, в результате образуется краситель «чёрный анилин».
Классическая реакция окисления анилина дихроматом калия в кислой среде часто используется как качественная реакция на анилин:
Аналитическим эффектом в данном случае служит появление окраски раствора от тёмно-синей до чёрной. Как и в большинстве реакций окисления анилина, продуктами являются различные Хиноны.
Другой качественной реакцией на анилин, очень чувствительной, является окисление анилина хлорной известью, при котором появляется фиолетовое окрашивание[1].
Аминогруппа, являясь заместителем первого рода, оказывает сильное активирующее влияние на бензольное кольцо, из-за чего при нитровании может произойти окисление молекулы анилина. Для предотвращения окисления аминогруппу перед нитрованием «защищают» ацилированием.
С азотистой кислотой образует катион диазония, например:
Эта реакция может быть использована для получения фенола, если вместо соляной кислоты использовать разбавленную серную:
Где сначала образуется та же диазониевая соль, которая при нагревании в разбавленном водном растворе гидролизуется и разлагается до фенола, при этом выделяется молекулярный азот.
В связи с нестойкостью азотистой кислоты её часто заменяют нитритом щёлочного металла в кислой среде. Диазониевые соли используют для реакции Зандмейера.
Гидрирование анилина в присутствии никелевого катализатора даёт циклогексиламин.
Анилин взаимодействует с соляной кислотой с образованием хлорида фениламмония[2]:
Анилин взаимодействует с бромом и даже бромной водой с образованием 2,4,6-триброманилина[3]:
Производство и применение
Изначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход анилина не превышал 15 %. При взаимодействии концентрированной соляной кислоты с железом выделялся атомарный водород, более химически активный по сравнению с молекулярным. Реакция Зинина является более эффективным методом получения анилина. В реакционную массу вливали нитробензол, который восстанавливается до анилина.
По состоянию на 2002 год, в мире основная часть производимого анилина используется для производства метилдиизоцианатов, используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков, гербицидов и красителей (фиолетового красителя мовеина)[4].
В России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты), но в связи с ожидаемым ростом производства полиуретанов возможно значительное изменение картины в среднесрочной перспективе.
Биологические свойства
![]() Анилин — высокотоксичное вещество. В больших концентрациях фениламин оказывает негативное воздействие на центральную нервную систему. Кровеносный яд, вызывает кислородное голодание организма за счёт образования в крови метгемоглобина, гемолиза и дегенеративных изменений эритроцитов.
Анилин — высокотоксичное вещество. В больших концентрациях фениламин оказывает негативное воздействие на центральную нервную систему. Кровеносный яд, вызывает кислородное голодание организма за счёт образования в крови метгемоглобина, гемолиза и дегенеративных изменений эритроцитов.
В организм анилин проникает при дыхании, в виде паров, а также через кожу и слизистые оболочки. Всасывание через кожу усиливается при нагреве воздуха или приёме алкоголя.
При лёгком отравлении анилином наблюдаются слабость, головокружение, головная боль, синюшность губ, ушных раковин и ногтей. При отравлениях средней тяжести также наблюдаются тошнота, рвота, иногда, шатающаяся походка, учащение пульса. Тяжёлые случаи отравления аминобензолом крайне редки.
При хроническом отравлении анилином (анилизм) возникают токсический гепатит, а также нервно-психические нарушения, расстройство сна, снижение памяти и т. д.
При отравлении анилином необходимо прежде всего удаление пострадавшего из очага отравления, обмывание тёплой (но не горячей) водой. Также применяют введение антидотов (метиленовая синь), сердечно-сосудистые средства или вдыхание карбогена. Пострадавшему надо обеспечить покой.
Предельно допустимая концентрация анилина в воздухе рабочей зоны 0,3 мг/м3[5] по ГОСТ 313-77. В водоёмах (при их промышленном загрязнении) — ПДК 0,1 мг/л (100 мг/м3)[6][7].
В соответствии с ГОСТ 12.1.007-76 аминобензол относится ко II классу опасности[8].
Охрана труда
Примечания
Литература
- Артёменко А. И. Органическая химия. — М.: «Высшая школа», 1987. — 430 с.
Ссылки
- Анилин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.

![{\displaystyle {\ce {C6H6 + HNO3 ->[H_2SO_4,50-60 C] C6H5NO2 + H2 O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/94e657028b4ce44e1f33f4b53a5e6a1e189b0ee5)




![{\displaystyle {\mathsf {C_{6}H_{5}NH_{2}+HCl\rightarrow [C_{6}H_{5}NH_{3}]^{+}Cl^{-}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/e1eb5f1a9f158fc6376f0e212dc540301d158558)
![{\displaystyle {\mathsf {[C_{6}H_{5}NH_{3}]^{+}Cl^{-}+Na^{+}OH^{-}{\xrightarrow[{}]{NaOH,\ -NaCl}}\ C_{6}H_{5}NH_{2}+NaCl+H_{2}O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/668ac6b51e55cadc2421df4b39b8d5d5838f2fd2)




![{\displaystyle {\mathsf {C_{6}H_{5}NH_{2}+HCl\rightarrow [C_{6}H_{5}NH_{3}]Cl}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/78450d6ad90e95d4f74b59f0422258d6e4054c31)