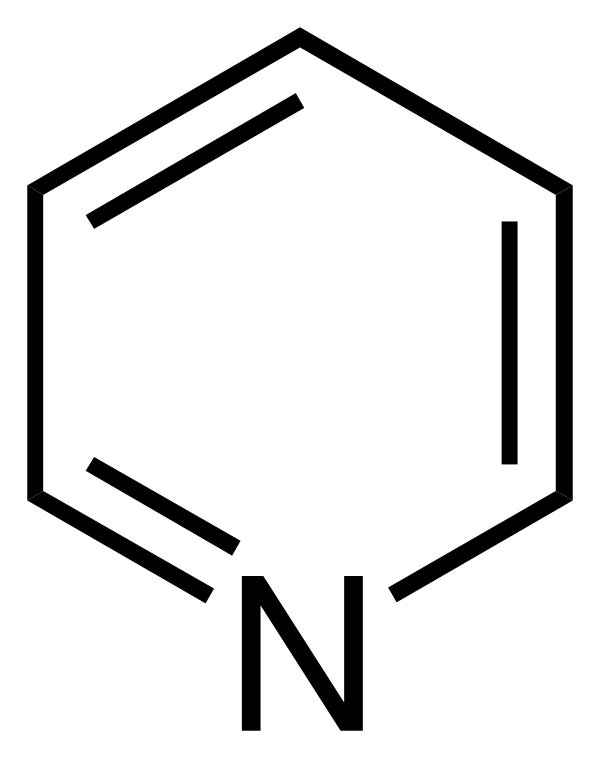
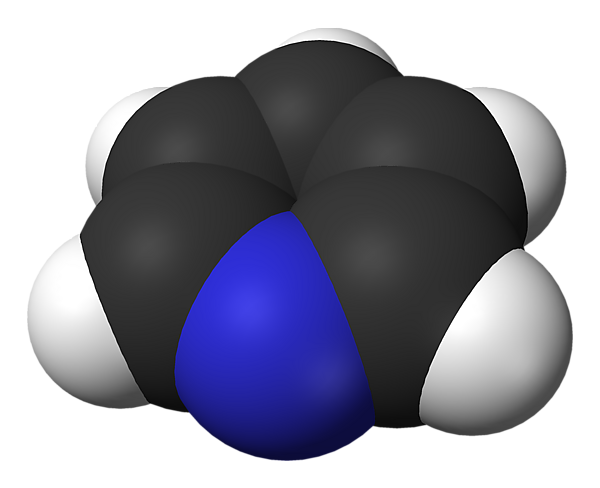
Пиридин
Пириди́н (Py, ази́н, 1-азациклогекса-1,3,5-триен) — органическое вещество, шестичленный ароматический гетероцикл с одним атомом азота, бесцветная жидкость с резким неприятным запахом; смешивается с водой и органическими растворителями. Образует азеотропную смесь с водой, содержащую 59,5 % пиридина (по массе) и кипящую при атмосферном давлении при температуре 93,0 °C[4]. Пиридин — слабое основание, даёт соли с сильными минеральными кислотами, легко образует двойные соли и комплексные соединения.
Общие сведения
| Пиридин | |
|---|---|
| Общие | |
| Систематическое наименование |
азин, пиридин |
| Традиционные названия | пиридин, азациклогексатриен |
| Хим. формула | C5H5N |
| Рац. формула | C5H5N |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 79,101 г/моль |
| Плотность | 0,9819 г/см³ |
| Динамическая вязкость | 0,94 Па·с |
| Энергия ионизации | 9,27[1] |
| Термические свойства | |
| Температура | |
| • плавления | −41,6 °C |
| • кипения | 115,6 °C |
| • вспышки | 68[1] |
| Пределы взрываемости | 1,8[1] |
| Давление пара | 16[1] |
| Классификация | |
| Рег. номер CAS | 110-86-1 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 1049 |
| UNII | NH9L3PP67S |
| CompTox Dashboard EPA | DTXSID9021924 |
| Рег. номер EINECS | 203-809-9 |
| SMILES | |
| InChI | |
| RTECS | UR8400000 |
| ChEBI | 16227 |
| ChemSpider | 1020 |
| ECHA InfoCard | 100.003.464 |
| Безопасность | |
| Предельная концентрация | 0,6 мг/м³[2] |
| Токсичность | Обладает общетоксическим действием. Среднесмертельная доза для крыс составляет около 100-145 мг/кг[3] |
| NFPA 704 | |
История открытия
Пиридин был известен ещё алхимикам, но первое письменное описание этого вещества было сделано шотландским химиком Томасом Андерсоном в 1851 году. Он обнаружил его при исследовании костяного масла, получающегося сухой перегонкой необезжиренных костей. Среди прочих веществ, была получена бесцветная жидкость с неприятным запахом. В 1869 году Кернер в частном письме к Канниццаро высказал мысль, что пиридин можно рассматривать как бензол, в котором одна группа СН замещена азотом. По мнению Кернера, подобная формула не только объясняет синтезы пиридина, но, главным образом, указывает, почему простейший член ряда пиридиновых оснований имеет пять атомов углерода. Через год Дьюар независимо от Кернера пришёл к той же формуле, которая затем нашла подтверждение и в работах других химиков. Позже изучением структуры пиридина занимались Томсен, Бамбергер и Пехманн, Чамичан и Деннштедт. В 1879 году А. Вышнеградский высказал мнение, что все растительные основания, возможно, являются производными пиридина или хинолина, а в 1880 году Кенигс даже предлагал называть алкалоидами только те растительные основания, которые могут рассматриваться как производные пиридина. Однако сейчас границы понятия «алкалоиды» значительно расширились.
Получение
Основным исходным материалом для получения пиридина является каменноугольная смола.
Одним из методов промышленного синтеза пиридина и 2-алкилпиридинов, например, 2-метилпиридина является циклизация по Бённеманну. Она предполагает образование молекулы пиридина из двух молекул ацетилена и одной молекулы циановодорода или какого-либо нитрила в присутствии катализатора. Катализатором являются соединения кобальта, преимущественно, кобальтоцен:
Химические свойства
Пиридин проявляет свойства, характерные для третичных аминов: образует N-оксиды, соли N-алкилпиридиния, способен выступать в качестве сигма-донорного лиганда.
В то же время пиридин обладает явными ароматическими свойствами. Однако наличие в кольце сопряжения атома азота приводит к серьёзному перераспределению электронной плотности. В таких реакциях реагируют преимущественно мета-положения кольца.
Для пиридина характерны реакции ароматического нуклеофильного замещения, протекающие преимущественно по мета-положениям кольца. Такая реакционная способность свидетельствует о электроннодефицитной природе пиридинового кольца, что может быть обобщено в следующем эмпирическом правиле: реакционная способность пиридина как ароматического соединения примерно соответствует реакционной способности нитробензола.
Применение
Применяют в синтезе красителей, лекарственных веществ, инсектицидов, в аналитической химии, как растворитель многих органических и некоторых неорганических веществ, для денатурирования спирта.
Охрана труда
Пиридин ядовит[5], обладает общетоксическим действием. Его ОБУВ[6] в воздухе рабочей зоны 0,6 мг/м³[7]. Порог восприятия запаха этого вещества может достигать 39 мг/м3 (среднее значение в группе)[8]
Для защиты от пиридина следует использовать замену фильтров и изменение технологии и средства коллективной защиты.
См. также
Примечания
Литература
- Д. А. Хардин. Пиридин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.