Синдром Хайду — Чейни
Синдро́м Ха́йду — Че́йни (СХЧ; акроостео́лиз с остеопоро́зом и измене́ниями че́репа и ни́жней че́люсти, артродентоостеодисплази́я, домина́нтный тип акроостео́лиза, синдро́м Че́йни или синдро́м змееви́дной малоберцо́вой ко́сти — поликисто́за по́чек) представляет собой редкое генетическое заболевание скелета, характеризующееся аутосомно-доминантным типом наследования. Основные проявления заболевания включают прогрессирующий акроостеолиз фаланг кистей и стоп, генерализованный остеопороз, специфические черепно-лицевые аномалии и низкорослость. Кроме того, синдром может сопровождаться широким спектром других клинических симптомов, что делает его течение вариабельным[1].
Общие сведения
История
Впервые заболевание было описано в 1948 году британскими врачами Хайду и Каунтце как «черепно-скелетная дисплазия». Они наблюдали 37-летнего мужчину с базилярной импрессией и выраженным остеопорозом. В 1965 году американский радиолог Чейни описал похожее состояние в семье из Мичигана, назвав его «акроостеолиз». В исследовании участвовали женщина и четверо её детей, у которых отмечались акроостеолиз, дополнительные костные включения в черепных швах, недоразвитие нижнечелюстной ветви, остеопороз и базилярная импрессия. В 1973 году Геррманн и коллеги, проанализировав ранее описанные случаи и добавив новый, предложили термин «артро-денто-остеодисплазия», а также ввели эпоним «синдром Хайду — Чейни». Они впервые предположили аутосомно-доминантный тип наследования. В 2001 году Бреннан и Паули на основе наблюдений за шестью пациентами из двух семей и анализа предыдущих публикаций разработали диагностические критерии синдрома для детей и взрослых. В 2011 году две независимые исследовательские группы (Симпсон с соавторами и Изидор с коллегами) обнаружили у пациентов с клинически подтверждённым СХЧ гетерозиготные мутации в 34-м экзоне гена NOTCH2, расположенного на хромосоме 1p12[1].
Классификация
Не разработана[2].
Этиология
В основе СХЧ лежит мутация в 34-м экзоне гена NOTCH2, который является терминальным экзоном этого гена. Причиной развития заболевания становятся либо нонсенс-мутации, либо делеции, приводящие к сдвигу рамки считывания и образованию стоп-кодона в 34-м экзоне NOTCH2[2].
Патогенез
Notch представляет собой семейство из четырёх трансмембранных рецепторов, которые активируются при взаимодействии с классическими лигандами — мембранными белками Jagged1/2 и дельта-подобными лигандами (Dll1,3,4). После связывания лиганда γ-секретазный комплекс (содержащий протеазы пресенилин-1/2) расщепляет трансмембранный домен Notch, что приводит к высвобождению внутриклеточного домена и его транспорту в ядро. В ядре внутриклеточный домен взаимодействует с ДНК-связывающим белком CSL, формируя транскрипционный комплекс, регулирующий экспрессию генов-мишеней[3].
В процессе эмбриогенеза Notch-сигналинг играет ключевую роль в сегментации осевого скелета во время сомитогенеза. В зачатках конечностей активация этого пути подавляет хондрогенез, преимущественно через индукцию транскрипционного фактора Hes1[3].
В зрелой костной ткани Notch выполняет важные регуляторные функции, влияя на дифференцировку и активность как остеобластов, так и остеокластов. Особенностью его действия является зависимость эффектов от стадии дифференцировки клеток-мишеней. На ранних этапах остеогенеза Notch подавляет созревание остеобластных предшественников, что приводит к угнетению процессов образования костей. В то же время в зрелых остеобластах и остеоцитах активация Notch-сигналинга оказывает противоположное действие — увеличивает трабекулярную костную массу за счёт подавления остеокластогенеза и костной резорбции, что опосредуется индукцией синтеза остеопротегерина[3].
В основе заболевания лежат либо нонсенс-мутации, либо делеции, приводящие к сдвигу рамки считывания и образованию стоп-кодона в 34-м экзоне NOTCH2 выше PEST-домена. PEST-домен содержит последовательности, необходимые для убиквитинилирования и последующей деградации белка NOTCH2 в протеасоме. В результате мутаций образуется стабильный, неразрушаемый белок, что приводит к постоянной активации NOTCH2-сигнального пути. Это происходит потому, что все ключевые последовательности, необходимые для формирования транскрипционного комплекса Notch, расположены выше PEST-домена и остаются неповреждёнными[2].
Эпидемиология
СХЧ представляет собой крайне редкое заболевание — в медицинской литературе описано менее 100 случаев, однако точная распространённость патологии остаётся неизвестной[2].
Диагностика
СХЧ представляет собой сложное мультисистемное заболевание с характерной клинической картиной, включающей несколько ключевых проявлений[1]:
- наиболее типичными признаками являются прогрессирующий акроостеолиз дистальных фаланг пальцев кистей и стоп, выраженный остеопороз с патологическими переломами, а также специфические черепно-лицевые аномалии и низкорослость. Заболевание отличается значительной клинической вариабельностью — симптомы развиваются постепенно и могут существенно различаться у разных пациентов. При рождении дети обычно не имеют выраженных внешних особенностей, за исключением микрогнатии, которая выявляется более чем у половины новорождённых;
- в раннем возрасте могут отмечаться антимонголоидный разрез глаз, гипертелоризм, уплощённая переносица и низко посаженные уши. С возрастом формируется характерный фенотип: долихоцефалическая форма черепа с батроцефалией, густые сросшиеся брови, длинные ресницы, уплощение средней трети лица, широкий нос с выступающими ноздрями, высокое арочное небо, микрогнатия и аномалии зубов, приводящие к их ранней потере. Акроостеолиз обычно развивается в позднем детском или подростковом возрасте, начинаясь с указательного и среднего пальцев, и сопровождается укорочением и деформацией ногтевых пластинок;
- генерализованный остеопороз проявляется патологическими переломами и прогрессирующими деформациями позвоночника. Среди других возможных проявлений отмечаются гипермобильность суставов, гирсутизм, нарушения слуха, рецидивирующие респираторные инфекции в детстве, врождённые пороки сердца и поликистоз почек. Заболевание имеет прогрессирующий характер с постепенным нарастанием костных изменений и ухудшением состояния пациентов, при этом интеллектуальное развитие обычно остаётся сохранным, хотя возможна задержка нервно-психического развития в раннем детстве[1].
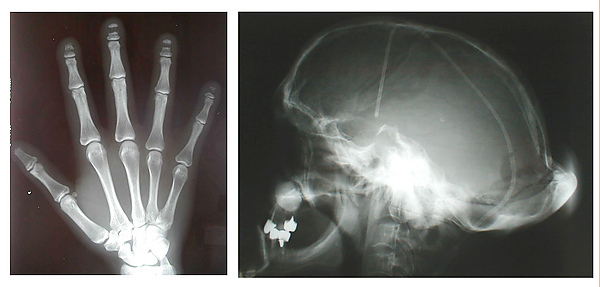
У пациентов с СХЧ наблюдаются характерные рентгенологические изменения: наиболее типичным признаком является акроостеолиз дистальных фаланг кистей и стоп. При рентгенографии черепа выявляются незаращенные швы, уплощение основания черепа, удлинённое турецкое седло и отсутствие лобных пазух. Исследование позвоночника демонстрирует снижение костной массы и компрессионные переломы[2].
Двухэнергетическая рентгеновская абсорбциометрия позволяет обнаружить снижение минеральной плотности костной ткани в сравнении с нормой[2].
Молекулярно-генетический анализ: характерно выявление мутации гена NOTCH2 методом секвенирования[1].
В биохимическом анализе крови возможно повышение активности щелочной фосфатазы[2].
В 2001 году Бреннан и Паули разработали диагностические критерии СХЧ, основанные на ключевых клинических признаках и подтверждённом семейном анамнезе[1].
| Диагностические критерии | Верификация диагноза | |
|---|---|---|
| У взрослых | У детей | |
| Акроостеолиз | Акроостеолиз + 3 любых дополнительных диагностических критерия, за исключением задокументированного отягощенного семейного анамнеза, или акроостеолиз + задокументированный отягощенный семейный анамнез, или задокументированный отягощенный семейный анамнез + 2 дополнительных диагностических критерия, кроме акроостеолиза | 4 любых диагностических критерия, за исключением задокументированного отягощенного семейного анамнеза, или задокументированный отягощенный семейный анамнез + 2 дополнительных диагностических критерия |
| Вставочные кости черепа или открытые швы | ||
| Платибазия | ||
| Преждевременная потеря зубов | ||
| Микрогнатия | ||
| Грубые черты лица | ||
| Жёсткие волосы | ||
| Уплощение средней части лица | ||
| Низкий рост (<5 процентиля) | ||
| Задокументированный семейный анамнез | ||
Дифференциальная диагностика
При проведении дифференциальной диагностики СХЧ необходимо учитывать широкий спектр заболеваний, проявляющихся акроостеолизом и/или остеопорозом. У детей акроостеолиз чаще всего наблюдается при генетических нарушениях (особенно при первичной гипертрофической остеоартропатии и различных скелетных дисплазиях), а также при ревматических заболеваниях, псориатическом артрите и системном склерозе. В перечень дифференцируемых состояний также входят гиперпаратиреоз, различные невропатии, последствия локальных травм и термических повреждений (обморожения, ожоги), спинальная дизрафия. Особое внимание следует уделить дифференциации с синдромом Вернера, несовершенным остеогенезом, синдромом Элерса — Данлоса, ключично-черепной дисплазией и идиопатическим ювенильным остеопорозом[1].
В дифференциально-диагностический ряд могут также входить следующие заболевания: склеродермия, системная красная волчанка, синдром Шегрена, ревматоидный артрит, болезнь Рейно, порфирия, псориаз[2].
Осложнения
К возможным осложнения относятся базилярная инвагинация (ведёт к неврологическим нарушениям) или формирование выраженной деформации грудной клетки (может снижать лёгочную вентиляцию)[1].
Лечение
На 2025 год не существует этиотропного лечения СХЧ, вся терапия носит симптоматический характер и направлена преимущественно на коррекцию остеопороза как одного из основных проявлений заболевания. В клинической практике применяются бисфосфонаты и деносумаб, которые демонстрируют способность повышать минеральную плотность костной ткани, однако не оказывают влияния на прогрессирование акроостеолиза. Данные об эффективности этих препаратов в профилактике платибазии и преждевременной потери зубов остаются ограниченными из-за редкости заболевания и отсутствия контролируемых клинических исследований. Тем не менее, учитывая ведущую роль повышенной костной резорбции в патогенезе остеопороза при данном синдроме, применение антирезорбтивной терапии на 2025 год считается патогенетически обоснованным подходом, несмотря на недостаточную доказательную базу[1].
Прогноз
СХЧ является тяжёлым заболеванием с неблагоприятным прогнозом, который во многом зависит от степени поражения различных органов и развития осложнений. Естественное течение болезни приводит к прогрессирующему акроостеолизу и выраженному остеопорозу с патологическими переломами, что существенно увеличивает риски инвалидизации и смертности. Особенно серьёзно прогноз ухудшается при развитии неврологических осложнений[2].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Древаль А. В., Камынина Т. С., Володина М. Н., Коталевская Ю. Ю., Демикова Н. С. Сочетание сахарного диабета 1-го типа и синдрома хайду-ченея // Проблемы эндокринологии. — 2011. — № 6.