Болезнь Шарко — Мари — Тута
James R. Lupski, Jeffrey G. Reid, Claudia Gonzaga-Jauregui, David Rio Deiros, David C.Y. Chen, Lynne Nazareth, Matthew Bainbridge, Huyen Dinh, Chyn Jing, David A. Wheeler, Amy L. McGuire, Feng Zhang, Pawel Stankiewicz, John J. Halperin, Chengyong Yang, Curtis Gehman, Danwei Guo, Rola K. Irikat, Warren Tom, Nick J. Fantin, Donna M. Muzny, Richard A. Gibbs. Whole-Genome Sequencing in a Patient with Charcot–Marie–Tooth Neuropathy (EN) // New England Journal of Medicine. — 2010-04. — Т. 362, вып. 13. — С. 1181–1191. — ISSN 1533-4406 0028-4793, 1533-4406.
Болезнь Шарко — Мари — Тута (ШМТ), или наследственная моторно-сенсорная нейропатия (НМСН) — наследственная периферическая нейропатия с хроническим прогрессирующим течением. При этой болезни больные страдают от слабости и атрофии мышц дистальных отделов конечностей, деформации стоп и кистей, у них наблюдается снижение сухожильных рефлексов, изменение походки, потеря чувствительности в конечностях[2].
Что важно знать
История
Болезнь Шарко — Мари — Тута была впервые обнаружена в 1886 году тремя учёными: Жан-Мартеном Шарко (1825—1893)[3], его ассистентом Пьером Мари (1853—1940)[3] и английским врачом Говардом Генри Тутом (1856—1925)[4]. В своей первой публикации «Об особой форме прогрессирующей мышечной атрофии» Шарко и Мари подтвердили, что подобные случаи были ранее опубликованы в медицинской литературе[5].
В 2010 году болезнь Шарко-Мари-Тута стала одним из первых заболеваний, точная генетическая причина которого была выявлена с помощью секвенирования всего генома. Анализ выявил две мутации в гене SH3TC2, который, как уже известно, связан с болезнью ШМТ. Для лучшего понимания механизма наследования сравнили геном больного человека с геномами его родителей и семи братьев и сестёр, у некоторых из которых было это заболевание, а у других — нет. Выяснилось, что оба родителя являются носителями одной нормальной и одной мутировавшей копии гена SH3TC2 и имеют либо слабо выраженные симптомы, либо не имеют их вовсе. Однако у детей, унаследовавших две мутировавшие копии гена, наблюдались все клинические проявления заболевания[6].
Классификация
НМСН является генетически гетерогенным заболеванием (мутации в различных генах), что отражает сложность его молекулярной основы. НМСН принято разделять на несколько основных типов[7][8].
| Тип | Название | Частота встречаемости | Описание |
|---|---|---|---|
| НМСН 1 | Демиелинизирующий тип | 30 % | Вызывает сильную демиелинизацию, тем самым снижая скорость нервной проводимости. Скорость проведения импульса по срединному нерву снижена и составляет менее 38 м/с. |
| НМСН 2 | Аксональный тип | 20—40 % | В основном поражает аксоны. Клинические симптомы часто менее выражены, чем при НМСН 1. Средняя скорость нервной проводимости обычно не меняется (иногда немного ниже нормы, но в основном выше 38 м/с). |
| НМСН 3 | Болезнь Дежерина-Сотта | Очень редко | Значительное снижение скорости нервной проводимости. |
| НМСН 4 | Спинальный тип | ||
| НМСН 5 | Пирамидальный тип | ||
| НМСН 6 | С атрофией зрительного нерва | ||
| НМСН сцепленная с X-хромосомой | X-образный тип | 10—20 % | Этот тип включает в себя все формы НМСН, которые наследуются по Х-сцепленному типу. Средняя скорость проведения импульса 25-40 м/с. |
Также выделяют промежуточные формы в зависимости от типа наследования и от того, затрагивает ли первичный дефект миелиновую оболочку или аксон[6][8].
Каждый тип далее подразделяется на подтипы, определяемые конкретным мутировавшим геном. Эта генетическая классификация помогает в диагностике, прогнозировании и, возможно, разработке таргетной терапии[6].
Этиопатогенез
Заболевание связано с генетическими мутациями, нарушающими работу важнейших белков в периферических нервах. Эти мутации преимущественно затрагивают белки, необходимые для структуры и функционирования миелиновой оболочки, в том числе периферический миелиновый белок 22 (мутация в гене PMP22), нулевой миелиновый белок (P0/MPZ), коннексин 32 (Cx32/GJB1) и периаксин (PRX), что приводит к демиелинизации. Кроме того, мутации в белках, отвечающих за целостность аксонов, таких как лёгкая цепь нейрофиламента (NF-L), динамин 2 (DNM2), ассоциированный с дифференцировкой ганглиозид-индуцированный белок 1 (GDAP1) и митофузин 2 (MFN2), могут вызывать аксональные формы НМСН. Мутации, затрагивающие ген MFN2, расположенный на 1-й хромосоме, нарушают функцию митохондриальных белков. Мутировавший MFN2 заставляет митохондрии образовывать скопления или агрегаты, ограничивая их движение вдоль аксонов к синапсам и тем самым нарушая синаптическую функцию[9].
При некоторых формах, таких как Х-сцепленная форма НМСН, мутации в гене GJB1 приводят к нарушению работы щелевых контактов в шванновских клетках, что ещё больше ухудшает передачу нервных сигналов[10]. Наследование болезни чаще всего аутосомно-доминантное, однако может быть аутосомно-рецессивным и Х-сцепленным[11] .
Наиболее распространённый тип НМСН 1А имеет аутосомно-доминантный тип наследования и вызван дупликацией участка короткого плеча 17-й хромосомы (17p11.2). Этот участок несёт ген PMP22, кодирующий белок PMP22, который является важным компонентом миелиновой оболочки периферических нервных волокон. В результате дупликации и увеличения дозы гена количество производимого белка PMP22 также увеличивается, что приводит к структурным и функциональным нарушениям миелиновой оболочки. Тип НМСН 1B с аутосомно-доминантным типом наследованием и вызвано мутацией в гене MPZ, который кодирует белок P0, который является ещё одним важным компонентом миелиновой оболочки. Менее распространённые типы НМСН 1C, НМСН 1D и НМСН 1F вызваны мутациями в генах LITAF, EGR2 и NEFL[12].
Эпидемиология
Распространённость в Российской Федерации варьирует от 7,14 до 13,3 на 100 000 населения. Болезнь ШМТ составляет 80 % наследственных невропатий[13].
Диагностика
На разнообразие симптомов и их тяжесть влияет конкретная генетическая мутация, вызывающая заболевание. Некоторые гены связаны с более ранним началом и более тяжёлыми формами НМСН, другие приводят к более лёгким формам с медленным прогрессированием. Кроме того, даже если задействован один и тот же ген, симптомы могут различаться у разных людей[14].
Первые признаки заболевания чаще проявляются в 15—30 лет, реже в дошкольном возрасте. На начальных этапах патологического процесса наиболее типичными клиническими проявлениями служат: неустойчивость походки, снижение мышечной силы и повышенная утомляемость, преимущественно локализующиеся в дистальных отделах нижних конечностей. Пациенты отмечают выраженную утомляемость при длительном стоянии на одном месте, что проявляется характерным «симптомом топтания» — потребностью переминаться с ноги на ногу для уменьшения дискомфорта в мышцах[15] .
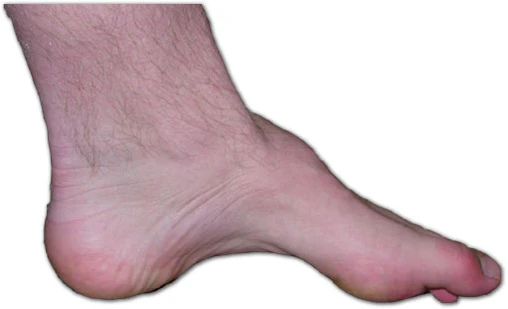
Заболевание также характеризуется развитием симметричных атрофий, первоначально возникающих в мышцах голеней и стоп, с преимущественным поражением перонеальной группы и передней большеберцовой мышцы. Это приводит к характерному сужению дистальных отделов нижних конечностей, которые приобретают форму «перевёрнутых бутылок» или «ног аиста». По мере прогрессирования патологии формируются типичные деформации стоп: высокий свод (pes cavus), молоткообразные пальцы и признаки косолапости, обусловленные атрофией мелких мышц стопы[16][13]. Клинически эти изменения проявляются слабостью в дистальных отделах ног, опущением стопы (степпаж), изменением походки с высоким подниманием колен и невозможностью ходьбы на пятках, что в совокупности формирует характерную неврологическую симптоматику, существенно ограничивающую двигательные возможности пациентов[15].
В ряде случаев заболевание дебютирует с сенсорных расстройств, включая болевые ощущения, парестезии (покалывание, «ползание мурашек») в стопах и голенях, а по мере прогрессирования развивается постепенное снижение всех видов чувствительности (болевой, температурной, тактильной). Определяются нарушения поверхностной чувствительности по периферическому типу («тип перчаток и носков»)[14][15].
Через несколько лет после появления первых признаков поражения нижних конечностей симметричные атрофические изменения распространяются на кисти и предплечья, затрагивая мышцы тенара, гипотенара и другие мелкие мышцы кистей. Это приводит к выраженным нарушениям мелкой моторики. При тяжёлом течении заболевания развиваются типичные деформации кистей по типу «когтистой» или «обезьяньей» лапы. Одновременно отмечается диффузное снижение мышечного тонуса в дистальных отделах конечностей. Характерной особенностью является неравномерное выпадение глубоких рефлексов: ахилловы рефлексы исчезают на ранних стадиях, тогда как коленные и рефлексы с мышц плеча могут длительное время оставаться сохранными. Часто имеются вегетативно-трофические на рушения — гипергидроз и гиперемия кистей и стоп[14][15].
- Биохимический анализ крови для оценки активности креатинфосфокиназы и лактатдегидрогеназы (маркеры вторичного вялотекущего рабдомиолиза)[17];
- Генетическое исследование позволяет окончательно диагностировать НМСН, выявляя специфические мутации[15];
- Гистологическое исследование икроножного нерва позволяет выявить гиперплазия шванновских клеток с формированием характерного морфологического признака «луковичные головки»[18].
- ЭМГ позволяет оценить скорость прохождения электрических импульсов (СПИ) по нервам. Пороговым значением СПИ по двигательным волокнам срединного нерва считается 38 м/с. ЭМГ-исследование позволяет подтвердить нейропатию, дифференцируя её с переднероговыми поражениями и миопатиями, определить тип нейропатии (аксональная/демиелинизирующая), оценить степень денервации и преимущественное поражение сенсорных или моторных волокон[7].
Дифференциальная диагностика
- Идиопатическая деформация стопы (полая стопа);
- Атаксия Фридрейха;
- Болезнь Рефсума;
- Болезнь Краббе;
- Дистальная миопатия Говерса—Веландер;
- Наследственная дистальная спинальная амиотрофия;
- Миотоническая дистрофия;
- Периферические интоксикационные невропатии;
- Инфекционные полиневриты[15][19].
Осложнения
Частые осложнения:
Лечение
В настоящее время специфическая терапия НМСН отсутствует, в связи с чем лечение носит исключительно симптоматический характер. Несмотря на отсутствие этиотропного лечения, современные методы симптоматической терапии и реабилитации позволяют существенно замедлить прогрессирование заболевания и улучшить функциональные возможности пациентов[20] .
Лечение остаётся в основном симптоматическим. Болевой синдром, связанный с костно-мышечными нарушениями, купируется парацетамолом или НПВС, тогда как нейропатическая боль может требовать назначения трициклических антидепрессантов, карбамазепина, габапентина или прегабалина. При хронической усталости применяют модафинил. Одним из перспективных препаратов является PXT3003 — комбинация баклофена, налтрексона и D-сорбитола. Клинические исследования показали его способность снижать нейротоксические эффекты избыточной экспрессии PMP22. Хотя значимого улучшения по шкалам CMTNS и ONLS зафиксировано не было, препарат продемонстрировал хорошую переносимость и безопасность[21][22].
Реабилитация направлена на сохранение двигательных функций и замедление прогрессирования заболевания. Основу составляют дозированные физические нагрузки, включающие аэробные упражнения, укрепляющие упражнения, направленные на компенсацию слабости дистальных мышц, а также проприоцептивные тренировки, направленные на контроль равновесия и походки. Не менее важны регулярные растяжки для профилактики контрактур, упражнения на мелкую моторику[21][22].
Ортопедическое лечение показано при контрактурах конечностей, умеренной деформации позвоночника и асимметричном укорочении конечностей[15].
Коррекция ортопедических нарушений начинается с подбора индивидуальных стелек, которые позволяют равномерно распределить нагрузку на стопу, уменьшая давление на опорные поверхности и тем самым предотвращая прогрессирование деформаций и снижая болевой синдром. При развитии слабости икроножных мышц и формировании свисающей стопы показано использование ортезов голеностопного сустава. Основное терапевтическое действие ортезов заключается в фиксации стоп в физиологическом положении и коррекции свода стопы. Дополнительными эффектами являются равномерное распределение нагрузки по всей нижней конечности и разгрузка дистальных отделов[18][22].
Своевременное проведение хирургической коррекции позволяет существенно замедлить развитие каво-варусных деформаций стоп и предотвратить формирование контрактур мягких тканей. На ранних стадиях заболевания гибкие деформации, включая конскую, каву или вальгусную деформацию передней части стопы и варусную деформацию задней части стопы, можно исправить с помощью остеотомий, щадящих суставы. Подобные оперативные вмешательства, выполненные в ранние сроки, способны не только устранить существующие деформации, но и предотвратить их прогрессирование с последующим развитием анкилозов в отдалённом периоде[22].
Прогноз
В большинстве случаев прогноз заболевания благоприятный[15] .
Примечания
Литература
- Паевский А.С., Хоружая А.Н. Болезнь Шарко-Мари-Тута // Вообще Чума! История болезней от лихорадки до Паркинсона. — Москва : Издательство АСТ, 2018. — 320 с. — (Научпоп Рунета).